Clear Sky Science · fr
La signalisation guanosine monophosphate cyclique-protéine kinase G atténue la calcification de la valve aortique via l’autophagie médiée par ULK1
Pourquoi la « rouille » des valves cardiaques compte
Avec l’âge, la valve aortique — la principale porte de sortie du cœur — peut lentement se raidir et s’entartrer de calcium, une affection appelée maladie calcifiante de la valve aortique. Cet « induration » oblige le cœur à pomper plus fort et peut entraîner des douleurs thoraciques, des syncopes, une insuffisance cardiaque ou la nécessité d’une chirurgie de remplacement valvulaire. Aujourd’hui, il n’existe pas de médicament qui ralentisse de façon fiable ce processus ; les médecins ne peuvent que patienter jusqu’à ce que la valve soit gravement endommagée puis opérer. Cette étude explore une voie cellulaire intrinsèque qui semble protéger la valve contre la calcification, et teste un médicament moderne utilisé en insuffisance cardiaque comme moyen potentiel de réactiver cette protection.
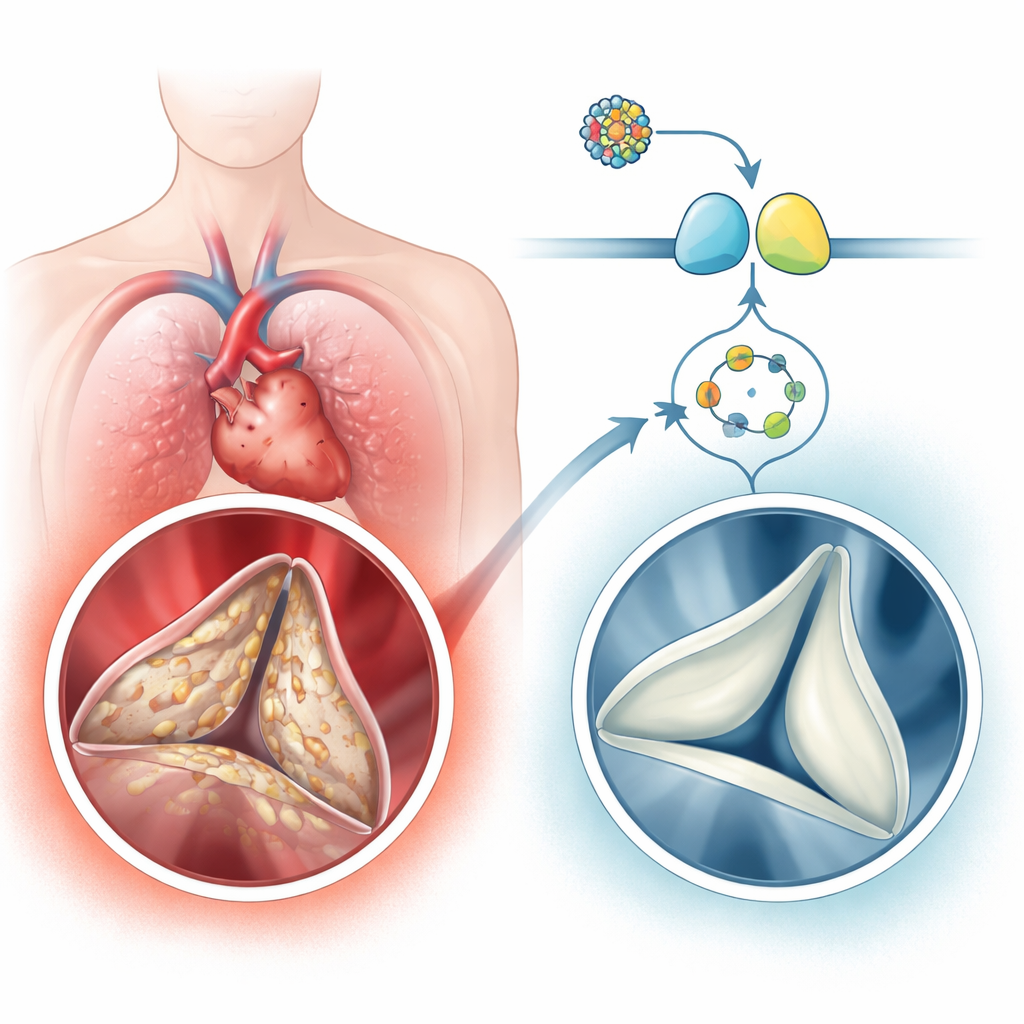
Un problème cardiaque courant mais négligé
La maladie calcifiante de la valve aortique est étonnamment fréquente chez les personnes âgées, touchant quelques pourcents des plus de 65 ans et jusqu’à une personne sur dix après 75 ans. La maladie n’est pas un simple « usure » passive. Les cellules du tissu conjonctif souple de la valve, appelées cellules interstitielles valvulaires, se transforment en états de cicatrisation et de type osseux. Elles déposent du collagène supplémentaire, puis du calcium, transformant les feuillets autrefois flexibles en lamelles dures comme la roche. Les auteurs ont analysé des tissus valvulaires humains et de larges jeux de données d’expression génique et ont constaté qu’une voie de signalisation centrée sur une petite molécule nommée cGMP et son enzyme partenaire, la protéine kinase G (PKG), était systématiquement atténuée dans les valves calcifiées, tandis que les gènes et protéines liés à la formation osseuse étaient augmentés. Les personnes présentant une calcification valvulaire sévère avaient également des niveaux de cGMP plus faibles dans le sang, corrélés avec le degré de rétrécissement et d’obstruction valvulaire.
Un signal protecteur qui disparaît
Pour examiner la causalité, l’équipe a utilisé des souris et des cellules valvulaires humaines en culture. Des souris génétiquement modifiées pour produire moins de PKG ont développé des feuillets valvulaires plus épais et davantage calcifiés après une lésion contrôlée de la valve aortique, et leurs valves présentaient des niveaux plus élevés d’une protéine maîtresse de formation osseuse. Dans des cellules valvulaires humaines cultivées en conditions favorisant l’accumulation de calcium, l’inhibition de PKG par des outils génétiques a accéléré cette transformation de type osseux. Ces résultats suggèrent que la signalisation cGMP‑PKG agit normalement comme un frein à la reprogrammation cellulaire néfaste dans la valve — et quand ce frein faiblit, la calcification s’accélère.
Réaffecter un médicament contre l’insuffisance cardiaque
Les chercheurs se sont ensuite demandé si stimuler cette voie pouvait ralentir ou inverser la calcification. Ils ont testé trois médicaments qui augmentent le cGMP par des mécanismes différents, dont le vericiguat, un médicament approuvé pour certains patients en insuffisance cardiaque. Dans des cellules valvulaires humaines, les trois médicaments ont réduit les dépôts calciques et les marqueurs de transformation osseuse, le vericiguat ayant l’effet le plus marqué. Le vericiguat a également diminué la calcification dans de petits fragments de valve humaine maintenus vivants hors du corps. Dans deux modèles murins — l’un induit par un régime riche en cholestérol et l’autre par une blessure mécanique de la valve — un traitement quotidien par vericiguat a conduit à des feuillets plus minces, moins calcifiés et à une meilleure circulation sanguine à travers la valve, sans affaiblir la puissance de contraction cardiaque. Lorsque PKG était réduit génétiquement, toutefois, le vericiguat perdait en grande partie ses bénéfices, indiquant que PKG est l’acteur clé en aval.
Ménage cellulaire, valves plus saines
En approfondissant, l’équipe a découvert que le vericiguat et la PKG protégeaient les petites centrales énergétiques des cellules valvulaires, les mitochondries. Dans des conditions de calcification, les cellules accumulaient des espèces réactives d’oxygène nocives, perdaient le potentiel de la membrane mitochondriale et produisaient moins d’énergie. Le vericiguat a restauré la fonction mitochondriale et réduit le stress oxydatif. Des cartographies à grande échelle des protéines et des sites de phosphorylation les ont orientés vers l’autophagie — le système interne de nettoyage et de recyclage de la cellule. Dans les valves humaines calcifiées, l’imagerie microscopique et les marqueurs protéiques ont montré une réduction de la formation et de l’activité des autophagosomes, les « sacs-poubelle » de l’autophagie. Dans des analyses monocellulaires, plusieurs sous-types de cellules valvulaires provenant de valves malades présentaient une vaste suppression des programmes liés à l’autophagie. In vitro, le blocage de l’autophagie a effacé l’effet protecteur de l’activation de PKG, ce qui implique que PKG agit en grande partie en ravivant ce système de nettoyage.
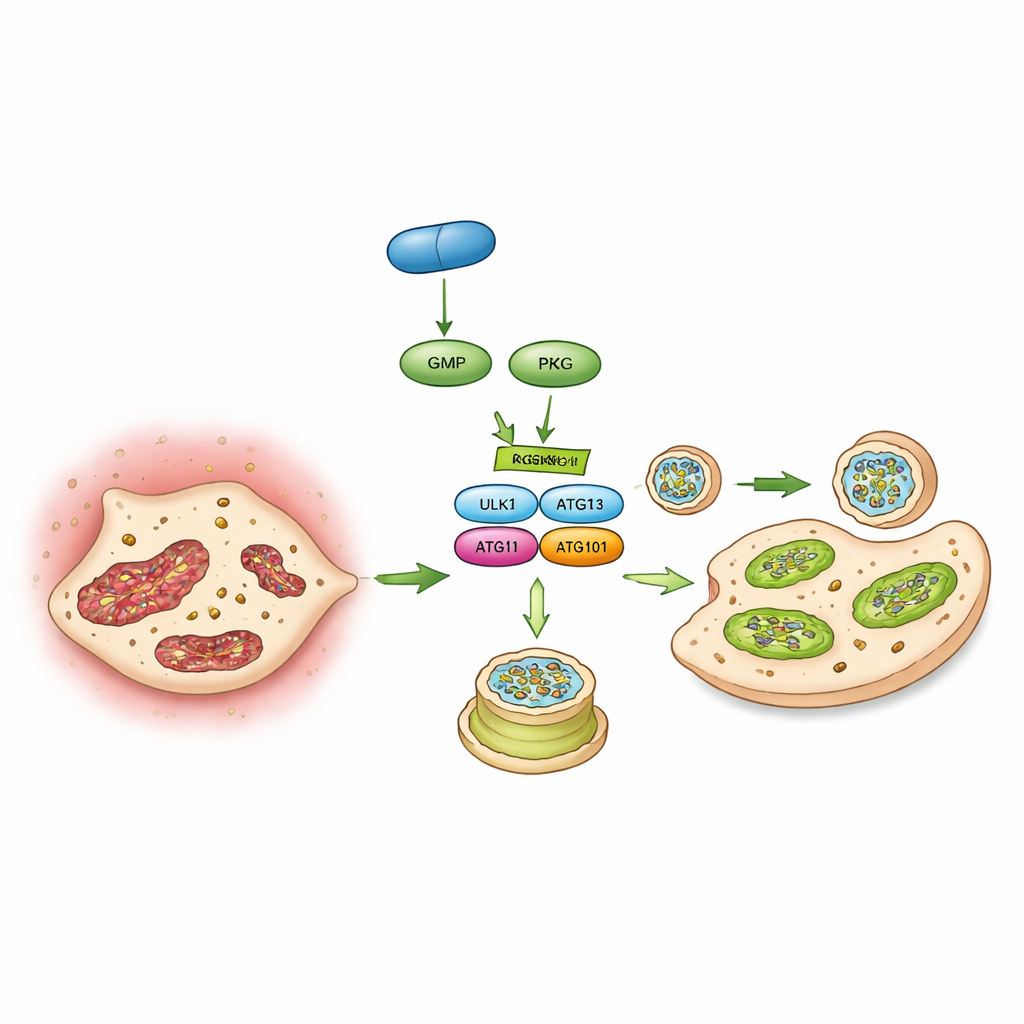
Inverser un interrupteur moléculaire
Enfin, les auteurs ont identifié un interrupteur moléculaire spécifique reliant PKG à l’autophagie : une protéine appelée ULK1 qui lance la formation des autophagosomes. À l’aide de phosphoprotéomique, d’études d’interaction et d’essais de kinase en tube à essai, ils ont montré que PKG ajoute directement un groupe phosphate à ULK1 à un site particulier (un acide aminé nommé sérine 556). Lorsque ce site était muté de sorte qu’il ne puisse plus être modifié, PKG n’a plus pu stimuler l’autophagie ni bloquer la calcification dans les cellules valvulaires. Chez la souris, l’expression dirigée de ce mutant ULK1 non réactif dans les cellules valvulaires a également annulé la capacité du vericiguat à protéger la valve. Ensemble, ces résultats décrivent une chaîne d’événements : le vericiguat stimule le cGMP, qui active la PKG, qui bascule l’interrupteur ULK1, qui ranime l’autophagie, qui préserve les mitochondries et empêche les cellules valvulaires de se transformer en cellules productrices d’os.
Ce que cela pourrait signifier pour les patients
Ce travail place l’axe cGMP–PKG–ULK1–autophagie comme un système de défense intrinsèque contre la « rouille » de la valve aortique. Dans la maladie valvulaire calcifiante, cette défense est affaiblie, permettant aux cellules d’accumuler des dommages et de dériver vers une identité de type osseux. En restaurant pharmacologiquement le signal avec un médicament déjà utilisé en clinique pour l’insuffisance cardiaque, les chercheurs ont ralenti la calcification dans plusieurs modèles expérimentaux. Si des essais chez l’homme dans la maladie valvulaire seront nécessaires, l’étude propose une idée claire et testable : stimuler avec précaution cette voie de nettoyage cellulaire pourrait, un jour, retarder ou réduire le besoin de chirurgie de remplacement valvulaire chez les adultes âgés à risque de sténose aortique.
Citation: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
Mots-clés: maladie calcifiante de la valve aortique, signalisation cGMP PKG, vericiguat, autophagie, calcification des valves cardiaques