Clear Sky Science · fr
Efficacité et effet immunomodulateur des cellules CAR-T armées spécifiques de Claudin18.2 exprimant IL-7/XCL1 dans les cancers du tube digestif : analyse préclinique et clinique
Retourner le système immunitaire contre les cancers digestifs
Les cancers de l’estomac et du pancréas figurent parmi les tumeurs les plus mortelles, en partie parce qu’ils résistent souvent à la chirurgie, à la chimiothérapie et à la radiothérapie. Cette étude explore une nouvelle façon de combattre ces cancers en suralimentant les propres cellules immunitaires de l’organisme afin qu’elles pénètrent dans les tumeurs solides, y survivent et appellent des renforts. En reprogrammant des lymphocytes T anti-cancer pour qu’ils libèrent des signaux immunitaires bénéfiques, les chercheurs visent non seulement à attaquer les tumeurs directement, mais aussi à réveiller le reste du système immunitaire au sein du quartier hostile de la tumeur.
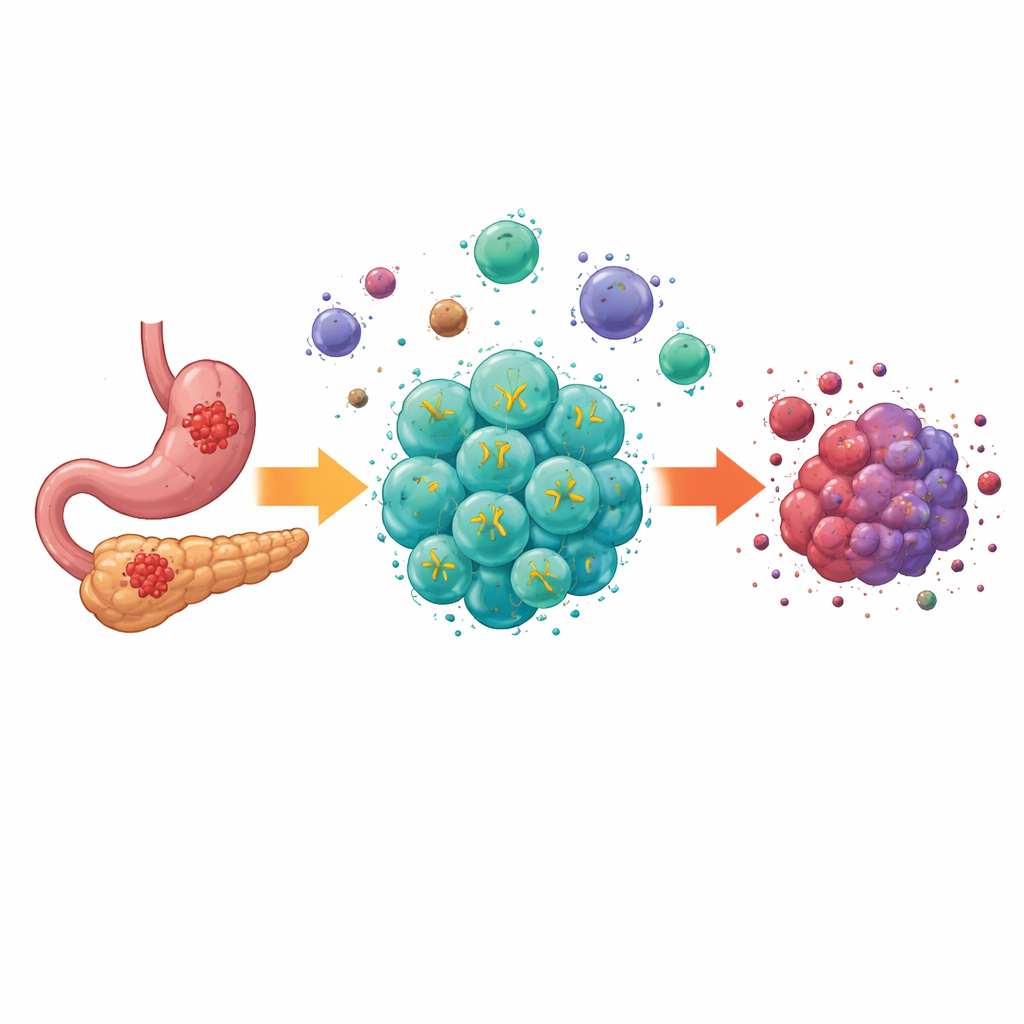
Pourquoi les tumeurs solides sont difficiles à traiter
Les thérapies cellulaires modernes appelées CAR-T ont produit des résultats spectaculaires dans les cancers du sang, en guérissant certains patients sans autre option. Mais les tumeurs solides, comme celles du tube digestif, présentent des obstacles supplémentaires. Leurs cellules varient d’un site à l’autre, l’intérieur de la tumeur est pauvre en nutriments et en oxygène, et un mélange de cellules et de molécules suppressives atténue les attaques immunitaires. Les générations précédentes de CAR-T pouvaient reconnaître des molécules cibles sur les cellules des cancers digestifs, mais elles échouaient souvent à se développer, à persister et à fonctionner dans cet environnement hostile, limitant leur impact en pratique clinique.
Une conception plus intelligente pour les lymphocytes T génétiquement modifiés
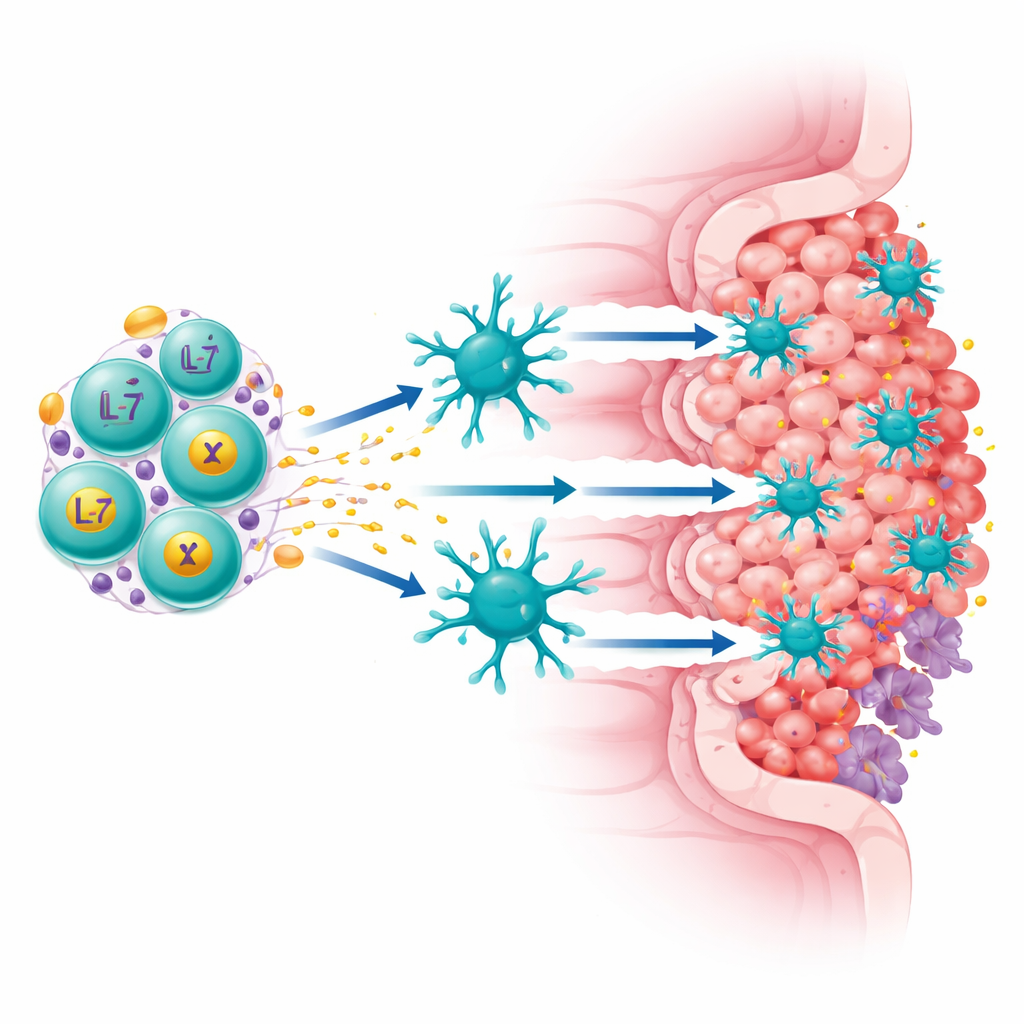
L’équipe s’est concentrée sur une protéine appelée Claudin18.2, exprimée à des niveaux élevés sur de nombreuses cellules de cancers gastriques et pancréatiques mais largement absente des tissus normaux. Ils ont construit une cellule CAR-T de « quatrième génération » qui remplit deux fonctions à la fois : elle reconnaît Claudin18.2 sur les cellules tumorales et sécrète en continu deux facteurs immunostimulants, IL-7 et XCL1. L’IL-7 aide les lymphocytes T à survivre et à conserver un état longuement persistant de type « stem-like », tandis que XCL1 agit comme un signal attirant un type rare mais puissant de cellules immunitaires appelées cDC1, particulièrement efficaces pour activer les lymphocytes T cytotoxiques. Ces cellules améliorées, appelées ExCAR-T ou RD07, sont conçues non seulement pour tuer ce qu’elles voient mais aussi pour remodeler le paysage immunitaire de la tumeur.
Contrôle tumoral puissant dans les modèles précliniques
Dans des modèles murins de cancers digestifs, les ExCAR-T ont surpassé les CAR-T conventionnels dépourvus d’IL-7 et de XCL1. In vitro, les cellules modifiées ont tué davantage de cellules cancéreuses et présenté plus de lymphocytes T mémoire de longue durée. Chez des animaux portant des tumeurs Claudin18.2-positives, le traitement ExCAR-T a fait régresser les tumeurs plus profondément et prolongé la survie comparé aux CAR-T standards. Les cellules améliorées se sont mieux développées dans le sang et ont déclenché une activité immunitaire plus large, incluant des signaux recrutant des cellules immunitaires additionnelles tout en réduisant des facteurs liés à la dissémination tumorale. Fait marquant, les souris guéries par ExCAR-T ont rejeté un deuxième défi par des cellules tumorales ne portant plus la cible Claudin18.2, indiquant que la thérapie avait suscité une mémoire immunitaire durable et globale plutôt qu’une réponse étroite dirigée contre une seule cible.
Résultats précoces d’un essai clinique chez l’homme
Encouragés par ces données, les chercheurs ont lancé un essai de première-injection humaine du RD07 chez 12 personnes atteintes de cancers avancés de l’estomac, de la jonction gastro-œsophagienne ou du pancréas, ayant déjà échoué aux traitements standards. Les effets indésirables étaient généralement gérables : les problèmes graves étaient surtout des baisses des chiffres sanguins liées à la chimiothérapie pré-infusée, et seules des réactions légères de libération de cytokines ont été observées ; aucune toxicité cérébrale grave n’a été rapportée. Parmi 10 patients évaluables, 7 ont présenté une réduction mesurable des tumeurs et 2 ont obtenu des réponses partielles. Les patients dont les tumeurs présentaient des niveaux modérés à élevés de Claudin18.2 ont particulièrement bien répondu, chaque patient de ce groupe bénéficiant au minimum d’une stabilisation de la maladie et certains vivant de nombreux mois de plus que prévu. Chez ces répondeurs, les lymphocytes T modifiés se sont développés plus fortement dans le sang et les taux sanguins d’IL-7 et de XCL1 ont augmenté, conformément au principe du traitement.
Explorer le microenvironnement immunitaire tumoral
Pour comprendre comment RD07 agit chez l’homme, l’équipe a examiné des échantillons tumoraux à résolution unicellulaire avant et après le traitement. Ils ont constaté que la proportion de cellules cancéreuses positives pour Claudin18.2 diminuait chez les patients répondeurs, confirmant que la thérapie atteignait sa cible. Simultanément, une augmentation de clones T divers a été observée, incluant des cellules cytotoxiques actives et des cellules mémoire tissulaires résidentes, ce qui suggère que l’organisme montait une offensive immunitaire plus large. Les cellules dendritiques spécialisées montraient des signes d’activité accrue et d’interactions renforcées avec des lymphocytes T en prolifération, cohérent avec le rôle de XCL1 pour les attirer dans la tumeur. Des études d’imagerie d’une coupe tumorale d’un patient ont révélé moins de cellules tumorales et de myéloïdes suppressifs après traitement, avec davantage de lymphocytes T et B et une réorganisation du tissu en zones riches en cellules immunitaires, signes d’un microenvironnement « chauffé » et plus inflammatoire.
Ce que cela pourrait signifier pour la prise en charge future du cancer
Pris ensemble, les résultats précliniques et cliniques précoces suggèrent que RD07 fait plus qu’ajouter un nouveau médicament ciblé à l’arsenal anticancéreux. En combinant reconnaissance tumorale et soutien immunitaire intégré, ces lymphocytes T génétiquement modifiés peuvent survivre plus longtemps, recruter des cellules partenaires clés et contribuer à entraîner le système immunitaire du patient à garder le cancer sous contrôle, même lorsque la cible initiale est perdue. Bien que l’essai soit petit et réalisé chez des patients fortement prétraités, la régression tumorale cohérente, la tolérance acceptable et le profond remodelage immunitaire sont prometteurs. Si ces résultats sont confirmés dans des études plus larges, cette approche pourrait ouvrir un nouveau chapitre dans le traitement des cancers du tube digestif, où l’empowerment de l’écosystème immunitaire intratumoral devient aussi important que le coup initial porté aux cellules cancéreuses elles-mêmes.
Citation: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
Mots-clés: Thérapie par cellules CAR-T, cancer du tube digestif, microenvironnement tumoral, Claudin18.2, immunothérapie