Clear Sky Science · fr
La protéine de type Visinin 1 perturbe l’homéostasie du calcium et favorise la fibrillation atriale chez l’humain et chez les rongeurs
Pourquoi cette histoire de rythme cardiaque compte
La fibrillation atriale est un trouble fréquent du rythme cardiaque qui augmente le risque d’accident vasculaire cérébral et d’insuffisance cardiaque. Beaucoup de personnes en vivent, et pourtant les médecins peinent encore à la prévenir ou à éviter les récidives après traitement. Cette étude met en lumière une protéine jusqu’ici négligée dans les cellules cardiaques, appelée VILIP-1, qui agit comme un commutateur calcique défaillant et contribue à la fibrillation atriale chez l’homme et les animaux. En identifiant ce commutateur et en montrant que des médicaments existants peuvent en réduire l’activité, ce travail ouvre une voie nouvelle vers des thérapies plus sûres et plus ciblées.
Un regard approfondi sur un battement chaotique
Dans un cœur sain, les ondes électriques se propagent de manière ordonnée à travers les cavités supérieures, ou oreillettes, guidant chaque battement. Cet ordre dépend largement du calcium, un ion qui entre et sort des cellules cardiaques pour coordonner contraction et relaxation. Dans la fibrillation atriale, ce trafic calcique devient anarchique : des fuites supplémentaires et des variations de concentration déclenchent des signaux électriques parasites qui peuvent dégénérer en rythmes rapides et irréguliers. Les médecins savent depuis des années que le mauvais contrôle du calcium est central dans ce trouble, mais les déclencheurs en amont qui initient ce chaos restaient flous.
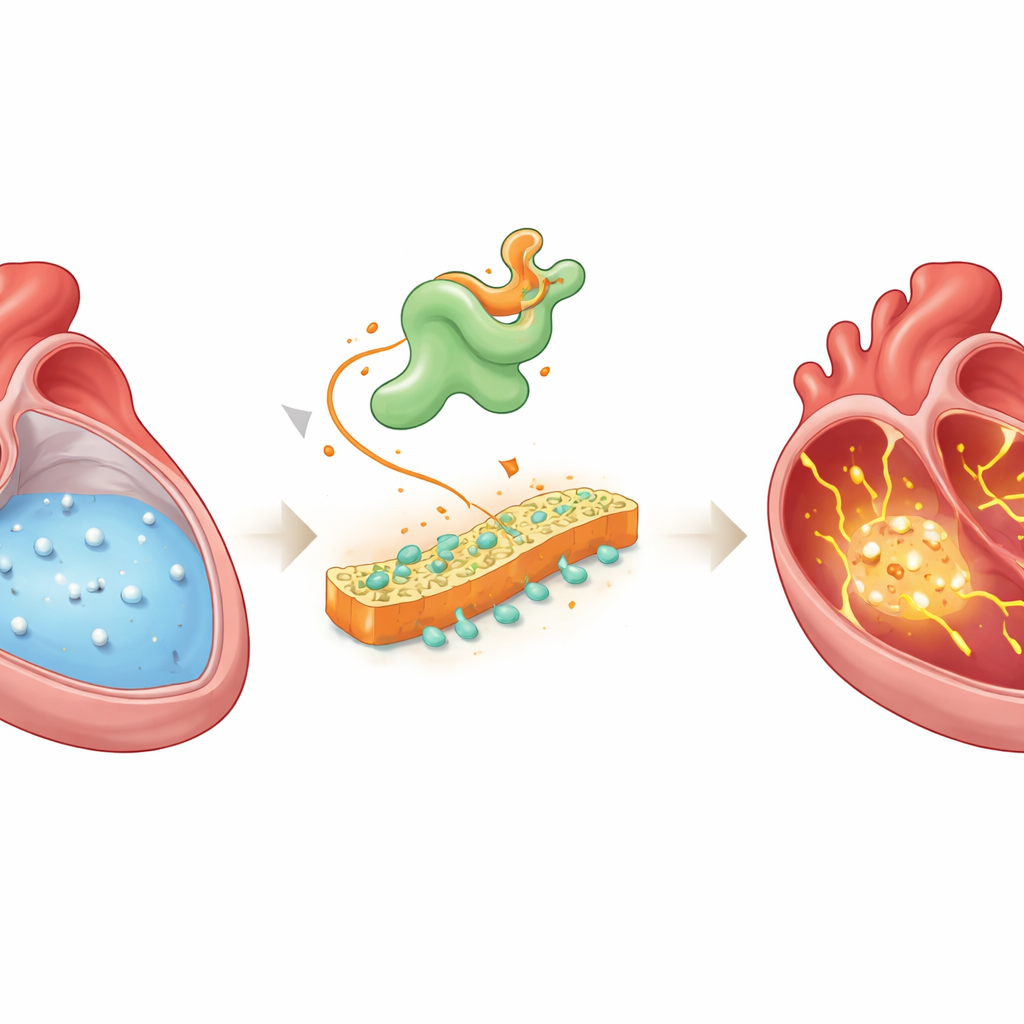
Découverte d’un perturbateur caché
Les chercheurs ont combiné plusieurs approches avancées pour rechercher des molécules reliant la perturbation du calcium à la fibrillation atriale. Ils ont enregistré les signaux calciques de centaines de cellules atriales individuelles chez des rats soumis à un rythme induit, puis séquencé l’ensemble des gènes exprimés dans ces mêmes cellules. Ils ont également comparé l’activité génique dans le tissu atrial de patients atteints de fibrillation atriale à celle de patients au rythme normal. En superposant ces jeux de données et en retraçant l’évolution des cellules du stade sain au stade pathologique, un gène est revenu de façon récurrente : Vsnl1, qui code la protéine VILIP-1, un détecteur de calcium étudié auparavant surtout dans le cerveau et le pancréas, mais pas dans le cœur.
Comment VILIP-1 perturbe l’équilibre calcique
Dans les tissus atriaux de patients et de modèles animaux, les niveaux de VILIP-1 étaient significativement augmentés et la protéine se localisait à la surface des cellules. Pour déterminer si ce changement était un simple témoin ou un moteur de la pathologie, l’équipe a forcé des cellules atriales de souris à produire un excès de VILIP-1. Ces souris n’ont pas montré de lésion structurelle évidente du cœur, mais leurs oreillettes sont devenues beaucoup plus faciles à déclencher en fibrillation atriale lors d’un pacing électrique. Des enregistrements électriques détaillés ont révélé davantage de dépolarisations retardées après le potentiel d’action — des impulsions anormales après chaque battement — et des alternances battement par battement de la forme du potentiel d’action, signatures classiques d’un comportement électrique instable associé à une surcharge calcique. L’imagerie calcique haute résolution a confirmé la présence fréquente d’ondes calciques spontanées et l’épuisement des réserves calciques internes, indiquant des fuites sévères à l’intérieur des cellules.
Le partenaire critique à la surface cellulaire
Pour comprendre comment VILIP-1 provoque cette perturbation, les scientifiques ont cartographié les protéines qui interagissent avec elle dans les cellules cardiaques. En utilisant deux méthodes complémentaires — l’extraction des partenaires d’interaction à partir de tissu atrial et le marquage des protéines voisines par une « auréole » de biotine dans des cellules vivantes — ils ont identifié NCX-1, le principal échangeur sodium–calcium de la membrane superficielle cardiaque. Cet échangeur aide normalement à expulser le calcium en échange de sodium, mais dans certaines conditions il peut fonctionner en sens inverse et faire entrer du calcium dans la cellule. L’étude a montré que VILIP-1 se lie physiquement à NCX-1 et augmente le nombre de molécules de NCX-1 intégrées à la membrane sans accroître la production totale de NCX-1. En résultat, les courants de l’échangeur sont devenus plus importants, et le blocage de NCX-1 par un inhibiteur sélectif a réduit les ondes calciques et rendu la fibrillation atriale plus difficile à provoquer chez les souris surexprimant VILIP-1.
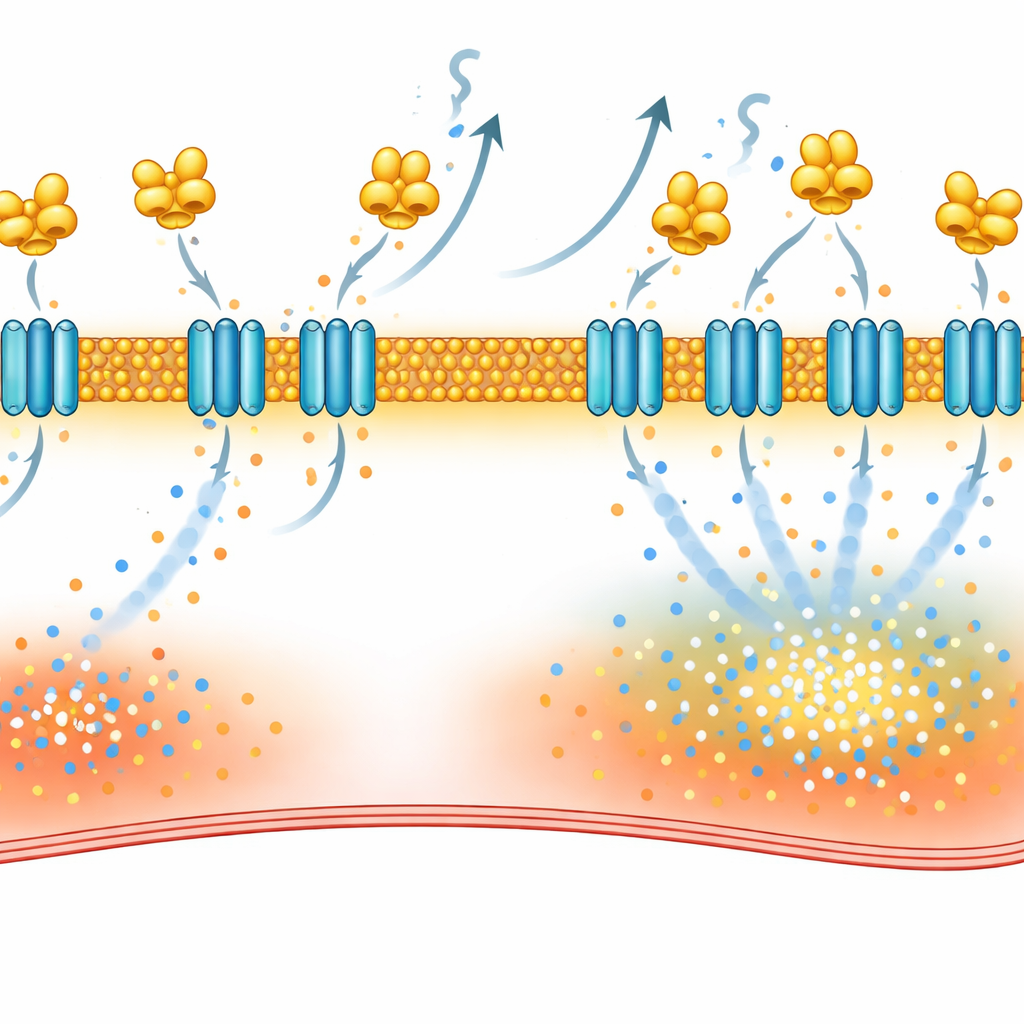
Éteindre le commutateur défectueux avec des médicaments existants
VILIP-1 s’ancre aux membranes via une chaîne lipidique appelée myristate, qui devient exposée lorsque le calcium se lie à la protéine. L’équipe a utilisé la desloratadine, déjà montrée capable d’interférer avec cette étape d’ancrage, et a constaté qu’elle réduisait la présence de NCX-1 à la surface cellulaire, normalisait les courants de l’échangeur, diminuait les ondes calciques et réduisait les épisodes de fibrillation atriale dans des modèles de rat. Ils ont aussi testé la répaglinide, un médicament antidiabétique connu pour se lier à des capteurs calciques apparentés. Des essais biophysiques ont confirmé que la répaglinide se fixe directement à VILIP-1. Chez des rats soumis à pacing et dans du tissu atrial de patients atteints de fibrillation atriale, le traitement par la répaglinide a réduit NCX-1 au niveau de la membrane, atténué les fuites calciques dans les cellules individuelles et diminué de façon notable la facilité d’induction de la fibrillation atriale.
Ce que cela signifie pour les personnes souffrant d’un rythme irrégulier
Au total, l’étude décrit une boucle autorenforçante : l’élévation du calcium attire VILIP-1 à la surface cellulaire, où il augmente NCX-1, ce qui à son tour favorise une surcharge calcique supplémentaire et prépare le terrain pour la fibrillation atriale. En interrompant cette boucle au niveau de VILIP-1 — soit en bloquant son ancrage lipidique, soit en ciblant son domaine de détection du calcium — des médicaments existants peuvent restaurer un équilibre calcique plus stable et réduire la vulnérabilité aux arythmies dans les tissus cardiaques humains et de rongeurs. Bien que des travaux supplémentaires soient nécessaires pour affiner la spécificité des médicaments et tester ces stratégies dans des modèles animaux plus grands et dans des essais cliniques, VILIP-1 apparaît désormais comme une nouvelle cible prometteuse pour prévenir et traiter ce trouble du rythme cardiaque, fréquent et souvent tenace.
Citation: Xiong, K., Wang, G., Li, D. et al. Visinin-like protein 1 disrupts calcium homeostasis and promotes atrial fibrillation in human and rodent models. Sig Transduct Target Ther 11, 105 (2026). https://doi.org/10.1038/s41392-026-02615-6
Mots-clés: fibrillation atriale, signalisation calcique, arythmie cardiaque, échangeur sodium-calcium, cibles thérapeutiques