Clear Sky Science · fr
SHR-A1811, un nouvel conjugué anticorps‑médicament ciblant HER2, dans les tumeurs solides avancées (HORIZON‑X) : un essai mondial de phase 1
Un nouvel espoir pour des personnes à court d’options
Pour de nombreuses personnes atteintes d’un cancer avancé, les traitements standards finissent par ne plus fonctionner, laissant peu d’alternatives satisfaisantes. Cette étude évalue un nouveau type de médicament ciblé, SHR‑A1811, chez des patients dont les tumeurs présentent des copies supplémentaires ou des mutations du signal de croissance connu sous le nom de HER2. Ces patients avaient déjà reçu plusieurs lignes de traitement. La question principale était de savoir si ce médicament expérimental pouvait réduire les tumeurs durablement sans provoquer d’effets indésirables dangereux.
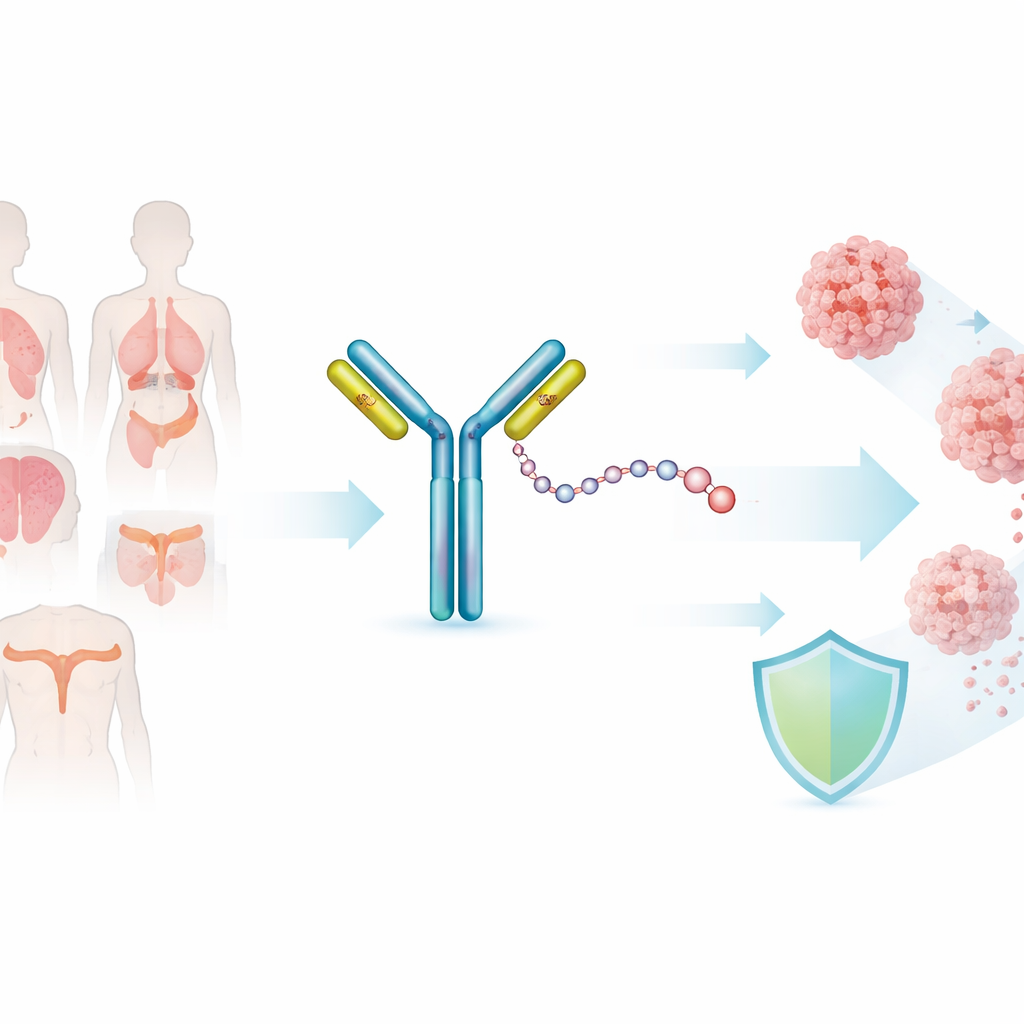
Un missile intelligent dirigé contre les cellules cancéreuses
SHR‑A1811 appartient à une classe plus récente de traitements appelés conjugués anticorps‑médicament, parfois décrits comme des « missiles intelligents ». Une partie du médicament est un anticorps qui reconnaît HER2, une protéine présente en forte quantité à la surface de certaines cellules cancéreuses. L’autre partie est une chimiothérapie très puissante, trop toxique pour être administrée seule. Un lien chimique spécial assemble ces éléments. L’idée est que l’anticorps transporte la charge toxique directement vers les cellules tumorales marquées par HER2, où elle est libérée à l’intérieur du cancer tout en épargnant une grande partie des tissus sains.
Qui a reçu le nouveau traitement
Cet essai mondial de phase 1 a recruté 396 adultes atteints de tumeurs solides avancées ou métastatiques dans 38 hôpitaux. Toutes les tumeurs produisaient soit un excès de HER2, soit portaient des mutations de HER2. La majorité des patients souffraient d’un cancer du sein, mais d’autres présentaient des cancers des voies biliaires, de la vessie, des ovaires et de l’utérus, du côlon, de l’estomac, des poumons, du pancréas, et d’autres encore. En moyenne, les patients avaient déjà reçu trois à quatre schémas thérapeutiques pour maladie métastatique, ce qui signifie que leurs cancers étaient difficiles à contrôler. SHR‑A1811 était administré par perfusion intraveineuse toutes les trois semaines à des doses variables pour déterminer une dose appropriée et surveiller les problèmes de sécurité et les premiers signes d’efficacité.
Équilibrer effets secondaires et sécurité
Presque tous les patients ont présenté des effets indésirables, comme on pouvait s’y attendre avec des médicaments anticancéreux puissants. Les problèmes les plus fréquents étaient des baisses des chiffres sanguins, incluant les globules blancs, les globules rouges et les plaquettes, ce qui peut augmenter le risque d’infection et entraîner fatigue ou ecchymoses. Ces effets ont généralement été gérables par des ajustements de dose, et seulement environ un patient sur dix a interrompu le traitement à cause d’effets indésirables. Une préoccupation majeure pour des médicaments similaires est la fibrose et l’inflammation pulmonaire, pouvant mettre la vie en danger. Dans cette étude, les problèmes pulmonaires de toute gravité sont survenus chez seulement 2,5 % des patients, principalement légers ; un seul patient est décédé de cette complication à la dose la plus élevée. Globalement, le profil de sécurité est resté stable sur plus de deux ans de suivi, sans risques nouveaux ou inattendus émergents.
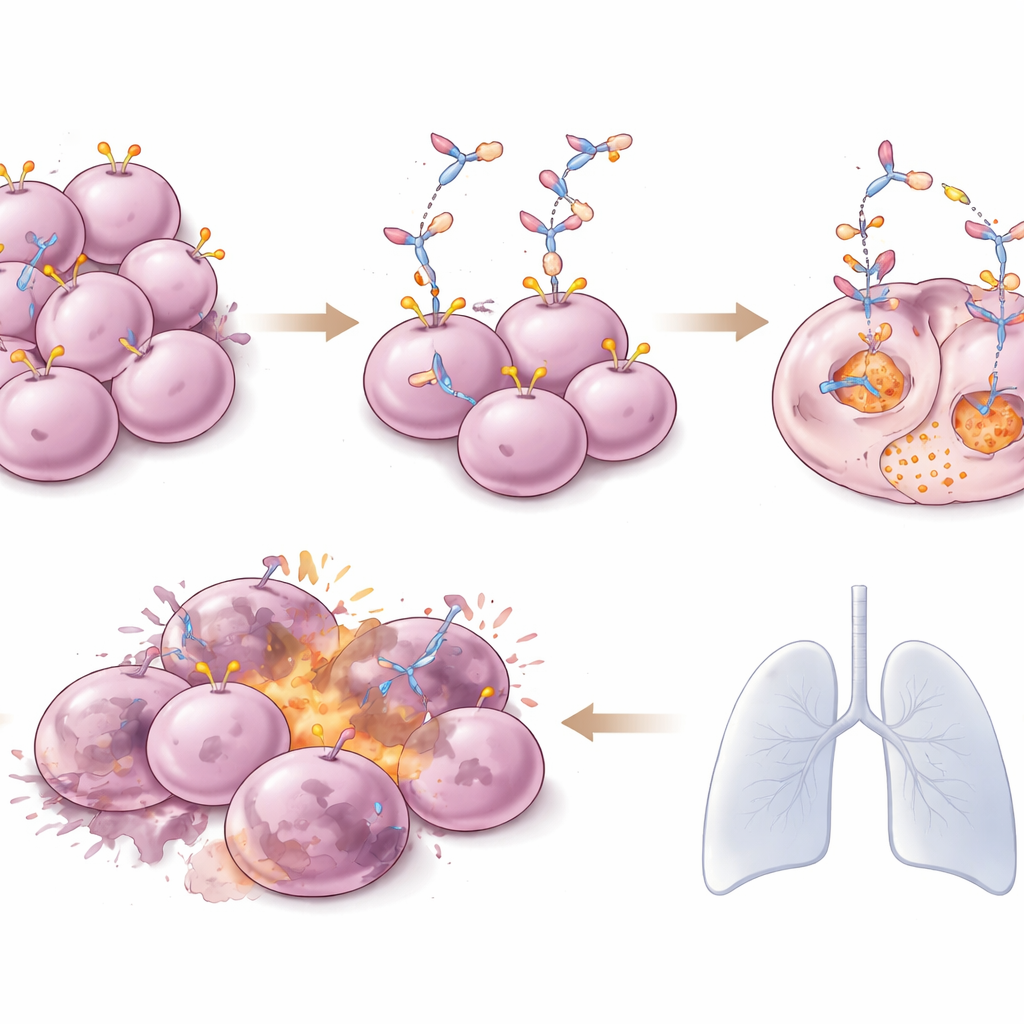
Réduction tumorale et contrôle prolongé
Les résultats sur le contrôle tumoral sont remarquables pour des patients aussi lourdement traités. Toutes tumeurs confondues, près de 60 % des patients ont vu leurs tumeurs diminuer, et certains ont présenté une disparition complète des lésions visibles aux examens d’imagerie. Chez les personnes atteintes d’un cancer du sein HER2‑positif, environ quatre sur cinq ont présenté une réduction tumorale, et le délai médian avant progression était légèrement supérieur à deux ans. Les patients dont les tumeurs mammaires présentaient des niveaux plus faibles de HER2 ont également bénéficié, avec un contrôle de la maladie durant en moyenne près d’un an. Pour les cancers non mammaires — y compris les voies biliaires, la vessie, les cancers gynécologiques, colorectaux, gastriques et pulmonaires — les réponses variaient mais restaient généralement encourageantes, de nombreux patients ayant bénéficié de plusieurs mois supplémentaires de contrôle de la maladie. Fait important, les réponses avaient tendance à se maintenir : parmi ceux dont les tumeurs ont diminué, beaucoup ont conservé le bénéfice pendant un an ou plus.
Atteindre des tumeurs à faible expression de la cible
Un résultat intrigant est que SHR‑A1811 a aidé certains patients dont les tumeurs présentaient très peu d’HER2 détectable — des niveaux traditionnellement considérés comme trop bas pour une thérapie ciblant HER2. Dans ce groupe, plus de la moitié ont quand même vu leurs tumeurs régresser, et le contrôle de la maladie a duré environ dix mois. Des travaux en laboratoire suggèrent que cela peut s’expliquer par le fait que la charge toxique, une fois libérée à l’intérieur d’une cellule marquée par HER2, peut diffuser vers les cellules cancéreuses voisines qui n’expriment pas ou peu HER2, un « effet bystander ». Cela laisse envisager que le médicament pourrait bénéficier à un éventail plus large de patients que ce que les définitions classiques de HER2‑positif indiquent.
Ce que cela signifie pour les personnes atteintes d’un cancer avancé
Dans l’ensemble, ce suivi à long terme de l’essai HORIZON‑X montre que SHR‑A1811 peut offrir un contrôle tumoral fort et durable chez de nombreux patients dont les cancers liés à HER2 avaient déjà résisté à de multiples traitements, tout en maintenant les effets indésirables graves — en particulier les atteintes pulmonaires — relativement rares. Bien qu’il ne s’agisse pas d’une comparaison directe, les résultats semblent au moins comparables à ceux d’un « missile intelligent » ciblant HER2 déjà approuvé, et parfois plus favorables, notamment sur le plan de la sécurité. Des essais randomisés plus larges sont encore nécessaires, mais les données actuelles suggèrent que SHR‑A1811 pourrait devenir une nouvelle option importante pour les patients atteints de cancers HER2‑dépendants difficiles à traiter.
Citation: Yao, H., Yan, M., Tong, Z. et al. SHR-A1811, a novel HER2-targeting antibody-drug conjugate, in advanced solid tumors (HORIZON-X): a global phase 1 trial. Sig Transduct Target Ther 11, 104 (2026). https://doi.org/10.1038/s41392-026-02612-9
Mots-clés: Thérapie ciblant HER2, conjugué anticorps‑médicament, cancer du sein métastatique, tumeurs solides, essai clinique