Clear Sky Science · fr
Signalisation fibrinogène–Bmal1 comme cible thérapeutique pour limiter la dissection aortique en préservant la contractilité des CMLV
Pourquoi le gardien caché de l’aorte compte
La dissection aortique est l’une des urgences les plus redoutées en médecine : la principale artère qui part du cœur peut se déchirer soudainement, souvent sans signe avant‑coureur, et de nombreux patients décèdent en quelques heures. La chirurgie peut sauver des vies, mais elle comporte des risques et n’est pas toujours réalisable immédiatement. Cette étude explore un allié inattendu déjà présent dans notre sang — le fibrinogène, une protéine de la coagulation — et montre que, au‑delà de son rôle pour arrêter les saignements, il pourrait en réalité aider à maintenir l’aorte et ralentir la maladie, offrant potentiellement aux cliniciens un temps précieux pour intervenir.
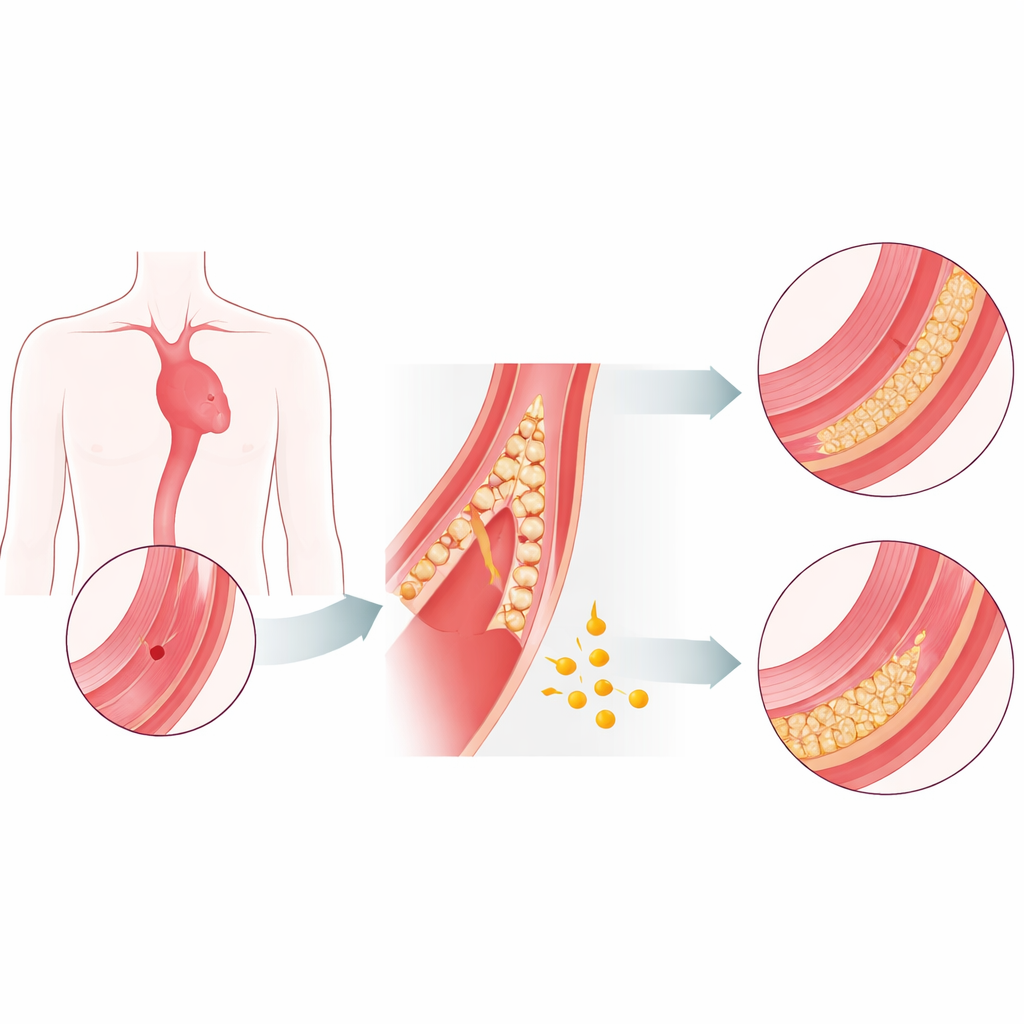
Un tueur silencieux qui manque d’options
L’aorte est construite comme un tuyau résistant à plusieurs couches. Lorsque ses couches internes s’affaiblissent et se séparent, le sang peut s’engouffrer dans la paroi et la déchirer — c’est la dissection aortique. Dans la phase dangereuse initiale, le risque de décès augmente heure après heure, et la chirurgie d’urgence est souvent la seule option. Les patients qui survivent suffisamment longtemps pour atteindre une phase chronique plus stable s’en sortent généralement beaucoup mieux. À ce jour, il n’existe pas de médicament prouvé capable de ralentir de façon fiable le processus de déchirure ou de renforcer la paroi aortique. Les auteurs ont cherché à savoir si le fibrinogène, une protéine sanguine courante surtout connue pour son rôle dans la coagulation, pourrait aussi agir comme un stabilisateur naturel de l’aorte.
Indices provenant des patients : plus de fibrinogène, meilleure survie
L’équipe a d’abord examiné 310 patients atteints d’une dissection aortique aiguë qui n’ont pas pu être opérés et ont été traités uniquement par des médicaments. Ils ont comparé ceux qui ont survécu à leur hospitalisation à ceux qui sont décédés. Les patients décédés présentaient en général des taux de fibrinogène sanguin beaucoup plus faibles. Lorsque les chercheurs ont regroupé les patients selon le taux de fibrinogène, ils ont constaté que des niveaux très bas (inférieurs à 2 grammes par litre) étaient associés à des taux de mortalité beaucoup plus élevés, tandis que des niveaux élevés (supérieurs à 4 grammes par litre) étaient liés à une meilleure survie. Ce schéma suggérait que le fibrinogène n’était pas simplement un spectateur, mais pouvait réellement aider l’aorte à résister à de nouvelles déchirures.
Observer la rupture et la réparation de l’aorte chez la souris
Pour dépasser l’association et tester la causalité, les scientifiques ont utilisé des modèles murins dans lesquels l’aorte peut être affaiblie et dissecquée. Chez ces animaux, le fibrinogène était normalement absent de la paroi aortique saine, mais à mesure que la maladie se développait, il commençait à s’infiltrer dans la couche moyenne où résident les cellules musculaires lisses. De manière frappante, l’accumulation la plus importante de fibrinogène apparaissait dans les segments sévèrement endommagés mais encore non rompus, suggérant que sa présence pouvait aider à empêcher la paroi de céder définitivement. Lorsque les chercheurs ont utilisé une thérapie génique pour réduire la production de fibrinogène par le foie, les dissections se sont aggravées : les aortes se sont davantage dilatées, les dommages structurels ont augmenté et davantage de souris sont mortes. La réinjection de fibrinogène purifié a inversé ces effets. Des expériences indépendantes utilisant un autre modèle d’anévrisme aortique ont montré une tendance protectrice similaire, renforçant l’idée que le fibrinogène protège activement la paroi vasculaire.
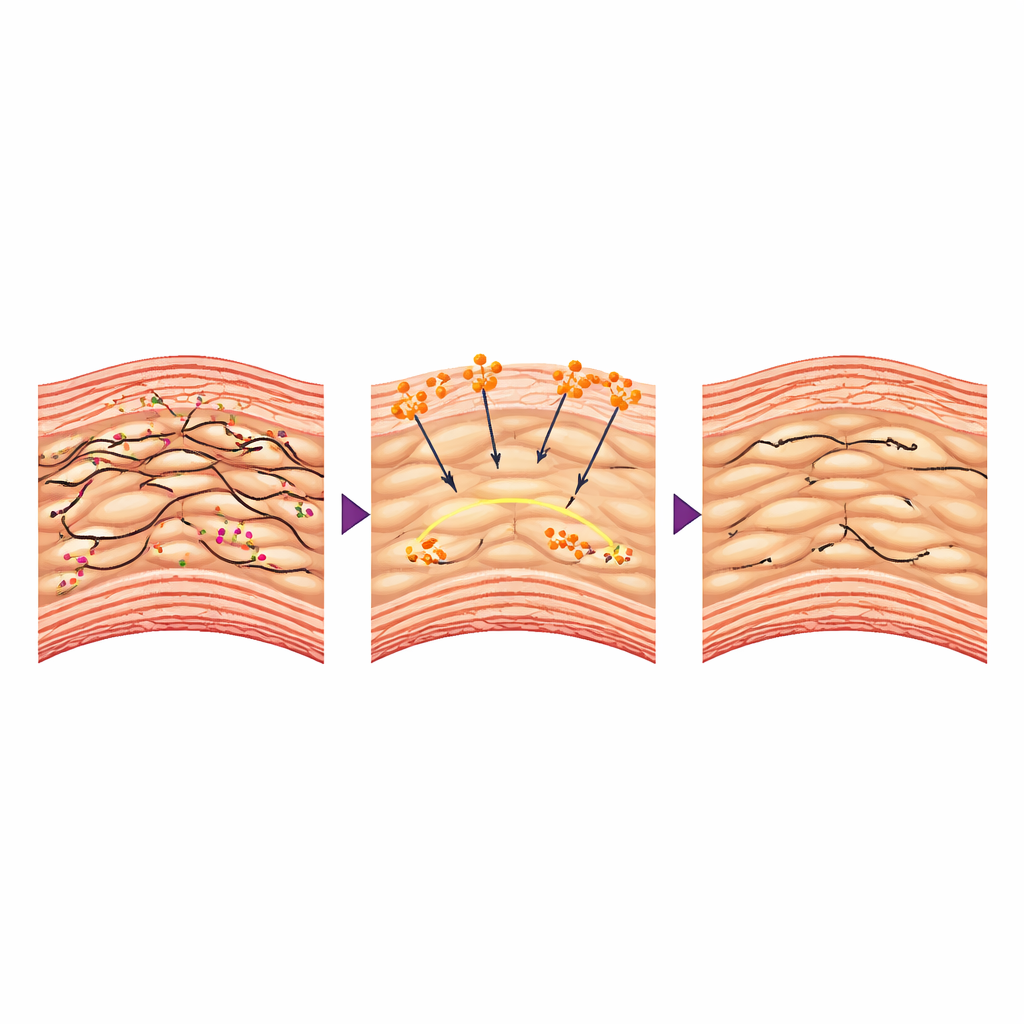
Le dialogue caché entre la protéine sanguine et les cellules musculaires
Comment une protéine de coagulation pourrait‑elle protéger l’aorte de l’intérieur ? Les auteurs se sont concentrés sur les cellules musculaires lisses vasculaires, les cellules contractiles qui forment la couche moyenne de l’aorte et jouent le rôle d’« anneaux de renfort » vivants. Dans la maladie, ces cellules perdent souvent leur état contractile serré et basculent vers une forme plus lâche et synthétique qui dégrade les tissus environnants. L’étude a montré que lorsque le fibrinogène pénétrait dans la paroi aortique, il interagissait avec des récepteurs spécifiques sur ces cellules et aidait à préserver leur échafaudage interne d’actine. Les cellules musculaires lisses d’animaux traités étaient plus rigides, se contractaient plus fortement lors d’essais et exprimaient davantage de marqueurs « contractiles » et moins de protéines qui dégradent la matrice de soutien. Au niveau génétique, le fibrinogène a atténué l’activité de Bmal1, un régulateur majeur lié à l’horloge biologique, qui dans ce contexte favorisait des changements nuisibles du comportement des cellules musculaires lisses. Forcer la réexpression de Bmal1 annulait les bénéfices du fibrinogène, montrant que cette voie de signalisation était centrale dans l’effet protecteur.
Du mécanisme au traitement potentiel
Parce que le fibrinogène favorise aussi la coagulation, l’équipe a cherché à savoir si son bénéfice était simplement dû à la formation de caillots plus solides. En utilisant un anticoagulant puissant pour bloquer la thrombine — l’enzyme qui transforme le fibrinogène en caillot solide — ils ont montré que le fibrinogène protégeait toujours l’aorte même lorsque la formation de caillot était largement inhibée. Enfin, ils ont testé différentes doses et observé que seules des quantités suffisamment élevées de fibrinogène administré ralentissaient la maladie, réduisaient les ruptures et préservaient la structure tissulaire. Ensemble, ces résultats présentent le fibrinogène comme une molécule à double fonction : à des niveaux plus élevés, le fibrinogène intact peut pénétrer une paroi aortique affaiblie, calmer une voie de signalisation nocive dans les cellules musculaires lisses et les aider à rester fortes et contractiles. Pour les patients, cela ouvre la possibilité que des perfusions de fibrinogène, soigneusement dosées, puissent un jour devenir un traitement de type pharmacologique pour ralentir la dissection aortique et prolonger en toute sécurité la fenêtre permettant une chirurgie programmée salvatrice.
Citation: Zhong, X., Li, D., Zhao, Y. et al. Fibrinogen–Bmal1 signaling as a therapeutic target to limit aortic dissection by preserving VSMC contractility. Sig Transduct Target Ther 11, 103 (2026). https://doi.org/10.1038/s41392-026-02610-x
Mots-clés: dissection aortique, fibrinogène, cellules musculaires lisses vasculaires, signalisation Bmal1, anévrisme aortique