Clear Sky Science · fr
Le circArhgap26 modifié par m6A atténue les lésions cardiaques d’ischémie‒reperfusion en supprimant la palmitoylation de la plakophiline‑1
Pourquoi il est important de protéger le cœur après un infarctus
Lorsqu’une personne fait un infarctus, les médecins s’efforcent de rouvrir l’artère obstruée et de rétablir le flux sanguin. Cette intervention sauve des vies, mais elle comporte aussi un revers : le retour brutal du sang peut endommager davantage le cœur, un problème appelé lésion d’ischémie–reperfusion. L’étude résumée ici explore un défenseur naturel inattendu à l’intérieur des cellules cardiaques — une molécule d’ARN circulaire nommée circArhgap26 — qui aide à protéger le muscle cardiaque contre cette seconde vague de dégâts. Comprendre comment fonctionne cette petite molécule pourrait orienter vers de nouveaux traitements et des tests sanguins pour les personnes atteintes de maladies cardiaques.
Un cercle caché dans le script génétique du cœur
La plupart d’entre nous imaginent les gènes sous forme de brins droits d’ADN et d’ARN, mais les cellules produisent aussi des molécules d’ARN en forme d’anneau, appelées ARN circulaires, qui sont particulièrement stables et peuvent affiner de nombreux processus cellulaires. Les chercheurs ont recherché dans le cœur de souris les ARN circulaires qui varient lors d’une lésion cardiaque et se sont concentrés sur l’un d’eux, circArhgap26, dont les niveaux chutaient fortement lorsque le flux sanguin était interrompu puis rétabli. Ils ont confirmé que cet ARN circulaire forme une boucle fermée, qu’il se trouve principalement dans le compartiment liquide de la cellule et qu’il ne sert pas de matrice pour fabriquer une protéine. Il semble plutôt jouer un rôle régulateur, interagissant avec d’autres molécules pour influencer si une cellule cardiaque survit ou meurt après un épisode de stress. 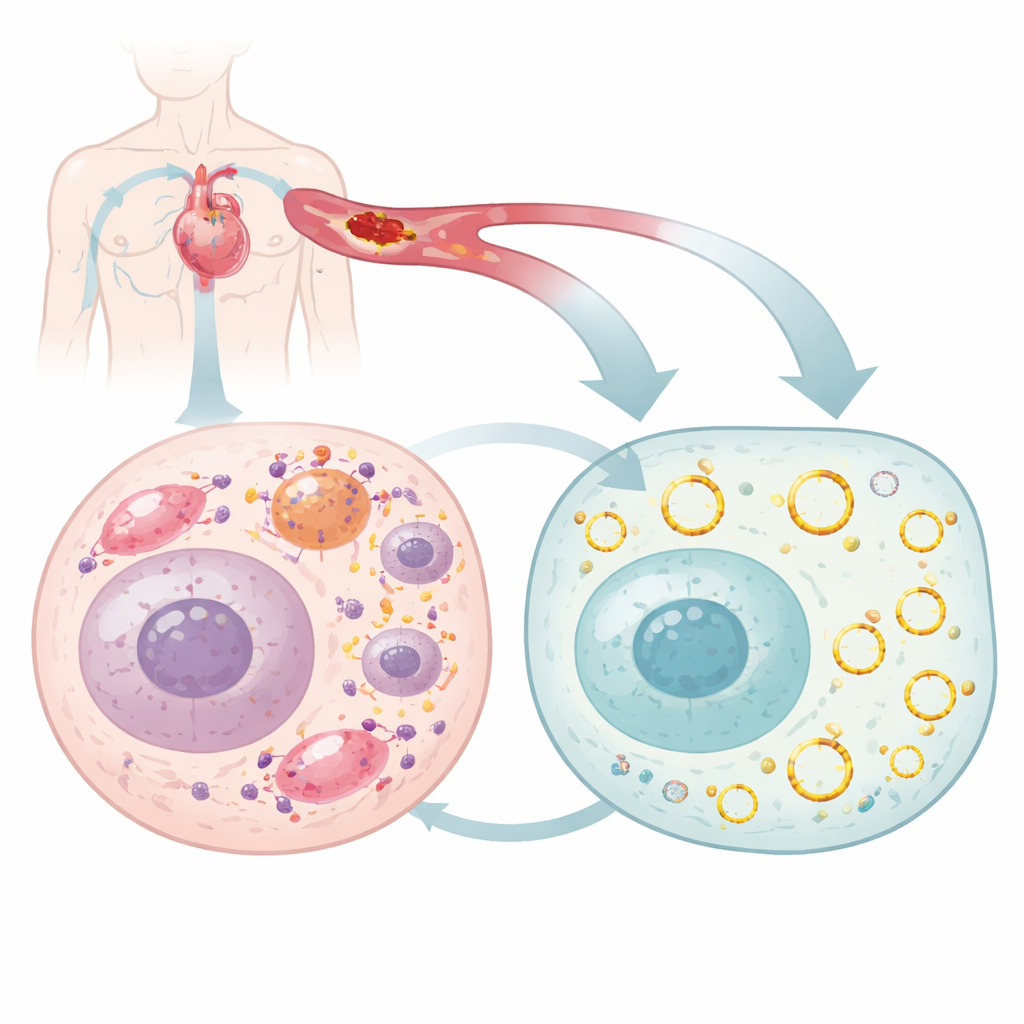
La preuve que l’ARN circulaire protège le cœur
Pour déterminer ce que fait réellement circArhgap26, l’équipe a augmenté ou diminué ses niveaux dans des cœurs de souris. Lorsqu’ils ont utilisé un virus pour relever circArhgap26 spécifiquement dans les cellules musculaires cardiaques, les animaux soumis à une occlusion temporaire d’une artère coronaire suivie d’un rétablissement du flux sanguin présentaient une contraction cardiaque plus forte, des zones lésées plus petites et moins de cellules en train de mourir. Les marqueurs classiques de lésion dans le sang et le tissu cardiaque étaient aussi plus bas. L’effet inverse a été observé lorsque l’ARN circulaire a été silencé : même sans infarctus induit, la fonction cardiaque s’est détériorée et la mort cellulaire a augmenté, et ces problèmes se sont aggravés en présence d’ischémie–reperfusion. Des effets protecteurs similaires sont apparus dans des cellules cardiaques de type humain en culture, suggérant que le mécanisme est conservé entre la souris et l’homme.
Un partenaire protéique nocif maintenu sous contrôle
En approfondissant, les chercheurs ont cherché comment circArhgap26 exerce cette protection. À l’aide de techniques biochimiques de pêche, ils ont découvert qu’il se lie directement à une protéine structurale appelée plakophiline‑1 (PKP1), qui peut influencer l’adhésion cellulaire et la propension des cellules à subir la mort programmée. Dans les cœurs lésés et les cellules cardiaques stressées, les niveaux de PKP1 augmentaient et étaient associés à des dégâts plus importants. La suppression de PKP1 a atténué les lésions cardiaques et la mort cellulaire, tandis que sa surexpression a aggravé les résultats. Lorsque circArhgap26 était accru, la quantité de protéine PKP1 diminuait bien que l’activité du gène ne changeât pas, ce qui indique un point de contrôle après la synthèse du message ARN. Des expériences ont montré que circArhgap26 accélère la dégradation de la protéine PKP1 en interférant avec un processus de modification lipidique appelé palmitoylation, qui stabilise normalement PKP1.
Une lutte moléculaire autour des signaux de mort cellulaire
La palmitoylation est réalisée par une famille d’enzymes ; l’une d’elles en particulier, ZDHHC1, a été identifiée comme ajoutant des groupes gras à PKP1 et le rendant plus durable. CircArhgap26 se lie à PKP1 sur la même région utilisée par ZDHHC1, créant une lutte moléculaire. Quand l’ARN circulaire l’emporte, PKP1 reçoit moins d’étiquettes lipidiques, devient moins stable et est éliminé plus rapidement. Cela a un effet en cascade : PKP1 favorise normalement la synthèse d’une autre protéine, APAF1, en interagissant avec un segment régulateur de son ARN. APAF1 est une pièce clé de la machinerie qui active les enzymes caspase‑9 et caspase‑3, exécutrices centrales de la mort cellulaire. Avec PKP1 moins stable, la production protéique d’APAF1 diminue, la cascade de signalisation de la mort est atténuée et les cellules cardiaques ont plus de chances de survivre au stress du rétablissement du flux sanguin. 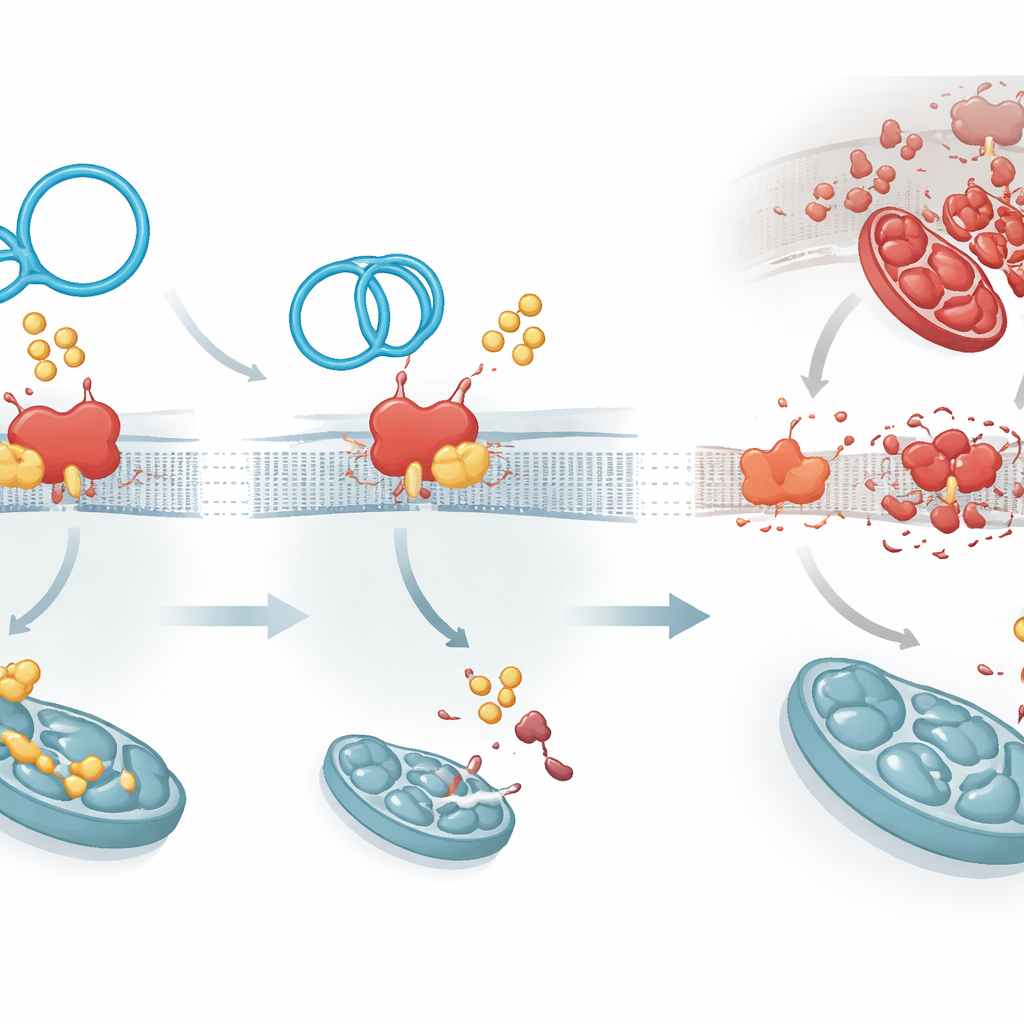
Affiner le cercle et son potentiel pour les patients
L’étude révèle aussi comment circArhgap26 lui‑même est réduit pendant la lésion. Une marque chimique courante sur l’ARN, appelée m6A, s’accumule sur cet ARN circulaire dans les cœurs stressés. Une protéine lectrice nommée YTHDF2 reconnaît cette marque et favorise la dégradation de circArhgap26, affaiblissant la défense naturelle du cœur au moment où elle est le plus nécessaire. Fait important, la version humaine de cet ARN circulaire est très proche de celle de la souris et se trouve à des niveaux sensiblement plus faibles dans le sang de patients soumis à des procédures de réouverture des artères comparés à des volontaires sains. Ensemble, ces résultats suggèrent que restaurer ou imiter circArhgap26 pourrait à la fois servir de marqueur sanguin de risque et proposer une nouvelle thérapie. En termes simples, ce travail met au jour une petite molécule circulaire qui agit comme un gardien contre les lésions de reperfusion en désamorçant une chaîne mortelle d’événements à l’intérieur des cellules cardiaques.
Citation: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Mots-clés: lésion d’ischémie‑reperfusion, ARN circulaire, infarctus, apoptose des cardiomyocytes, thérapie à base d’ARN