Clear Sky Science · fr
La synergie chimio‑photothermique déclenche l’immunité antitumorale via la ferroptose
Transformer la chaleur et la lumière du corps en arme contre le cancer
Les médicaments de chimiothérapie peuvent réduire les tumeurs, mais ils s’accompagnent souvent d’effets secondaires sévères et n’empêchent pas toujours la récidive. Cette étude explore une nouvelle façon de rendre un médicament existant, le docétaxel, plus efficace et plus intelligent en l’encapsulant dans de minuscules particules thermosensibles et en les activant par lumière proche infrarouge. L’objectif n’est pas seulement de tuer les cellules tumorales avec plus de précision, mais aussi d’éveiller le système immunitaire pour qu’il reconnaisse et traque le cancer dans tout l’organisme et prévienne les rechutes futures. 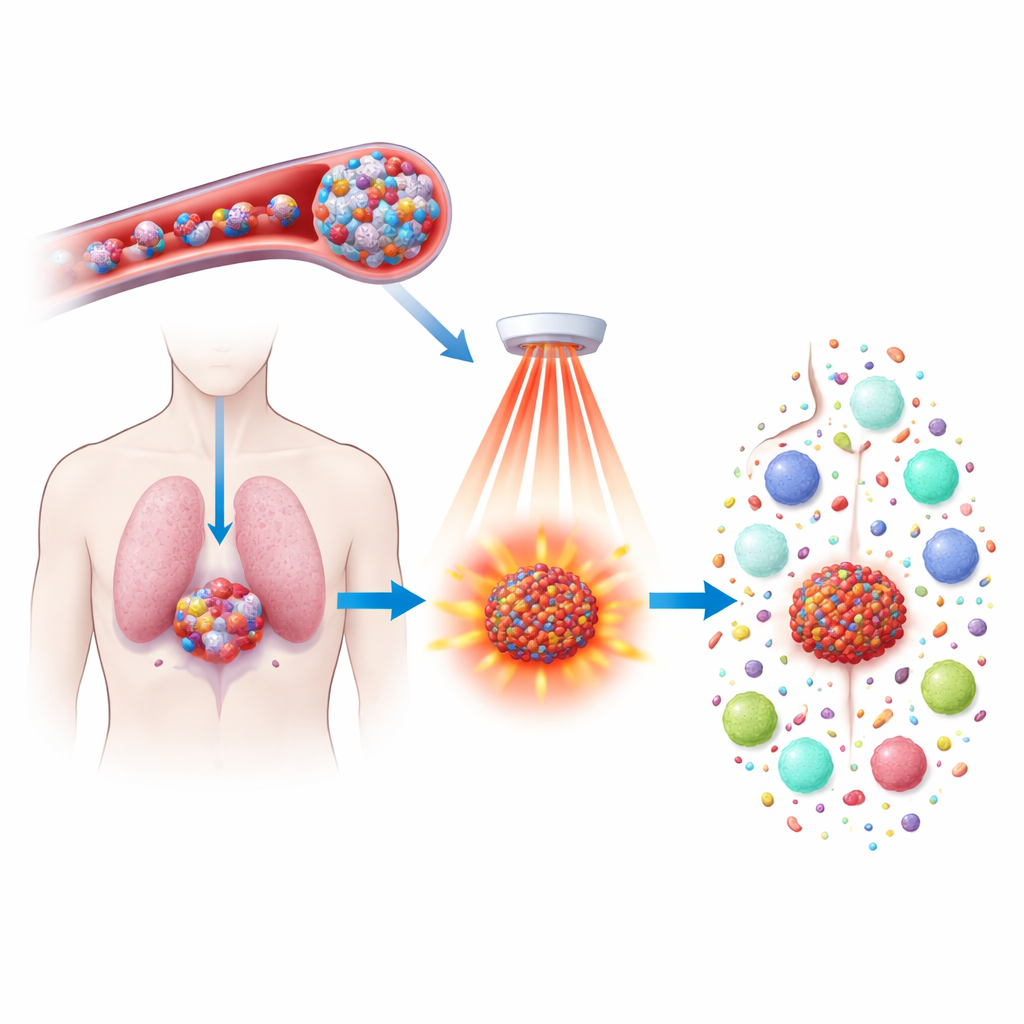
De minuscules coursiers qui savent où aller
Les chercheurs ont conçu un nouveau type de nanoparticule à partir d’un polymère contenant du ferrocène, une molécule porteuse de fer qui réagit fortement avec le peroxyde d’hydrogène — un oxydant présent en plus grande quantité dans les tumeurs que dans les tissus sains. Ces polymères s’autoassemblent en sphères hydrophiles capables de transporter à la fois du docétaxel et un colorant absorbant la lumière appelé IR808. Une fois injectées dans la circulation sanguine, les particules sont suffisamment petites et stables pour circuler et s’accumuler dans les tumeurs, où la porosité des vaisseaux sanguins et les concentrations élevées de peroxyde d’hydrogène commencent à fragiliser les particules et à libérer lentement leur cargaison. Cette conception concentre le traitement au niveau des tumeurs tout en limitant les dommages aux organes sains.
Utiliser la lumière pour suralimenter les lésions locales
On dirige ensuite sur la zone tumorale de la lumière proche infrarouge, qui pénètre les tissus en toute sécurité. L’IR808 à l’intérieur des nanoparticules absorbe cette lumière et la convertit en chaleur tout en générant des espèces réactives de l’oxygène. La combinaison du peroxyde d’hydrogène produit par la tumeur et des oxydants induits par la lumière provoque une désintégration plus rapide des particules et la libération de leur charge médicamenteuse exactement là où elle est nécessaire. Parallèlement, le fer contenu dans le segment ferrocène aide à transformer ces oxydants en formes particulièrement agressives qui attaquent les composants lipidiques des membranes cellulaires. Cette attaque chimique et thermique ciblée augmente nettement le pouvoir destructeur par rapport au seul docétaxel ou au traitement par lumière. 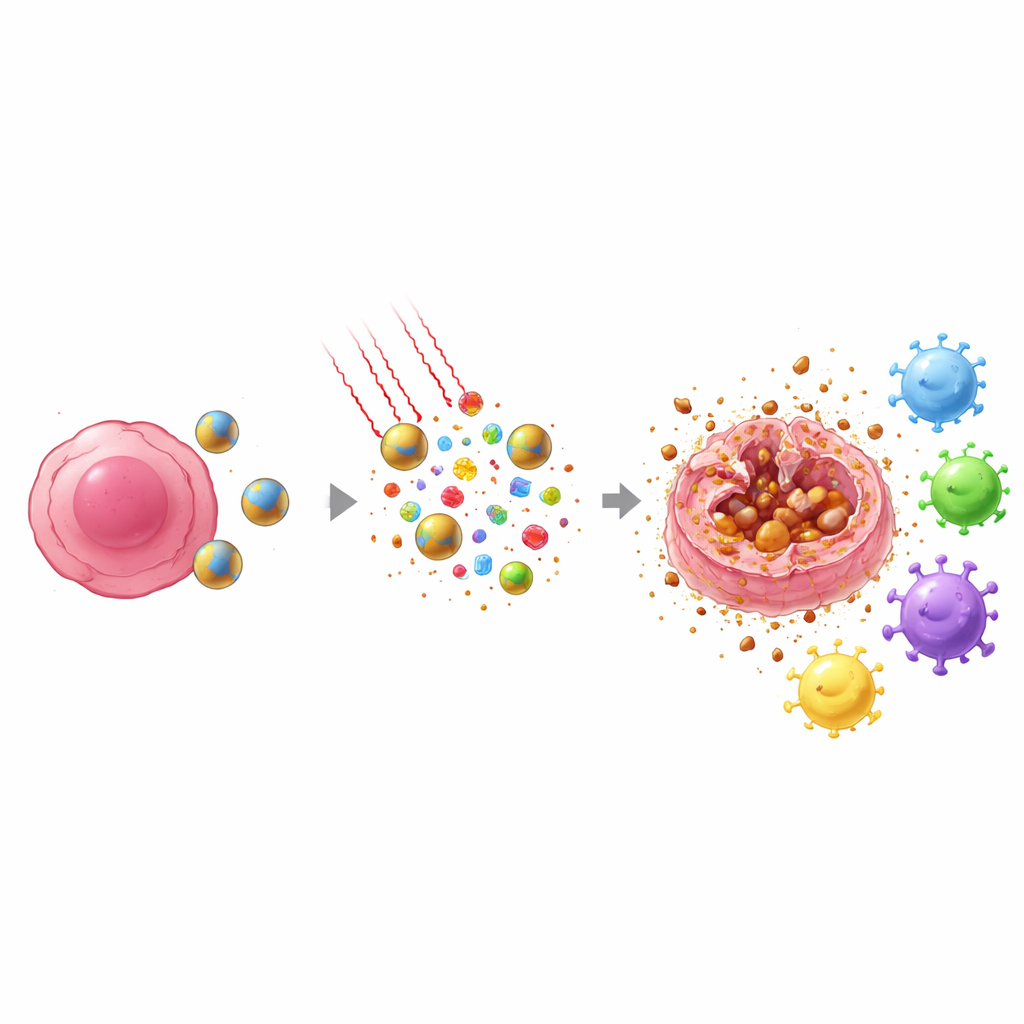
Un "brûlage contrôlé" qui signale au système immunitaire
Il est important de noter que le mode de mort des cellules tumorales sous ce traitement diffère de la chimiothérapie classique. Au lieu de se décomposer discrètement en fragments, de nombreuses cellules subissent un processus appelé ferroptose, une forme de mort lipidique, dépendante du fer, au cours de laquelle la membrane externe se rompt. Quand cela se produit, les cellules libèrent des signaux d’alarme internes et des fragments tumoraux spécifiques dans leur environnement. Parallèlement, le docétaxel provoque la translocation d’une protéine nucléaire clé, HMGB1, vers le bord cellulaire, la préparant à être libérée. Chaleur, oxydants et action du médicament créent ensemble une décharge de signaux de danger et d’antigènes que des sentinelles immunitaires voisines — les cellules dendritiques — peuvent détecter et transporter jusqu’aux ganglions lymphatiques.
De l’attaque locale à la défense systémique
Dans des modèles murins de tumeur, ce traitement chimiothérapeutique combiné à la photothermie a non seulement réduit les tumeurs directement chauffées plus efficacement que chaque composant pris isolément, mais il a aussi modifié le paysage immunitaire. Les tumeurs présentaient davantage de cellules dendritiques matures et un plus grand nombre de lymphocytes T cytotoxiques, tant dans la tumeur elle‑même que dans les ganglions drainants. Chez certains souris immunocompétentes, les tumeurs primaires ont disparu après seulement deux cycles de traitement. Lorsque les scientifiques ont implanté plus tard de nouvelles tumeurs à distance ou dans le flanc opposé, ces poussées secondaires ont été ralenties ou supprimées, indiquant que les animaux avaient développé une forme de mémoire immunitaire spécifique au cancer. L’ajout d’un anticorps bloquant les points de contrôle empêchant l’épuisement des lymphocytes T a en outre réduit les métastases pulmonaires et prolongé la survie, suggérant que ce traitement local peut être associé aux immunothérapies modernes.
Pourquoi cela compte pour les soins futurs contre le cancer
Pour un non‑spécialiste, l’essentiel est que cette approche transforme le docétaxel d’un poison systémique brut en un élément d’une stratégie anticancéreuse intelligente et en plusieurs étapes. En encapsulant le médicament dans des nanoparticules activées par la lumière et contenant du fer, réactives à la chimie propre de la tumeur, la thérapie inflige davantage de dégâts à l’intérieur des tumeurs tout en épargnant les tissus sains. Le profil particulier de mort cellulaire qu’elle induit agit comme un vaccin provenant de la tumeur elle‑même, apprenant au système immunitaire à reconnaître et à mémoriser le cancer. Si ces résultats se traduisent chez l’humain, de tels systèmes chimio‑photothermiques pourraient aider à convertir des tumeurs résistantes « froides » en tumeurs « chaudes » répondant beaucoup mieux aux traitements basés sur l’immunité, réduisant potentiellement les récidives et améliorant le contrôle à long terme.
Citation: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Mots-clés: nanomédecine contre le cancer, thérapie photothermique, ferroptose, immunothérapie anticancéreuse, libération de docétaxel