Clear Sky Science · fr
Pro-drogues nanozymes à coordination conductrice déclenchant précisément la pyroptose, la cuproptose et la ferroptose pour une vaccination anticancéreuse in situ
Transformer les tumeurs en leurs propres vaccins
Le traitement du cancer vise généralement à tuer directement les cellules tumorales, mais que se passerait-il si une tumeur pouvait être transformée en un vaccin contre elle-même ? Cette étude décrit une « pro-drogue » nanoparticulaire intelligente qui circule sans danger dans l’organisme, ne s’active qu’au sein des tumeurs, puis oblige les cellules cancéreuses à mourir d’une manière qui alerte puissamment le système immunitaire. Le résultat n’est pas seulement la réduction des tumeurs primaires, mais aussi l’apprentissage pour l’organisme de traquer les tumeurs distantes et les métastases.
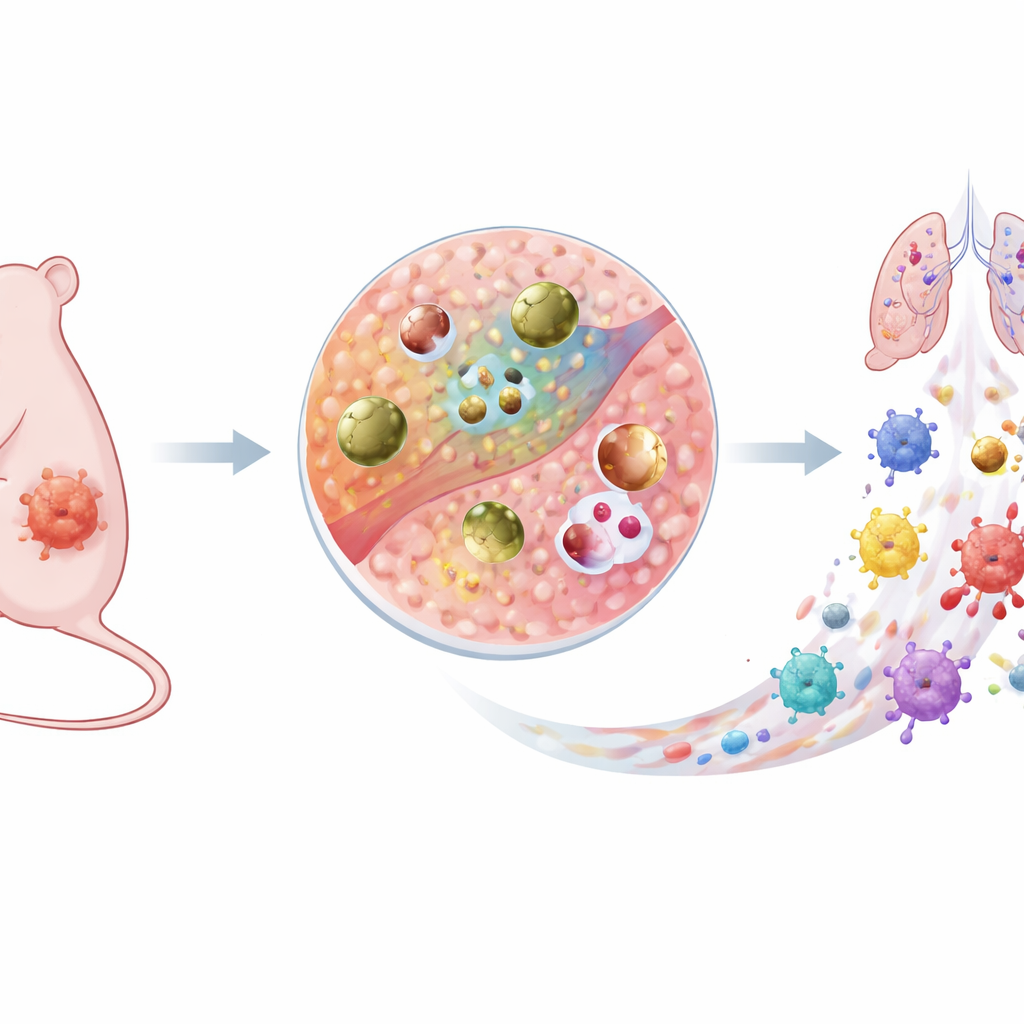
Une nouvelle arme intelligente contre le cancer
Les chercheurs ont conçu une particule minuscule à base de cuivre appelée Cu–DHN qui se comporte comme un médicament en sommeil pendant la circulation et comme un combattant agressif contre le cancer une fois qu’elle atteint une tumeur. Elle est assemblée à partir d’ions cuivre, d’une molécule précurseur inoffensive (1,5-di hydroxynaphtalène, ou DHN) et de l’acide aminé cystéine. Ensemble, ils forment un réseau de coordination conducteur, ce qui signifie que les électrons peuvent se déplacer facilement à travers la particule. Cette « autoroute » interne pour les électrons permet à l’ensemble de la nanoparticule, et pas seulement à sa surface, de participer aux réactions chimiques. De manière cruciale, Cu–DHN est conçue pour ne répondre qu’à la chimie particulière du microenvironnement tumoral, où le glutathion antioxydant et le peroxyde d’hydrogène sont tous deux anormalement élevés.
Comment la chimie tumorale active l’interrupteur
À l’intérieur des tumeurs, Cu–DHN agit comme une enzyme artificielle. En présence simultanée de glutathion et de peroxyde d’hydrogène, elle utilise d’abord le glutathion pour réinitialiser ses ions cuivre dans un état hautement réactif, puis exploite le peroxyde d’hydrogène pour générer un flux continu d’oxydants très agressifs (radicaux hydroxyles). Ces oxydants remplissent deux fonctions : ils endommagent les composants cellulaires et convertissent le DHN inoffensif enfermé dans la particule en juglone, un composé anticancéreux puissant. La juglone, à son tour, supprime les défenses antioxydantes de la tumeur et augmente encore les niveaux de peroxyde d’hydrogène, créant une boucle d’amplification auto-entretenue de stress oxydatif qui reste confinée à la tumeur, car seules les tumeurs fournissent les entrées chimiques adéquates pour lancer le cycle.
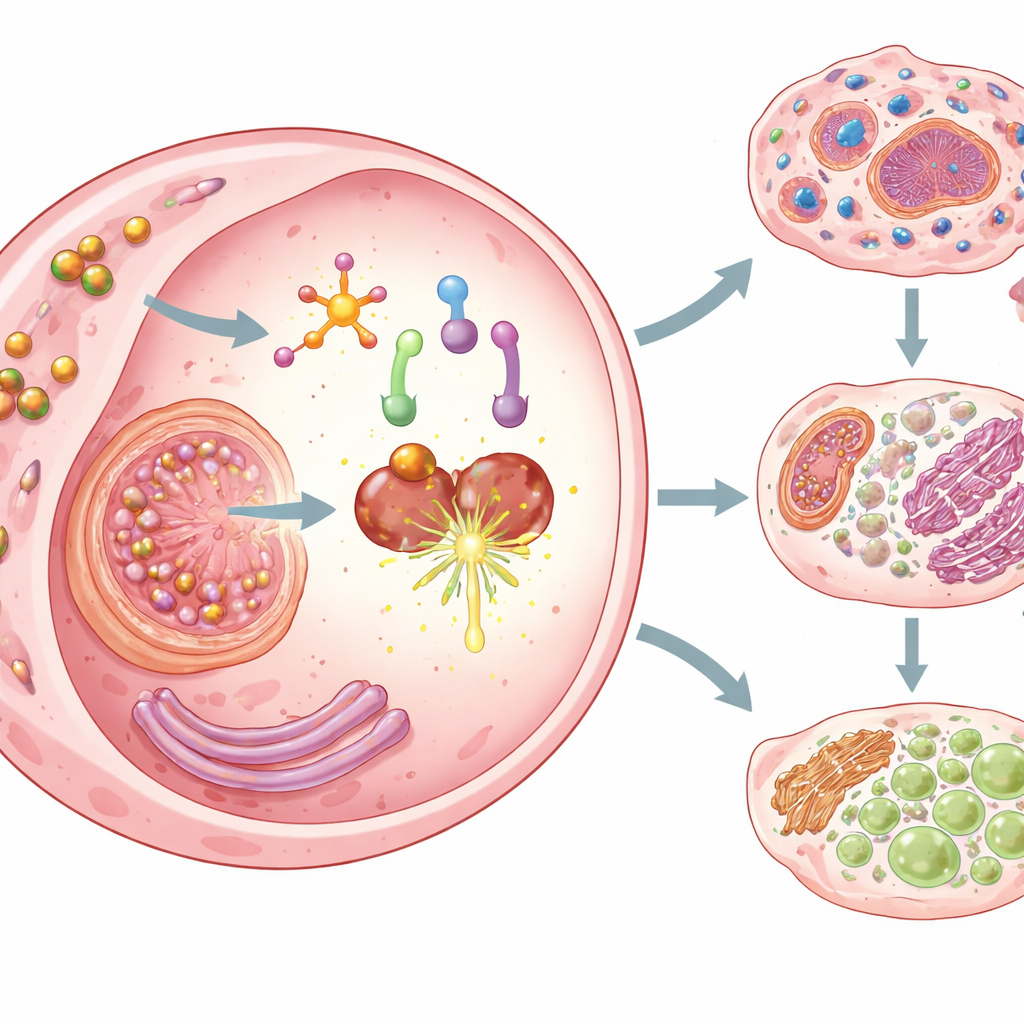
Déclencher trois formes de mort cellulaire cancéreuse
Une fois activée, Cu–DHN fait plus que simplement empoisonner les cellules cancéreuses. Elle déclenche trois formes régulées de mort cellulaire particulièrement visibles par le système immunitaire. D’abord, la juglone inverse le silence épigénétique d’une protéine formant des pores appelée gasdermine D et active un complexe capteur inflammatoire, de sorte que les cellules subissent la pyroptose — une forme de mort spectaculaire, bulleuse, qui fait éclater la membrane et déverse le contenu intracellulaire. Ensuite, le cuivre apporté par les nanoparticules, absorbé efficacement par les cellules cancéreuses, induit la cuproptose, une forme de mort liée à l’accumulation toxique de cuivre dans des éléments clés du métabolisme. Troisièmement, en épuisant le glutathion et en désactivant une enzyme protectrice (GPX4), Cu–DHN favorise la ferroptose, une mort due à la peroxydation des lipides. Ensemble, ces modes assurent que les cellules cancéreuses ne sont pas seulement tuées efficacement, mais meurent d’une manière particulièrement immunogène.
De l’attaque locale à la défense systémique
La pyroptose et les dommages oxydatifs qui l’accompagnent amènent les cellules tumorales à libérer une cascade de signaux d’alarme : antigènes associés à la tumeur, molécules de danger telles que l’ATP et HMGB1, et marqueurs de stress à leur surface. Dans des modèles murins de cancer du sein agressif, une seule injection de Cu–DHN dans la tumeur primaire a entraîné une forte activation des cellules dendritiques dans les ganglions lymphatiques voisins et une vague de lymphocytes CD8 cytotoxiques dirigés contre la tumeur. Ces cellules immunitaires ont ensuite migré vers des tumeurs non traitées du côté opposé du corps et vers les poumons, où elles ont ralenti ou presque empêché la croissance de nouvelles tumeurs et de nodules métastatiques. Le blocage des cellules CD8 a largement supprimé cette protection, confirmant que Cu–DHN transforme la tumeur primaire en un vaccin in situ qui apprend au système immunitaire à reconnaître et détruire le cancer ailleurs.
Effets puissants avec un profil de sécurité amélioré
Une préoccupation importante des thérapies basées sur la pyroptose est le risque d’endommager les tissus sains, qui possèdent eux aussi les mêmes protéines formant des pores. Lorsque la juglone est administrée directement sous sa forme active, les souris souffrent de toxicités importantes au niveau du foie, des reins et du sang. En revanche, Cu–DHN reste inerte dans les tissus sains, car ceux-ci ne présentent pas la combinaison de déclencheurs chimiques nécessaire pour activer la particule. Chez la souris, Cu–DHN a égalé la puissance cytotoxique et anti-métastatique de la juglone active tout en évitant les lésions d’organes, les anomalies sanguines et la perte de poids. En termes simples, ce travail montre comment une nanoparticule conductrice électriquement intelligente peut rester silencieuse dans l’organisme, ne s’éveiller qu’à l’intérieur des tumeurs, forcer les cellules cancéreuses à mourir d’une manière immunostimulante, et agir ainsi comme une plateforme de vaccin anticancéreux précise et autonome.
Citation: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
Mots-clés: immunothérapie du cancer, nanomédecine, pyroptose, vaccins contre le cancer, microenvironnement tumoral