Clear Sky Science · fr
Le profil spatiotemporel révèle des dynamiques distinctes et des régulations des points de contrôle des cellules CAR-T et CAR-NKT contre les tumeurs solides
Pourquoi cette recherche compte pour les soins du cancer de demain
Beaucoup de gens ont entendu parler des cellules CAR-T, un traitement de pointe dans lequel les propres cellules immunitaires d’un patient sont modifiées pour traquer le cancer. Ces thérapies fonctionnent remarquablement bien dans les cancers du sang mais ont du mal à lutter contre les tumeurs solides comme les cancers de l’ovaire, du poumon ou du pancréas. Cette étude pose une question simple mais cruciale : existe-t-il un type de cellule immunitaire meilleur pour cette tâche ? En comparant les cellules CAR-T classiques à un autre type modifié appelé CAR-NKT, les chercheurs cartographient le comportement de chacune dans l’organisme au fil du temps et proposent des pistes pour rendre les thérapies cellulaires de nouvelle génération, prêtes à l’emploi, plus sûres et plus efficaces contre les tumeurs solides.
Deux types de cellules antitumorales conçues sur mesure
L’équipe a créé deux thérapies reconnaissant le même marqueur tumoral, la mésothéline, fréquemment exprimée sur les tumeurs de l’ovaire et d’autres tumeurs solides. Les cellules CAR-T conventionnelles ont été générées à partir de lymphocytes T sanguins adultes, similaires à ceux utilisés dans les produits cliniques actuels. Les cellules CAR-NKT, en revanche, ont été dérivées de cellules souches de sang de cordon transformées en un sous-type immunitaire spécialisé appelé cellules NKT invariantes, puis équipées à la fois d’un récepteur ciblant la tumeur et d’un réservoir intégré du facteur de croissance IL-15. Alors que les CAR-T attaquent principalement via leur récepteur artificiel, les CAR-NKT peuvent tuer de plusieurs façons simultanément : via le CAR, via leur récepteur T naturel, et via de puissants récepteurs de type « natural killer ». En culture, les CAR-NKT ont détruit un large éventail de lignées de cancer ovarien, y compris celles exprimant peu ou pas de mésothéline, alors que les CAR-T étaient en grande partie limitées aux tumeurs présentant fortement la cible.
Contrôle tumoral plus fort avec moins d’effets systémiques
Testées chez des souris porteuses de tumeurs ovariennes humaines, la différence est devenue encore plus nette. Les deux thérapies ont été injectées dans la cavité abdominale, où les tumeurs se développaient. Les CAR-T ont initialement ralenti la croissance tumorale mais se sont finalement disséminées dans tout l’organisme et ont connu une expansion explosive, provoquant une maladie de type greffon contre l’hôte et la mort chez tous les animaux traités. Les CAR-NKT, en revanche, se sont dirigées efficacement vers les tumeurs, se sont développées de manière contrôlée, ont éliminé le cancer, puis ont progressivement régressé tout en restant détectables pendant plus de 100 jours. Elles sont restées pour la plupart confinées à la région tumorale au lieu d’envahir les organes sains, et les souris n’ont pas développé les toxicités sévères observées avec les CAR-T. Les auteurs ont aussi montré que l’ajout d’IL-15 aux CAR-T augmentait leur puissance mais aggravait considérablement leurs effets secondaires, alors que des CAR-NKT ingénieurs avec IL-15 gagnaient en persistance sans déclencher d’inflammation dangereuse.
Comment la localisation, le métabolisme et la mémoire distinguent les CAR-NKT
Pour comprendre pourquoi ces deux thérapies se comportent si différemment, les chercheurs ont profilé des centaines de milliers de cellules individuelles prélevées dans les tumeurs, le sang, la rate et le foie sur plusieurs semaines. Les CAR-NKT présentaient un profil de récepteurs chimiokines favorisant le « rester sur place », c’est‑à‑dire la rétention dans les tissus inflammés et les tumeurs, plutôt que la recirculation par les ganglions lymphatiques. Au sein des tumeurs, elles s’établissaient dans des états effecteurs et apparentés à la mémoire durables avec des signes d’épuisement relativement faibles, et maintenaient des voies énergétiques robustes telles que la phosphorylation oxydative et un métabolisme des acides aminés stable. Les CAR-T, en revanche, montraient des basculements plus erratiques entre états de prolifération, d’attaque et d’épuisement, surtout dans les tumeurs et la rate, et leurs programmes métaboliques étaient moins stables. Globalement, les CAR-NKT progressaient plus lentement vers l’épuisement terminal et conservaient davantage de souplesse pour continuer à combattre.
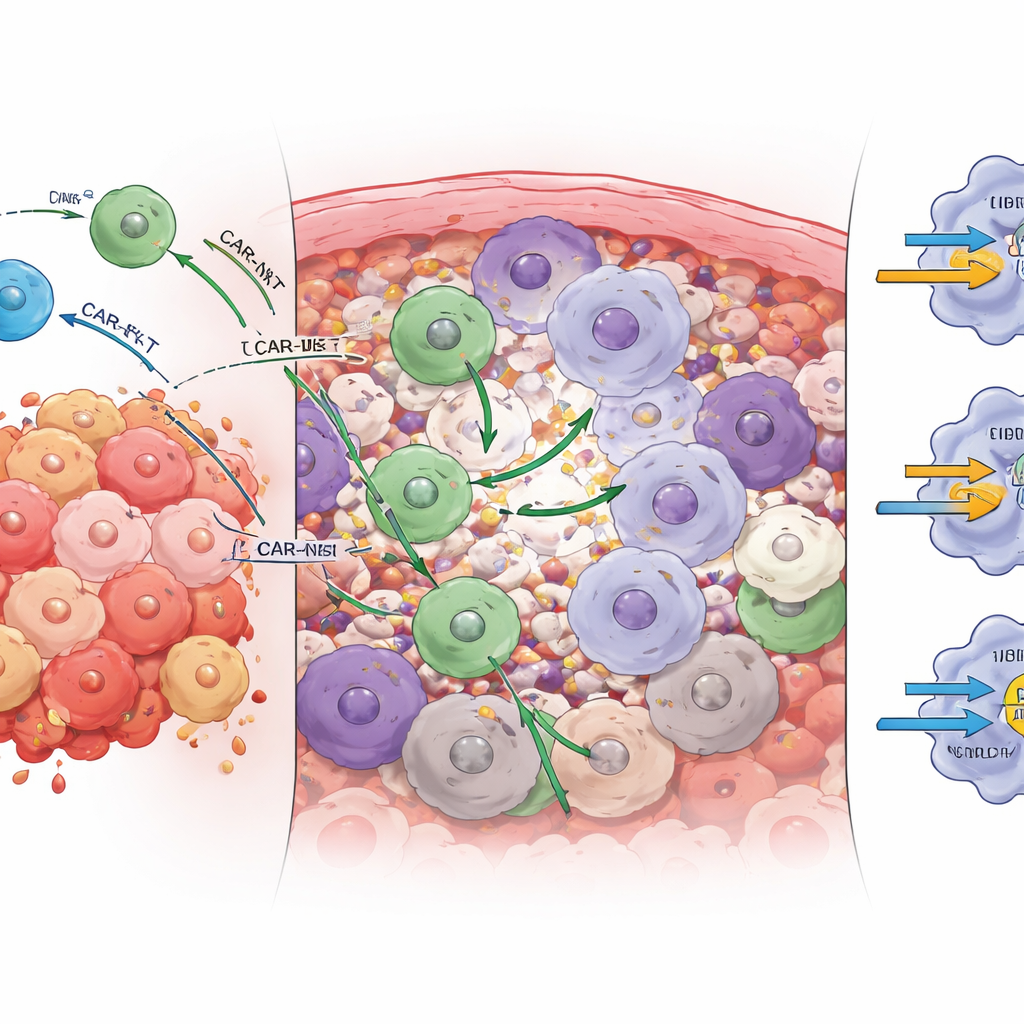
Des « freins » différents contrôlent chaque thérapie cellulaire
Le microenvironnement tumoral utilise des soi‑disant points de contrôle immunitaires — des freins moléculaires sur les cellules immunitaires — pour atténuer les attaques. En analysant la communication entre cellules modifiées et cellules tumorales via des paires récepteur‑ligand, l’étude a montré que les freins dominants ne sont pas les mêmes pour les CAR-T et les CAR-NKT. Pour les CAR-T, une interaction inhibitrice clé impliquait le récepteur TIGIT sur les cellules immunitaires se liant à son partenaire sur les cellules tumorales. Chez la souris, le blocage de TIGIT a significativement amélioré le contrôle tumoral et la survie avec les CAR-T. Les CAR-NKT, en revanche, étaient le plus fortement freinées par un récepteur apparenté appelé CD96. Le blocage de CD96 — et non de TIGIT — a augmenté le nombre de CAR-NKT, leur activation et l’élimination tumorale. Le blocage traditionnel PD‑1/PD‑L1, qui a déçu dans de nombreux essais sur tumeurs solides, a eu peu d’effet dans ce modèle, en cohérence avec de faibles niveaux de PD‑L1 sur les tumeurs ovariennes étudiées.
Ce que cela signifie pour les thérapies anticancéreuses de nouvelle génération
Pour un lecteur non spécialiste, le message principal est que toutes les cellules immunitaires modifiées ne se valent pas. Les CAR-NKT, surtout lorsqu’elles sont produites à partir de cellules souches comme produits standardisés prêts à l’emploi, ont montré une capacité de destruction tumorale plus large, un meilleur adressage des tumeurs, une mémoire à long terme renforcée et moins d’effets secondaires dangereux que les CAR-T classiques dans ces modèles de tumeurs solides. Autre point important, l’étude révèle que chaque type cellulaire est régi par ses propres points de contrôle dominants — TIGIT pour les CAR-T et CD96 pour les CAR-NKT — ce qui plaide pour des combinaisons de médicaments plus ciblées plutôt que des solutions universelles. Ensemble, ces résultats soutiennent l’idée que les CAR-NKT pourraient constituer l’épine dorsale de thérapies cellulaires plus sûres et plus polyvalentes contre les cancers solides difficiles à traiter.
Citation: Li, YR., Li, M., Chen, Y. et al. Spatiotemporal profiling reveals distinct dynamics and checkpoint regulations of CAR-T and CAR-NKT cells against solid tumors. Sig Transduct Target Ther 11, 92 (2026). https://doi.org/10.1038/s41392-026-02602-x
Mots-clés: Thérapie par cellules CAR-NKT, Cellules CAR-T, Tumeurs solides, Points de contrôle immunitaires, Immunothérapie cellulaire