Clear Sky Science · fr
Nanoréacteurs enzymatiques en cascade confinée inspirés de la nature pour une thérapie ciblée de l’athérosclérose
Combattre les obstructions artérielles avec de petites aides intelligentes
L’athérosclérose — artères obstruées et enflammées — est une cause majeure d’infarctus et d’accidents vasculaires cérébraux. Beaucoup de personnes prennent déjà des médicaments hypocholestérolémiants, mais des plaques dangereuses peuvent encore se former et rester inflammatoires. Cette étude décrit un « nanoréacteur » inspiré de la nature, une particule minuscule conçue pour imiter les défenses antioxydantes de notre organisme afin d’apaiser les plaques enflammées, d’éliminer les molécules nocives et de ralentir le vieillissement artériel chez des modèles animaux. 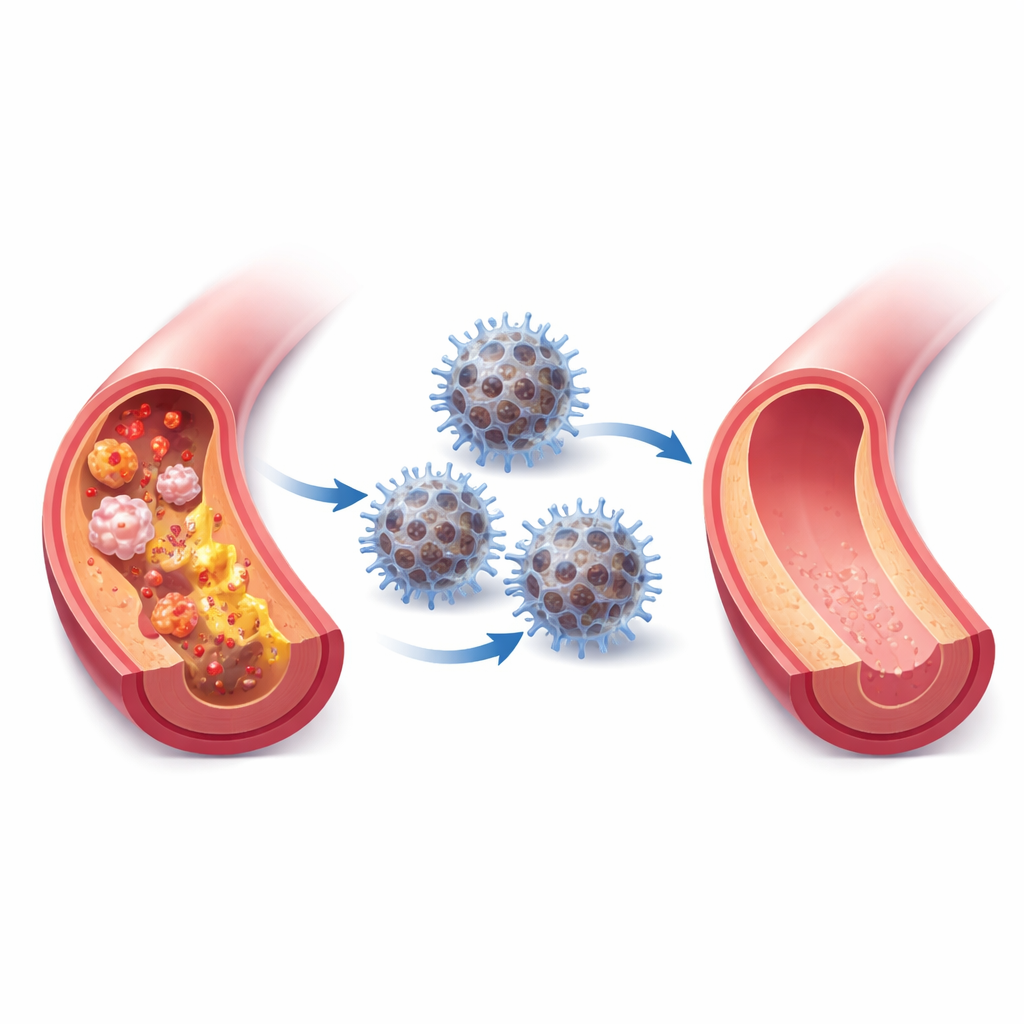
Pourquoi les plaques sont plus que de la simple graisse
Les médecins pensaient autrefois que les plaques artérielles relevaient surtout d’un dépôt de cholestérol. On sait maintenant qu’elles sont aussi entraînées par le stress oxydatif et l’inflammation chronique. Dans les artères malades, des molécules instables appelées espèces réactives de l’oxygène endommagent les lipides, transformant le cholestérol normal en une forme plus nocive qui est engloutie par les cellules immunitaires, formant des « cellules spumeuses » et des plaques instables. Le vieillissement et le stress des cellules qui tapissent les vaisseaux alimentent encore l’inflammation en libérant davantage de signaux pro‑inflammatoires. Les enzymes naturelles dans les tissus sains contrôlent habituellement ces molécules réactives, mais dans les plaques cet équilibre est rompu, et l’apport de simples antioxydants isolés n’a pas donné de bons résultats chez les patients.
Emprunter les stratégies des usines enzymatiques naturelles
Dans les cellules vivantes, les enzymes protectrices qui neutralisent les espèces réactives de l’oxygène travaillent souvent côte à côte en équipes serrées, transmettant rapidement des intermédiaires nocifs les uns aux autres dans une cascade. Les chercheurs ont cherché à reproduire cette stratégie avec des matériaux artificiels. Ils ont conçu un nanoréacteur en « cascade confinée » en empaquetant des particules ultrafines de bleu de Prusse — qui se comportent comme plusieurs enzymes antioxydantes — à l’intérieur d’une sphère de silice dendritique et poreuse dopée au sélénium, un élément clé d’une autre enzyme antioxydante naturelle. Cette structure poreuse concentre à la fois les catalyseurs et leurs cibles, permettant une détoxification progressive des espèces réactives de l’oxygène de façon plus efficace que si chaque composant était dispersé dans le sang. 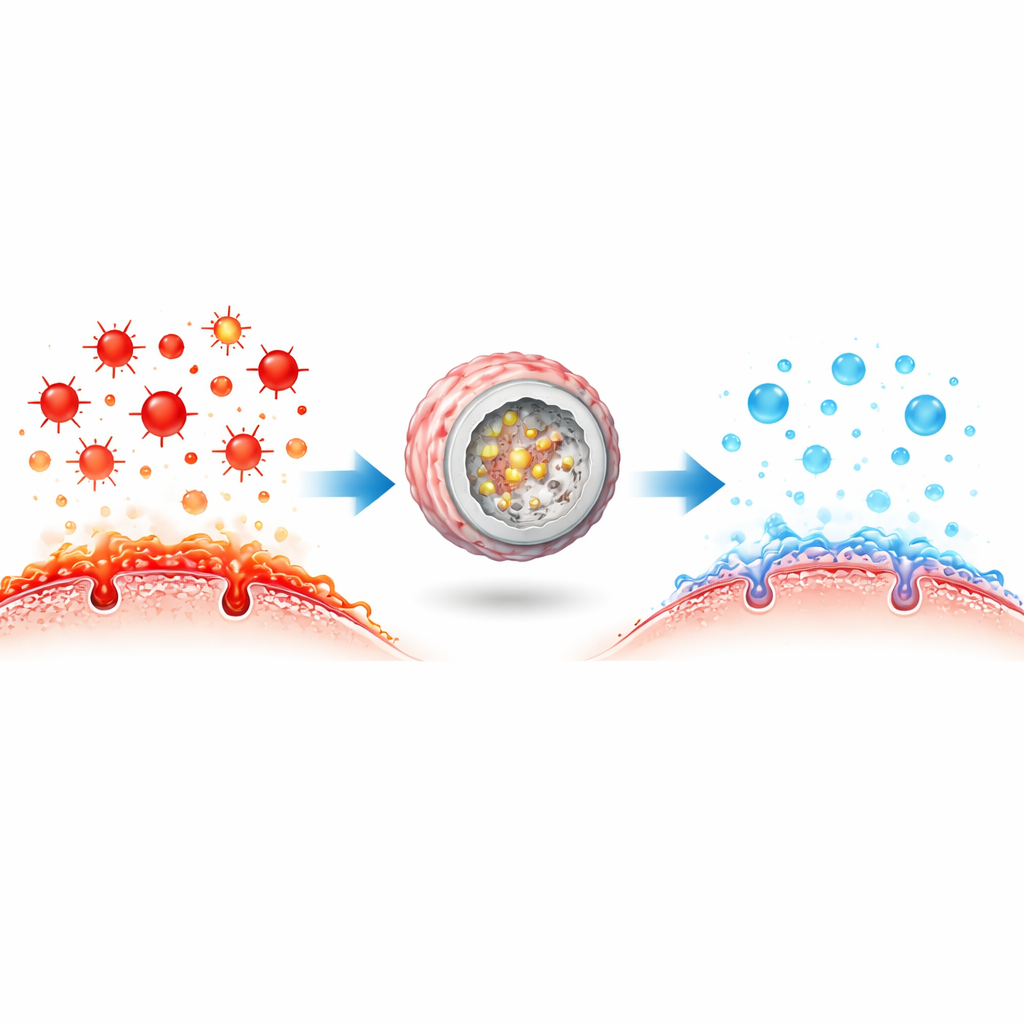
Donner aux nanoréacteurs un déguisement de neutrophile
Amener un médicament au bon endroit reste un défi majeur. Ici, l’équipe a enveloppé ses nanoréacteurs dans des membranes prélevées sur des neutrophiles, un type de globule blanc naturellement attiré par les foyers d’inflammation. Ce camouflage aide les particules à circuler plus longtemps, à échapper à une élimination rapide et à se diriger vers les plaques, où les cellules vasculaires malades et les cellules immunitaires exposent des marqueurs d’adhérence compatibles. Dans des expériences cellulaires, ces nanoréacteurs recouverts ont été internalisés plus facilement par les cellules endothéliales enflammées et par les macrophages que les témoins non recouverts, montrant que cette « coque » biologique les oriente activement vers les zones problématiques.
Apaiser l’inflammation, les cellules spumeuses et le vieillissement cellulaire
En culture, les nanoréacteurs ont pu imiter plusieurs enzymes à la fois, décomposant différents types d’espèces réactives de l’oxygène et générant des produits inoffensifs. Lorsqu’on les a ajoutés à des cellules immunitaires et des cellules endothéliales enflammées, ils ont fortement réduit le stress oxydatif, diminué la libération de médiateurs inflammatoires clés et poussé les macrophages d’un état promoteur de dommages vers un état réparateur. Ils ont aussi réduit l’accumulation de lipides à l’intérieur des macrophages, limitant la formation de cellules spumeuses, et protégé les cellules endothéliales des dommages à l’ADN et des marqueurs du vieillissement. Ces effets étaient plus marqués que ceux observés avec chacun des composants isolés, soulignant l’importance d’un design confiné et en plusieurs étapes.
Protéger les artères dans un modèle murin
L’équipe a ensuite testé les nanoréacteurs recouverts de membranes de neutrophiles chez des souris génétiquement prédisposées à l’athérosclérose et alimentées avec un régime riche en graisses. Les particules ont circulé dans le sang pendant de nombreuses heures, se sont accumulées dans les plaques et ont montré une accumulation limitée dans les organes sains. Après plusieurs semaines de traitement, les souris recevant le nanoréacteur complet présentaient des zones de plaque plus petites, moins de cellules inflammatoires, plus de collagène stabilisant et des taux plus faibles d’enzymes liées à la rupture de plaque comparé aux témoins ou aux animaux recevant des formulations plus simples. Les colorations tissulaires ont révélé une réduction du stress oxydatif et moins de cellules sénescentes dans la paroi vasculaire, le tout sans signes évidents de toxicité ni de perte de poids.
Ce que cela pourrait signifier pour les traitements cardiaques futurs
Pour un non‑spécialiste, ce travail suggère une nouvelle manière d’aborder la maladie artérielle : au lieu de se contenter d’abaisser le cholestérol ou de bloquer un seul déclencheur inflammatoire, on utilise de petites machines inspirées de la nature pour nettoyer discrètement les molécules nocives, refroidir l’inflammation et ralentir le vieillissement cellulaire directement au sein des plaques. Loin d’être prêtes pour un usage humain, ces nanoréacteurs en cascade confinée montrent toutefois que la combinaison de matériaux intelligents et d’un camouflage biologique pourrait offrir une approche puissante et plus ciblée pour stabiliser les artères obstruées et, un jour, réduire le risque d’infarctus et d’AVC.
Citation: Wu, Y., Xia, H., Ding, H. et al. Nature-inspired confined cascade enzyme nanoreactors for targeted atherosclerosis therapy. Sig Transduct Target Ther 11, 84 (2026). https://doi.org/10.1038/s41392-026-02598-4
Mots-clés: athérosclérose, nanomédecine, stress oxydatif, inflammation, nanozyme