Clear Sky Science · fr
Libérer le potentiel d’une nanobombe bimétallique activant la voie STING pour renforcer un engageur bispécifique des lymphocytes T contre la photo-immunothérapie du cancer colorectal
Retourner le système immunitaire contre le cancer du côlon
Les cancers du côlon et du rectum sont fréquents et souvent mortels, en partie parce que les tumeurs apprennent à se cacher du système immunitaire. Cette étude explore une nouvelle stratégie qui rassemble plusieurs mécanismes anti-cancer dans une minuscule « nanobombe » pour réveiller les défenses de l’organisme, aider les cellules immunitaires à repérer la tumeur et empêcher la rechute ou la dissémination du cancer.
Pourquoi les médicaments immunitaires actuels ont besoin d’un amélioration
Une classe prometteuse de médicaments contre le cancer, les engageurs bispécifiques des lymphocytes T, agit comme des entremetteurs biologiques : une extrémité saisit un lymphocyte T (un acteur clé de l’immunité) et l’autre se fixe à un marqueur d’une cellule tumorale, les forçant à se rapprocher pour permettre au lymphocyte de tuer. Bien qu’efficaces dans les hémopathies, ces médicaments peinent face aux tumeurs solides comme le cancer colorectal. Ils sont rapidement éliminés de l’organisme, peuvent cibler des tissus sains exprimant le même marqueur, et se heurtent souvent à des tumeurs « froides » qui manquent de cellules immunitaires nécessaires à l’efficacité du traitement. Médecins et chercheurs cherchent donc des moyens de délivrer ces agents de façon plus sûre et de transformer les tumeurs froides en tumeurs « chaudes » riches en cellules immunitaires activées.
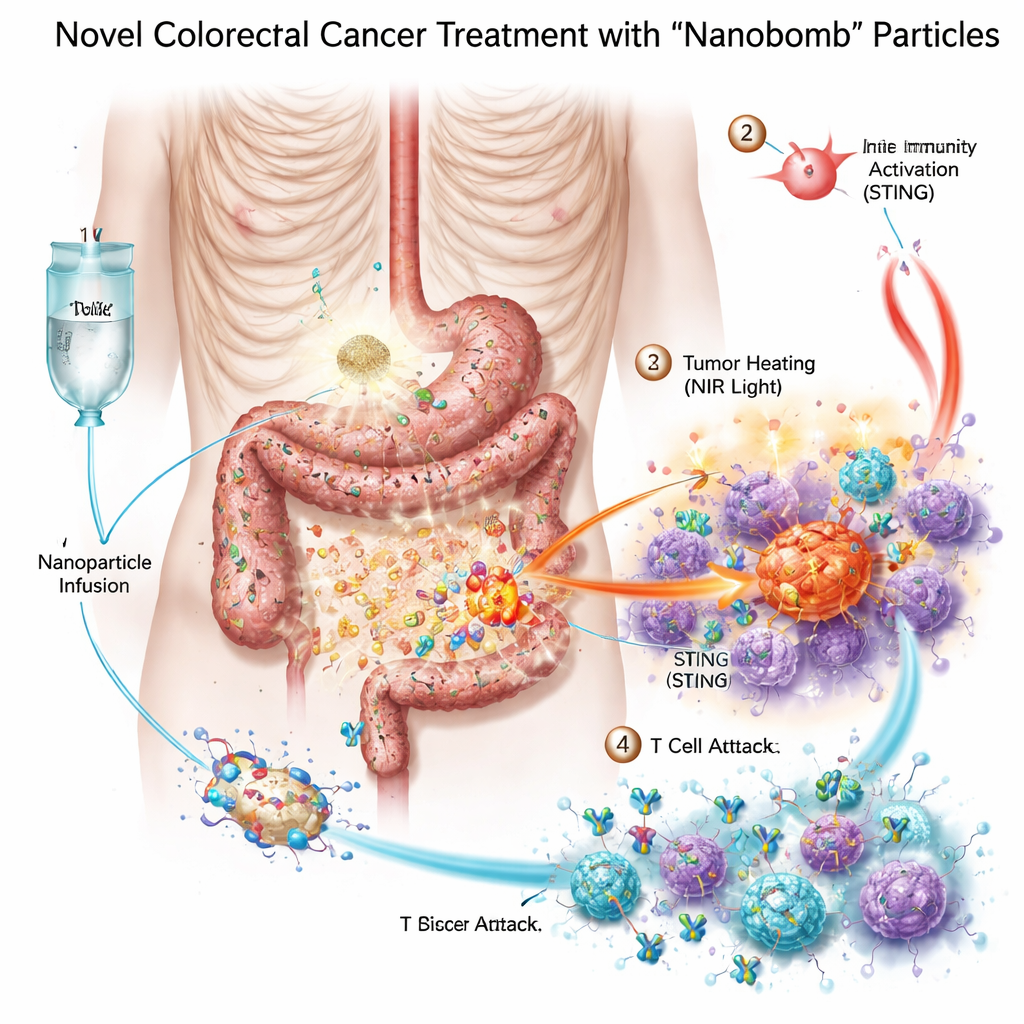
Trois armes réunies dans une minuscule « nanobombe »
Les chercheurs ont conçu une nanobombe bimétallique — nom scientifique MnO2/Co‑DA@BiTE/HPT — qui combine trois modes thérapeutiques dans une seule particule. D’abord, le cœur contient du manganèse et du cobalt, des métaux capables d’activer un système d’alarme cellulaire appelé voie STING, qui aide l’organisme à détecter le danger et à mobiliser les cellules immunitaires. Ensuite, la surface de la particule est revêtue d’un engageur bispécifique des lymphocytes T qui relie les lymphocytes T aux cellules cancéreuses. Troisièmement, le matériau absorbe la lumière proche infrarouge, permettant de chauffer la tumeur de l’extérieur via une photothérapie thermique. Pour que les nanobombes ciblent spécifiquement les cellules du cancer colorectal, l’équipe a ajouté un court fragment d’ADN, un aptamère, qui reconnaît PD‑L1, une molécule souvent abondante sur ces tumeurs. Une fois les particules arrivées dans la tumeur, des enzymes naturelles présentes dans le tissu tumoral contribuent à les décomposer et à libérer leur cargaison précisément là où elle est nécessaire.
Chauffer, alerter et recruter l’armée immunitaire
En éprouvette, les nanobombes ont tué les cellules de cancer colorectal plus efficacement que chaque composant pris isolément. Lorsqu’elles sont illuminées par une lumière proche infrarouge, les particules chauffent, stressent et endommagent les cellules tumorales, et contribuent à générer des espèces réactives de l’oxygène — des molécules très réactives qui blessent davantage les cellules tumorales. Ce stress a brisé l’ADN des cellules et a induit une forme de mort particulièrement visible qui émet des signaux de « danger ». Les cellules immunitaires voisines, notamment les cellules dendritiques, ont phagocyté le matériel tumoral mourant et activé la voie STING grâce au manganèse et au cobalt libérés. Elles ont alors produit des interférons et d’autres médiateurs inflammatoires qui favorisent la maturation et l’attraction des lymphocytes T. Parallèlement, l’engageur bispécifique à la surface de la nanobombe a physiquement rapproché les lymphocytes T des cellules tumorales PD‑L1‑positives, améliorant l’activation des lymphocytes T et la destruction tumorale même dans des tumeurs auparavant froides.
De la régression tumorale à une mémoire immunitaire durable
Dans plusieurs modèles murins — y compris des tumeurs colorectales sous-cutanées, des tumeurs bilatérales, des métastases pulmonaires et un modèle de récidive après chirurgie — les nanobombes associées à la lumière ont fortement ralenti ou presque arrêté la croissance tumorale. Les tumeurs traitées contenaient beaucoup plus de lymphocytes T CD8 tueurs et moins de lymphocytes T régulateurs qui suppriment normalement les réponses immunitaires. Les cellules dendritiques dans les tumeurs et les ganglions lymphatiques présentaient des signes de maturation, et les analyses sanguines montraient des niveaux accrus de cytokines stimulant l’immunité. Fait important, les souris qui avaient éradiqué leurs tumeurs après le traitement par nanobombe étaient mieux protégées lors d’une réintroduction du cancer et développaient moins de métastases pulmonaires, indiquant que la thérapie avait favorisé la formation d’une mémoire immunitaire à long terme plutôt qu’une simple réduction ponctuelle de la tumeur.
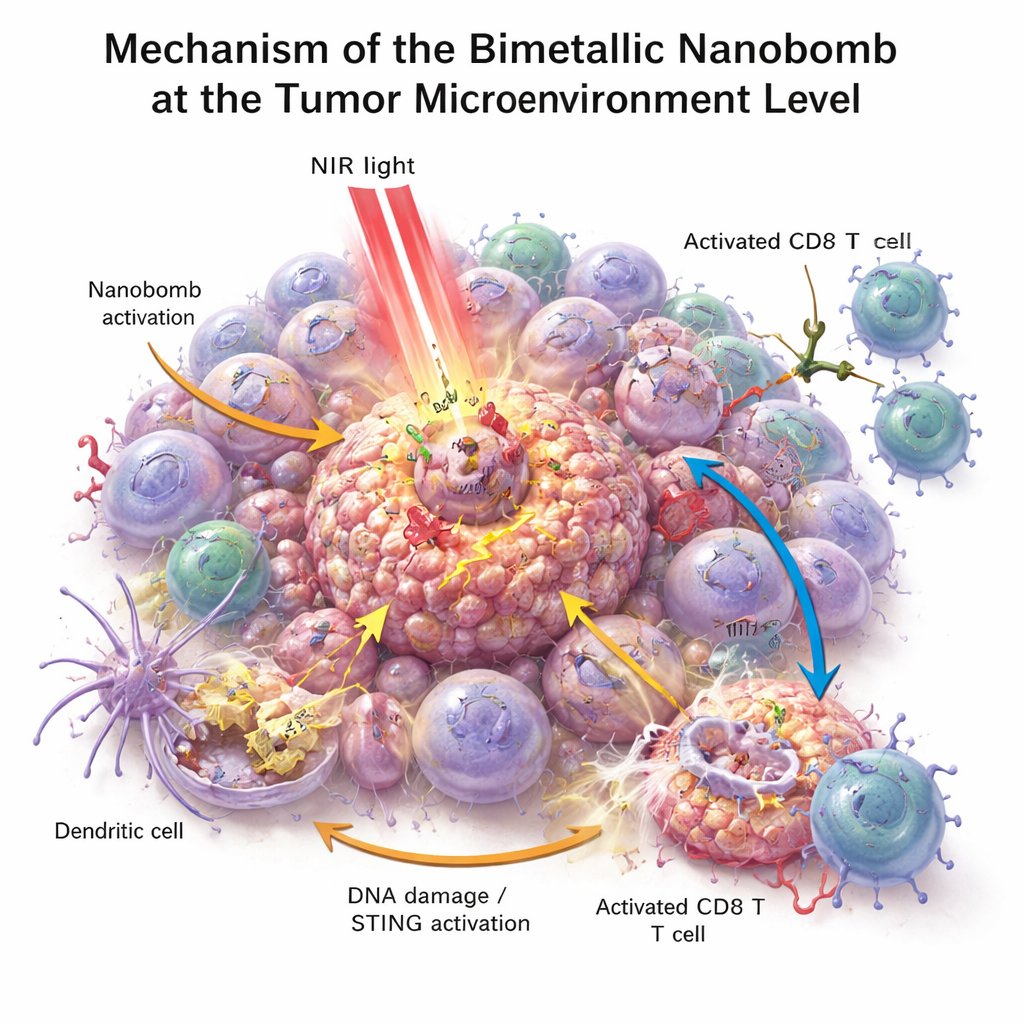
Ce que cela pourrait signifier pour les soins futurs du cancer
Ce travail présente une nanomédicine « triple action » qui chauffe les tumeurs, déclenche une alarme interne de danger et guide les lymphocytes T directement vers les cellules cancéreuses, le tout à l’intérieur d’une particule ciblée unique. Chez la souris, cette approche a non seulement transformé des tumeurs colorectales froides en tumeurs chaudes et enflammées, mais a aussi aidé à prévenir la récidive et la dissémination. Si la technologie est encore loin d’une utilisation clinique — la montée en échelle, la sécurité à long terme et les essais chez l’humain restant des défis majeurs — elle offre un modèle pour des traitements futurs qui allient matériaux intelligents et médicaments immunitaires afin d’offrir aux patients une réponse anti‑cancer plus robuste et plus durable.
Citation: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Mots-clés: cancer colorectal, immunothérapie, nanoparticules, voie STING, engageur bispécifique des lymphocytes T