Clear Sky Science · fr
Thérapie guidée pharmacocinétique–pharmacodynamique personnalisée via une plateforme multi-organoïde dérivée de cellules souches pluripotentes induites dans le cancer du sein mutant NF1
Pourquoi cette recherche compte pour les patients
De nombreuses personnes atteintes de cancer reçoivent des médicaments qui fonctionnent bien chez certains patients mais pas chez d’autres, et provoquent souvent des effets secondaires sévères. Cette étude décrit une nouvelle façon d’évaluer des traitements anticancéreux en dehors du corps en utilisant des mini-organes cultivés en laboratoire à partir des propres cellules d’un patient. Le travail se concentre sur une forme de cancer du sein difficile à traiter, causée par des altérations d’un gène appelé NF1, et montre comment la combinaison d’une stratégie de réparation génique et d’un médicament ciblé pourrait conduire à une thérapie plus sûre, plus efficace et véritablement personnalisée.
Construire une version miniature du corps du patient
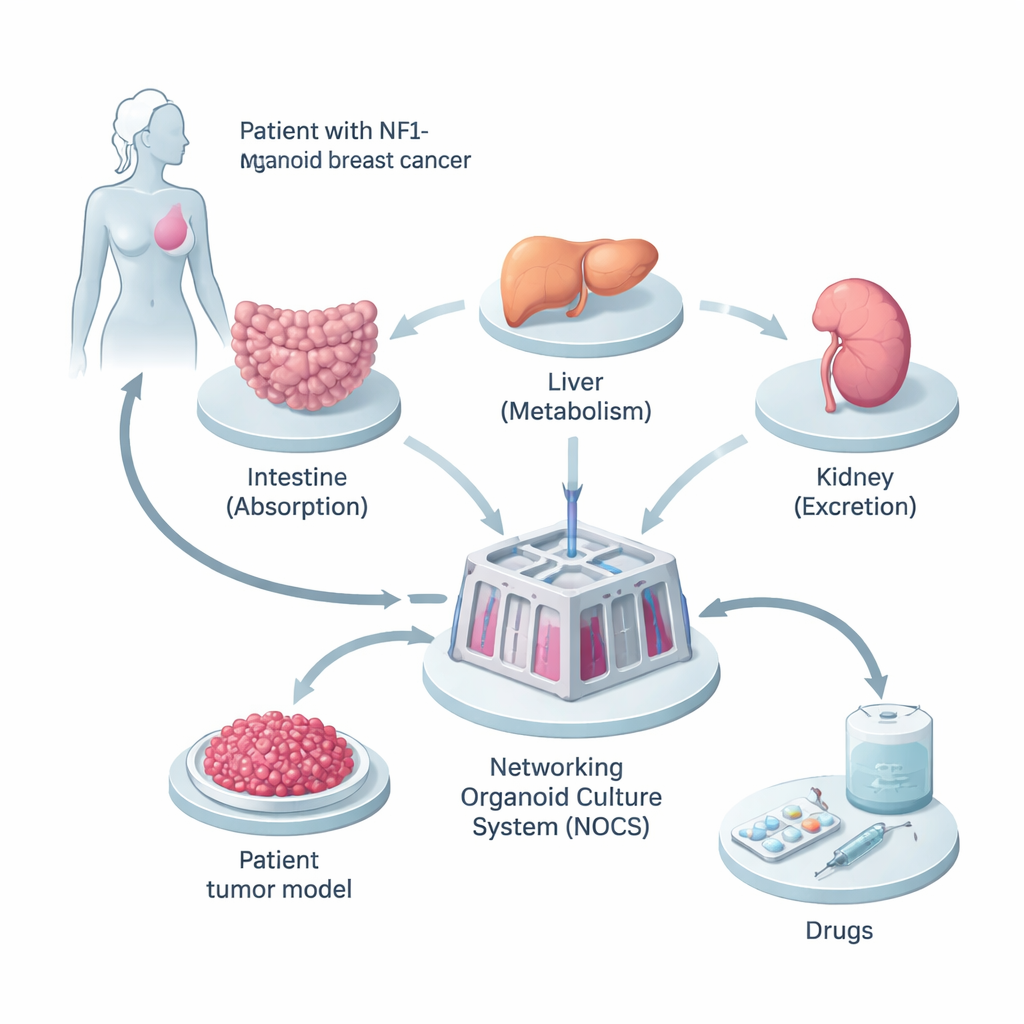
Les chercheurs ont commencé avec un prélèvement chez une femme dont le cancer du sein portait une mutation héréditaire du gène NF1. Ils ont reprogrammé ses cellules cutanées normales en cellules souches pluripotentes induites, capables de devenir presque n’importe quel type cellulaire du corps. À partir de celles-ci, ils ont cultivé trois types de mini-organes — intestin grêle, foie et rein — car ce sont les sites clés où les médicaments sont absorbés, transformés et éliminés. En parallèle, ils ont créé des « sphéroïdes » tumoraux 3D à partir de ses cellules cancéreuses, préservant la diversité cellulaire et les altérations génétiques trouvées dans la tumeur d’origine.
Un circuit vivant pour tester les médicaments
Pour que ces mini-organes se comportent davantage comme un véritable organisme, l’équipe les a reliés dans un dispositif rempli de fluide appelé Networking Organoid Culture System, ou NOCS. Dans ce montage, un milieu liquide circule entre les compartiments intestin, foie, rein et tumeur, imitant la circulation sanguine. Les médicaments peuvent être administrés de manière comparable à l’ingestion d’une pilule ou à une injection, et des capteurs et des pompes contrôlent la vitesse de circulation du « sang » et la fréquence de son renouvellement. Cela a permis aux scientifiques de suivre la quantité de médicament absorbée, la vitesse de sa dégradation et l’intensité de son action sur la tumeur — le tout dans un modèle humain spécifique au patient.
Corriger un gène déficient par exclusion d’exon
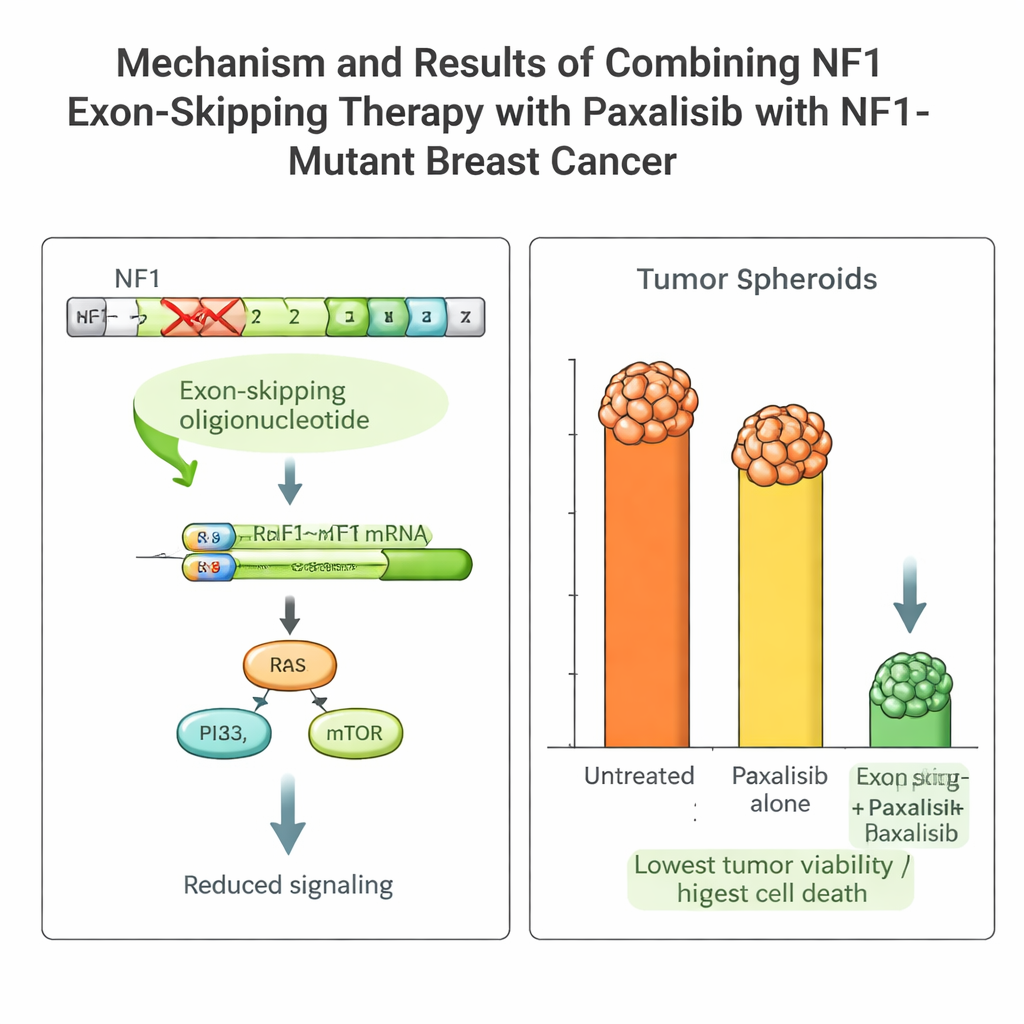
La tumeur de la patiente portait une mutation délétère de NF1 qui maintient activés des circuits de croissance et rend inefficaces de nombreux médicaments standards. L’équipe a conçu de courts fragments d’acide nucléique, appelés oligonucléotides antisens, pour amener la machinerie de traitement de l’ARN cellulaire à sauter la région défaillante (exon 2) du gène NF1. À l’aide d’un vecteur viral d’administration à action prolongée, ils ont induit un « saut d’exon » stable dans les cellules tumorales de la patiente. Cela a produit une protéine NF1 plus courte mais fonctionnelle, réduit les signaux de croissance hyperactifs et rendu les cellules tumorales plus sensibles au traitement.
Choisir le bon médicament ciblé avec une guidance PK/PD
Équipée de cette plateforme, l’équipe a comparé plusieurs médicaments de pointe bloquant la voie PI3K–mTOR, qui agit en aval de NF1. Ils ont mesuré la pharmacocinétique (la façon dont l’organisme traite le médicament) et la pharmacodynamique (l’effet du médicament sur la tumeur) à la fois chez la souris et dans le NOCS. Un médicament, le Paxalisib, s’est distingué : bien absorbé au niveau intestinal, il persistait dans le système à des concentrations utiles et présentait un comportement similaire chez l’animal et dans le dispositif d’organoïdes. Associé au saut d’exon NF1, le pouvoir cytotoxique du Paxalisib contre les cellules tumorales de la patiente a augmenté de façon spectaculaire, avec de fortes réductions de la croissance et des signes évidents de mort cellulaire programmée, tant dans le NOCS que chez des souris greffées avec la tumeur du patient.
Équilibrer bénéfices et risques entre les organes
Parce que les modèles d’intestin, de foie et de rein faisaient partie du même circuit, les chercheurs ont également pu observer des signes précoces de lésions d’organes. Le Paxalisib a provoqué des réponses au stress et un affaiblissement subtil des barrières dans les modèles intestinal et rénal ainsi que des signes de tension dans le foie, mais sans perte majeure de viabilité cellulaire à la dose testée. Ce type de vision globale, utilisant des tissus humains, offre une manière de comparer les options thérapeutiques non seulement sur leur capacité à réduire les tumeurs, mais aussi sur leur impact potentiel sur les organes sains avant qu’un médicament n’atteigne jamais un patient.
Ce que cela pourrait signifier pour la prise en charge future du cancer
En termes simples, cette étude montre qu’il est désormais possible de faire croître un « mini-corps sur puce » simplifié et spécifique au patient capable d’évaluer le comportement et les interactions de différents médicaments — et même d’approches de correction génique. Pour cette patiente atteinte d’un cancer du sein mutant NF1, la stratégie optimale était la combinaison d’une thérapie d’exclusion d’exon NF1 et du médicament oral Paxalisib, qui ensemble ont ralenti la croissance tumorale bien plus que chacun pris séparément. Si ces plateformes sont développées et testées chez davantage de patients, elles pourraient orienter les médecins vers des plans de traitement adaptés aux gènes et à la biologie de chaque personne, augmentant les chances de succès tout en réduisant la toxicité inutile.
Citation: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Mots-clés: oncologie personnalisée, cancer du sein, organoïdes, mutation NF1, thérapie ciblée