Clear Sky Science · fr
Exploiter les voies immunométaboliques pilotées par les lipides dans les métastases omentales pour améliorer l’immunothérapie chez les patientes atteintes de cancer de l’ovaire
Pourquoi la graisse abdominale compte pour le cancer de l’ovaire
Le cancer de l’ovaire se propage souvent vers un tablier graisseux de l’abdomen appelé l’omentum. Cette région est riche en adipocytes et en cellules immunitaires, et elle s’avère bien plus qu’un simple spectateur passif. L’étude résumée ici montre que la manière dont les cellules immunitaires utilisent et traitent les lipides dans ces dépôts omentaux peut aider à expliquer pourquoi seule une faible fraction de patientes bénéficie des immunothérapies modernes. Elle suggère aussi de nouvelles combinaisons médicamenteuses et des tests d’imagerie susceptibles d’élargir l’efficacité de ces traitements.
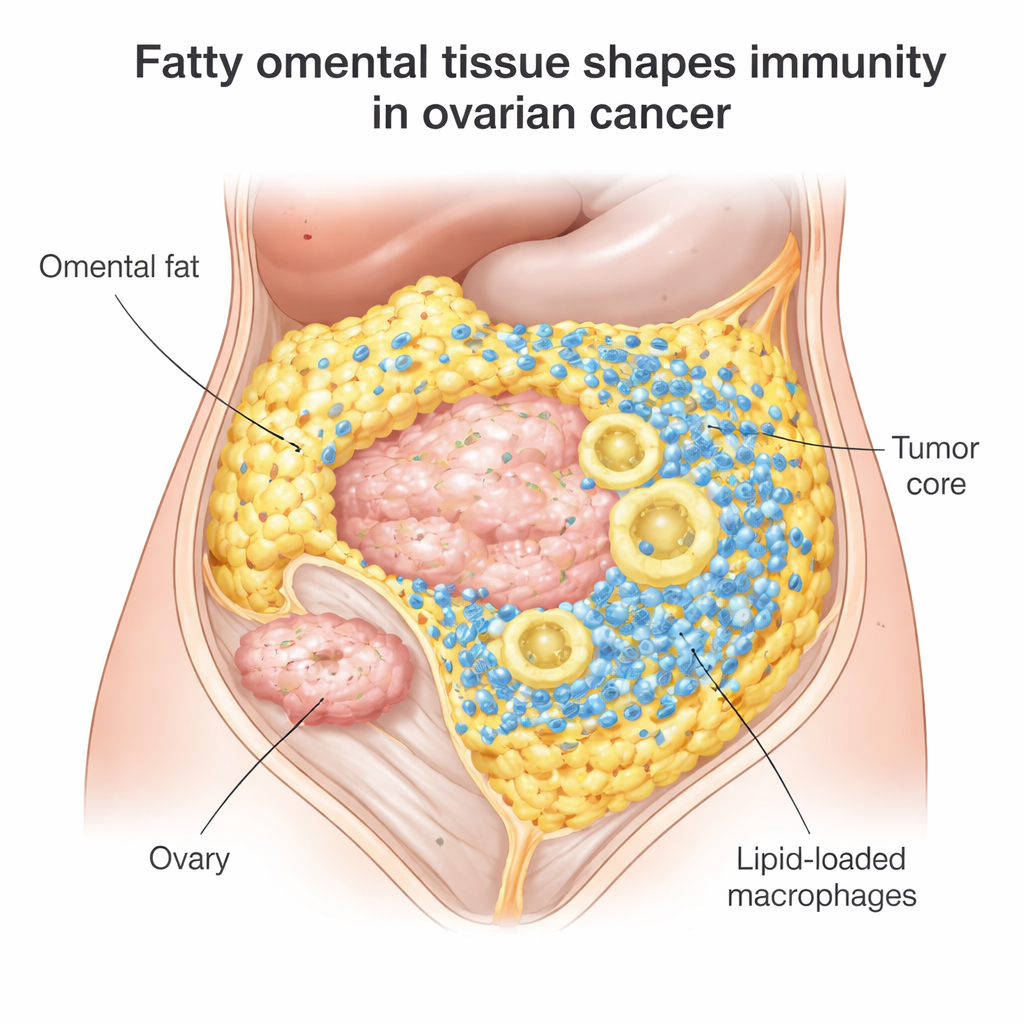
Un champ de bataille caché dans la graisse abdominale
La plupart des femmes atteintes d’un carcinome épithélial de l’ovaire répondent d’abord à la chirurgie et à la chimiothérapie, mais 70–80 % voient la maladie récidiver, et les inhibiteurs de points de contrôle tels que le nivolumab ou le pembrolizumab n’aident qu’environ 10–15 % des patientes. Les chercheurs se sont concentrés sur les métastases omentales, un site fréquent où le cancer de l’ovaire s’implante parmi les cellules graisseuses. En examinant plus de 100 échantillons tumoraux, ils ont constaté que les tumeurs omentales étaient abondamment peuplées de cellules immunitaires : des lymphocytes T cytotoxiques capables d’attaquer la tumeur et de grosses cellules épuratrices appelées macrophages. Mais il y avait un bémol. Ces lymphocytes T avaient tendance à se regrouper à la frontière entre la tumeur et la graisse, plutôt qu’à pénétrer dans le cœur tumoral où ils seraient le plus utiles.
Une graisse qui nourrit certains effecteurs immunitaires mais en submerge d’autres
En approfondissant, l’équipe a montré que les lymphocytes T dans ces tumeurs graisseuses s’adaptent à l’environnement local en captant des lipides, ou graisses, provenant des adipocytes voisins. Cela semble maintenir leur « forme » métabolique : leur activité génique et des tests en laboratoire indiquaient qu’ils étaient capables de reconnaître et de tuer les cellules tumorales de la patiente. En revanche, de nombreux macrophages associés à la tumeur dans l’omentum étaient fortement chargés de gouttelettes lipidiques. Ces macrophages gavés de lipides présentaient des signes de stress oxydatif élevé — usure chimique liée aux espèces réactives de l’oxygène — et basculaient vers un état immunosuppresseur favorisant la tumeur. Autrement dit, ce même environnement riche en lipides qui peut nourrir des lymphocytes T efficaces pousse aussi les macrophages vers une voie délétère qui atténue l’attaque immunitaire globale.
Reprogrammer des macrophages suralimentés avec des médicaments existants
Les scientifiques se sont ensuite demandé s’il était possible de retourner ces macrophages stressés du côté des alliés. En utilisant des fragments tumoraux frais cultivés en laboratoire, ils ont testé deux approches. La première impliquait le maraviroc, un médicament anti‑VIH qui bloque CCR5, un récepteur de la molécule de signalisation immunitaire CCL5 abondante à la frontière tumeur‑graisse. L’autre ciblait CD36, un récepteur « épurateur » clé permettant aux macrophages d’importer des acides gras. Les deux traitements ont réduit la charge lipidique à l’intérieur des macrophages, diminué les marqueurs de stress oxydatif et de peroxydation lipidique délétère, et déclenché des vagues de signaux inflammatoires. Surtout, ils ont permis aux lymphocytes T cytotoxiques de se multiplier et de migrer de la périphérie graisseuse vers le cœur tumoral, renforçant l’activité immunitaire locale sans apporter de cellules immunitaires supplémentaires de l’extérieur.
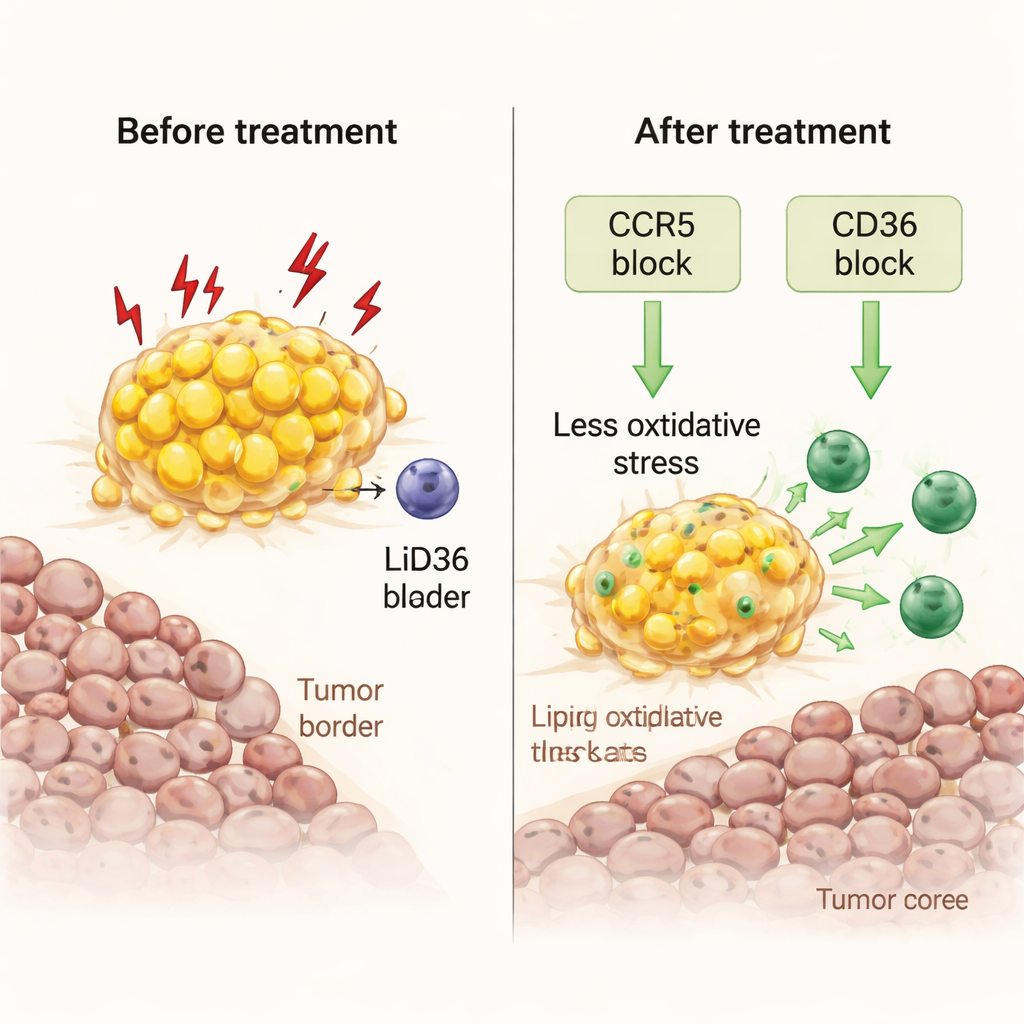
Des voies cellulaires aux modèles et patientes réels
Pour tester ces idées dans un contexte plus réaliste, l’équipe a utilisé des souris humanisées dotées d’un système immunitaire de type humain et leur a implanté des tumeurs mammaires humaines dans des tissus riches en graisse. Le traitement au maraviroc a reprogrammé les macrophages humains chez ces animaux de manière similaire aux échantillons dérivés de patientes : réduction des signatures lipidiques et de stress, augmentation de la production de cytokines et soutien renforcé des voies liées aux lymphocytes T. Cliniquement, les chercheurs ont réexaminé un essai japonais de nivolumab chez des patientes atteintes d’un cancer de l’ovaire résistant à la chimiothérapie. Toutes les patientes qui ont tiré bénéfice du médicament présentaient des métastases omentales visibles dans les échantillons chirurgicaux. En combinant des scanners CT ou IRM avec une analyse par apprentissage machine de la distribution des graisses corporelles, ils ont construit un arbre de décision capable de repérer de façon non invasive les patientes dont les tumeurs sont probablement proches de la graisse viscérale — et dans un cas prospectif, cette méthode a correctement prédit une patiente qui a ensuite répondu au nivolumab.
Ce que cela pourrait signifier pour les traitements futurs
Pour un non‑spécialiste, la conclusion est que « où » le cancer de l’ovaire se développe dans le corps, et la manière dont la graisse voisine reconfigure les cellules immunitaires, peuvent fortement influencer l’efficacité de l’immunothérapie. Les dépôts omentaux riches en graisse semblent abriter des lymphocytes T vigoureux mais aussi des macrophages suralimentés et stressés qui atténuent l’attaque. En allégeant la charge lipidique de ces macrophages et en réduisant leur détresse oxydative — grâce à des bloqueurs de CCR5 comme le maraviroc, des agents ciblant CD36 ou des stratégies apparentées — il pourrait être possible de transformer une réponse immunitaire partiellement bloquée en une offensive complète contre la tumeur. Parallèlement, des mesures d’imagerie de l’atteinte omentale pourraient aider les médecins à sélectionner les patientes les plus susceptibles de bénéficier des inhibiteurs de points de contrôle, ouvrant la voie à une approche plus personnalisée et potentiellement plus efficace du traitement du cancer de l’ovaire.
Citation: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Mots-clés: cancer de l’ovaire, tissu adipeux omental, immunothérapie, macrophages associés à la tumeur, métabolisme des lipides