Clear Sky Science · fr
GPR54 régule le développement du cancer du poumon non à petites cellules via la dopa-décarboxylase
Pourquoi cette histoire de cancer du poumon est importante
Le cancer du poumon reste l’un des cancers les plus meurtriers, et la plupart des cas correspondent à une forme appelée cancer du poumon non à petites cellules (CPNPC). De nombreux patients finissent par manquer d’options thérapeutiques efficaces parce que les tumeurs s’adaptent ou développent une résistance aux traitements actuels. Cette étude révèle un système de contrôle jusque-là peu reconnu à l’intérieur des cellules cancéreuses pulmonaires, centré sur un récepteur nommé GPR54 et une enzyme appelée dopa-décarboxylase (DDC). En comprenant comment ces molécules aident les tumeurs à croître et à s’alimenter, les chercheurs mettent en lumière de nouvelles voies pour ralentir ou même réduire le CPNPC.
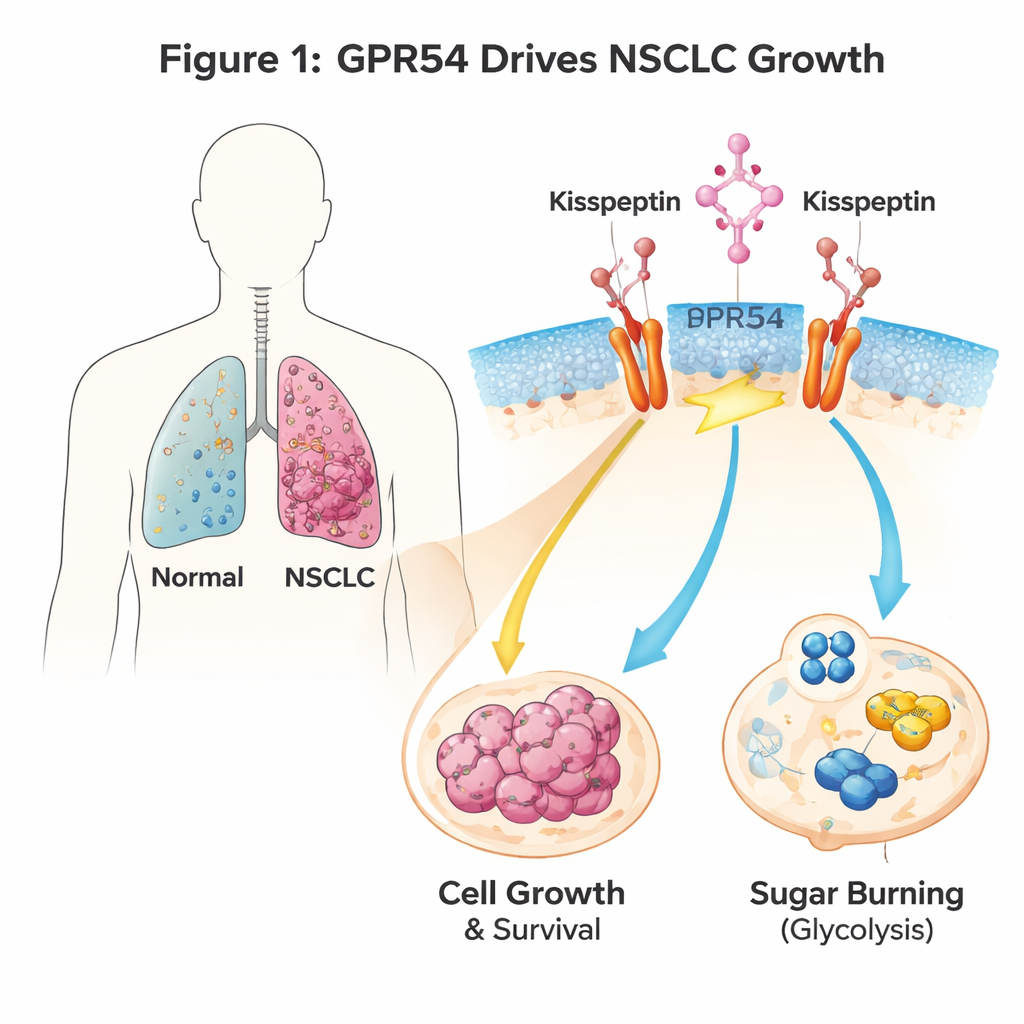
Un interrupteur de signal à la surface des cellules tumorales
GPR54 est un senseur situé à la surface des cellules qui répond à un signal naturel appelé kisspeptine. Il est surtout connu pour son rôle dans la puberté et la reproduction, mais il apparaît aussi dans de nombreux cancers. Les auteurs ont utilisé des souris génétiquement modifiées qui développent un CPNPC lorsqu’un gène oncogène appelé Kras est activé dans les cellules pulmonaires. En supprimant le gène Gpr54 chez ces souris, les animaux ont vécu plus longtemps, développé moins de tumeurs pulmonaires et de plus petite taille, et leurs cellules cancéreuses ont montré des signes nets d’autodestruction (apoptose). Les lignées cellulaires humaines de CPNPC racontent la même histoire : lorsque les niveaux de GPR54 étaient réduits, les cellules tumorales proliféraient plus lentement, formaient moins de colonies et mouraient plus facilement, indépendamment de leurs mutations génétiques particulières.
Comment GPR54 maintient les cellules tumorales en vie
En approfondissant, les chercheurs ont cherché quels circuits internes GPR54 utilise. Ils ont découvert que GPR54 alimente deux grandes voies de croissance intracellulaires, connues sous les noms AKT et ERK. Ce sont des « nœuds » courants qui poussent les cellules cancéreuses à se diviser et à résister à la mort. Lorsque GPR54 était bloqué ou supprimé, l’activité d’AKT et d’ERK diminuait et les cellules devenaient plus susceptibles à l’apoptose. Restaurer des signaux AKT ou ERK forts pouvait partiellement sauver les cellules, confirmant que GPR54 aide les cellules de CPNPC à survivre en s’appuyant sur ces circuits de croissance.
Réagencer l’utilisation du sucre par le cancer
Les cellules cancéreuses reprogramment souvent leur usage des nutriments, favorisant une dégradation rapide du sucre (glycolyse) pour alimenter la croissance. Le profil d’expression génique des tumeurs de souris dépourvues de Gpr54 montrait que de nombreux gènes impliqués dans la gestion du sucre et la production d’énergie étaient réprimés. Dans des cellules de cancer du poumon traitées par kisspeptine pour activer GPR54, les mesures d’utilisation d’oxygène et de production d’acide—indicateurs du métabolisme énergétique—ont révélé que GPR54 stimule la glycolyse. Bloquer la voie GPR54 à divers niveaux (le commutateur Gαq/11, PI3K, AKT ou mTOR) réduisait la consommation de glucose et la production de lactate et poussait les cellules vers l’apoptose. En termes simples, GPR54 aide les cellules de CPNPC à brûler le sucre plus vite et plus efficacement, soutenant ainsi leur croissance rapide.
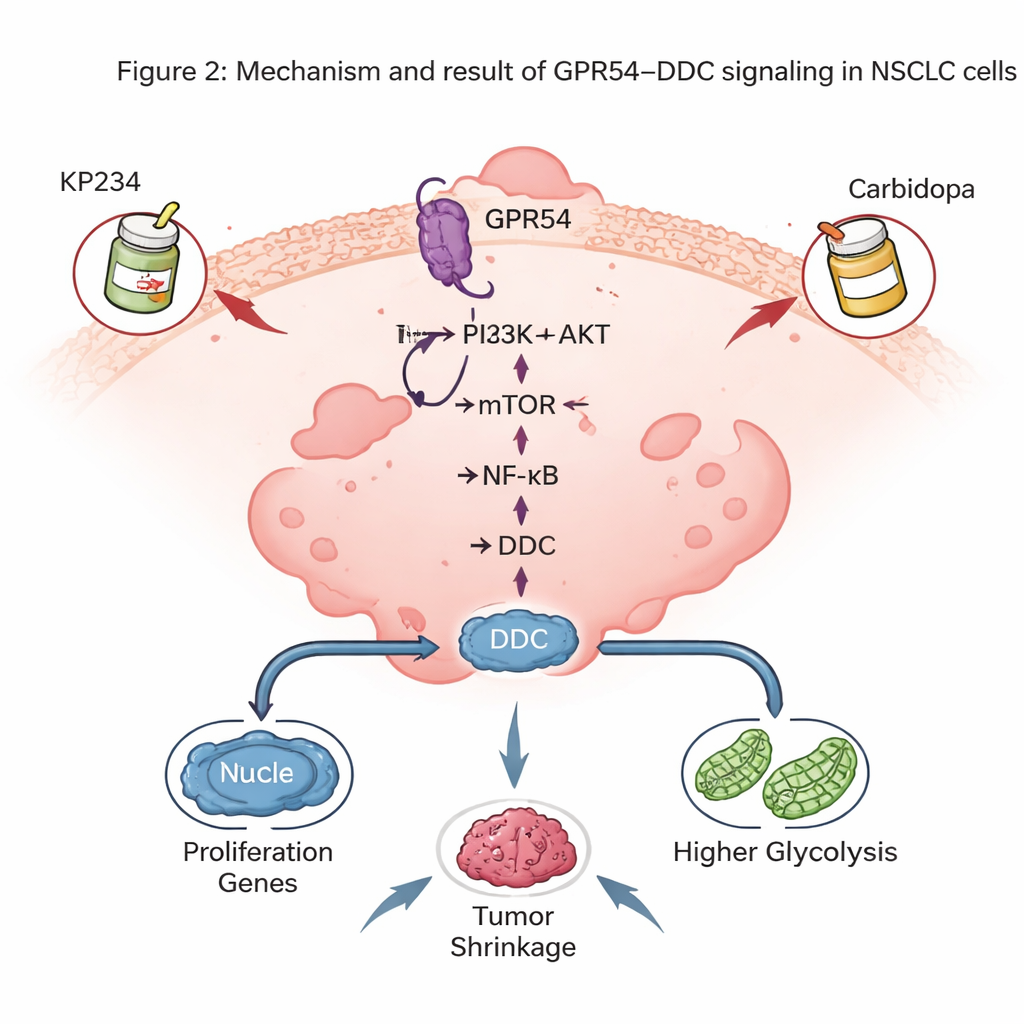
Le rôle surprenant d’une enzyme liée au cerveau
Une des découvertes les plus marquantes est que GPR54 contrôle les niveaux de DDC, une enzyme surtout connue pour synthétiser les neurotransmetteurs dopamine et sérotonine. Dans les tumeurs de souris, les niveaux de DDC suivaient de près ceux de GPR54 : moins de GPR54 signifiait moins de DDC. Les tumeurs humaines de CPNPC et les lignées cellulaires présentaient également davantage de DDC que les cellules pulmonaires normales, et les patients avec des taux élevés de DDC avaient une survie moindre. Réduire l’expression de DDC dans les cellules de cancer du poumon ralentissait la croissance tumorale chez la souris, diminuait la division cellulaire en culture et déclenchait davantage d’apoptose. Au niveau moléculaire, la DDC contribuait à maintenir l’activité de la voie NF-κB, un régulateur majeur qui favorise la survie des cellules cancéreuses et l’inflammation, et soutenait également l’état de glycolyse élevée des cellules tumorales.
Tester une stratégie d’association de médicaments
Parce que la DDC est déjà ciblée dans la maladie de Parkinson par un médicament appelé carbidopa, les auteurs ont exploré si combiner un bloqueur de GPR54 (KP234) avec la carbidopa pouvait frapper le CPNPC sur deux fronts. En cultures cellulaires et dans des modèles murins où des cellules humaines de CPNPC étaient implantées dans le poumon, le traitement combiné a réduit la croissance tumorale davantage que chaque médicament seul et augmenté la mort des cellules cancéreuses, sans perte de poids évidente chez les animaux. Ces associations ont aussi montré un potentiel en combinaison avec certains médicaments ciblés modernes visant des gènes RAS mutés, suggérant que la signalisation GPR54–DDC peut s’ajouter aux thérapies de précision existantes.
Ce que cela signifie pour les soins futurs du cancer du poumon
Pour un non-spécialiste, le message clé est que les cellules de CPNPC dépendent d’un partenariat jusqu’ici sous-estimé entre un interrupteur de surface (GPR54) et une enzyme métabolique (DDC) pour rester en vie et brûler du carburant rapidement. Perturber ce partenariat affaiblit les tumeurs, les faisant croître plus lentement et mourir plus facilement dans des modèles expérimentaux. Bien qu’il reste beaucoup de travail avant que de telles stratégies n’atteignent la clinique, cette étude positionne GPR54 et DDC comme des biomarqueurs potentiels pour identifier les CPNPC agressifs et comme des cibles prometteuses pour de nouvelles combinaisons thérapeutiques susceptibles d’améliorer le pronostic des patients dont les cancers échappent actuellement aux thérapies standard.
Citation: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Mots-clés: cancer du poumon non à petites cellules, GPR54, dopa-décarboxylase, métabolisme du cancer, thérapie ciblée