Clear Sky Science · fr
Espèces réactives de l’oxygène (ROS) dans le cancer : du mécanisme aux implications thérapeutiques
Quand des molécules utiles deviennent dangereuses
À l’intérieur de chaque cellule, de minuscules étincelles chimiques appelées espèces réactives de l’oxygène, ou ROS, sont constamment produites dans le cadre du fonctionnement normal. À des niveaux appropriés, elles aident les cellules à croître, à communiquer et à se défendre contre les microbes. Mais cette revue explique comment ces mêmes molécules peuvent aussi endommager l’ADN, perturber l’architecture cellulaire et favoriser la croissance, la dissémination et la résistance aux traitements des cancers. Comprendre cette « double vie » des ROS aide les chercheurs à concevoir de nouvelles thérapies anticancéreuses qui cherchent soit à calmer le stress oxydatif nuisible, soit à le pousser délibérément au-delà d’un seuil létal pour tuer les cellules tumorales.
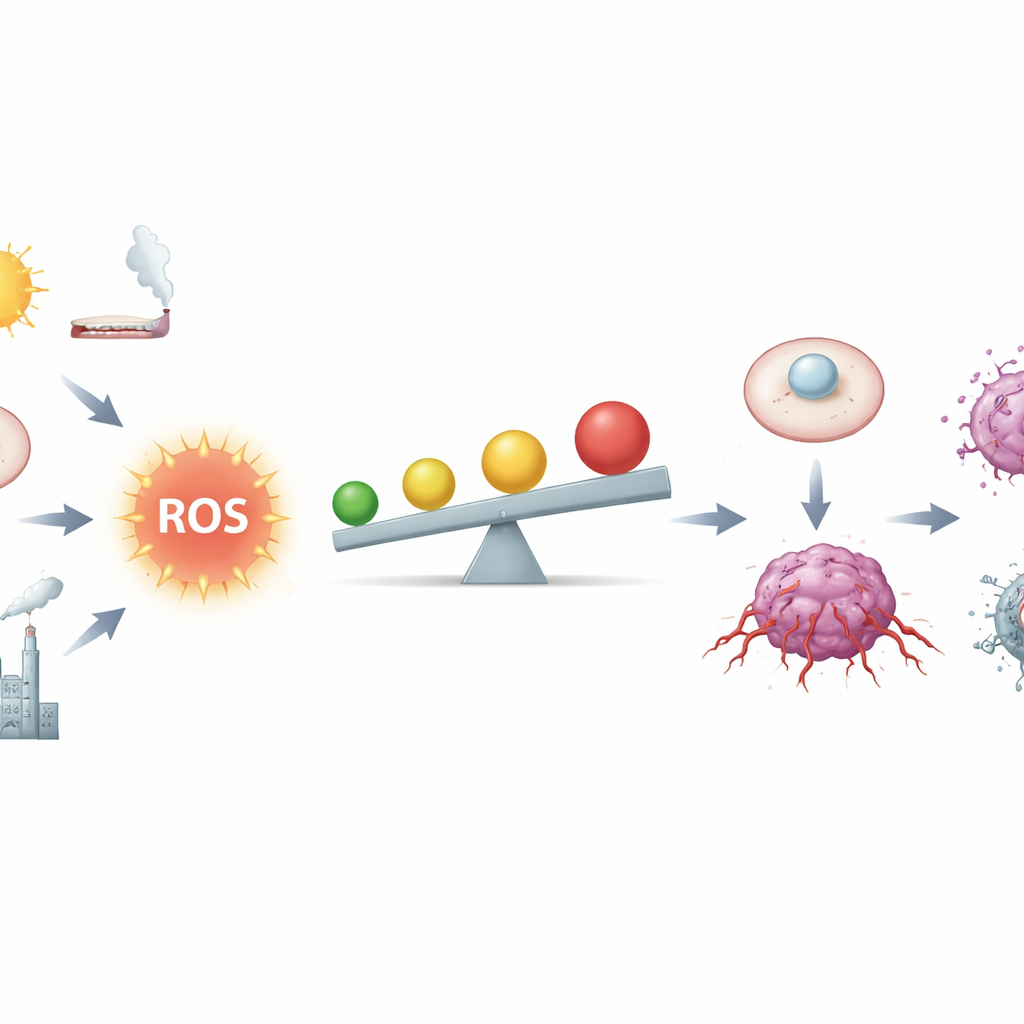
La ligne fine entre carburant et incendie
Les auteurs décrivent les ROS comme des sous-produits chimiques de la respiration et du métabolisme, mais aussi comme de puissants messagers. Dans les tissus sains, de faibles quantités de ROS contribuent au contrôle du cycle cellulaire, à la réparation des dommages et à l’ajustement fin de l’immunité. Les cellules maintiennent ces signaux en équilibre grâce à un réseau complexe d’antioxydants, comprenant des molécules comme le glutathion et des enzymes régulées par un commutateur maître appelé Nrf2. Les cellules cancéreuses, en revanche, vivent plus près de la zone de danger : des gènes défectueux, des mitochondries surmenées, l’inflammation chronique, le tabac, les radiations et certains métaux augmentent tous les ROS. À des niveaux modérément élevés, les ROS peuvent entailler l’ADN, déstabiliser les chromosomes et activer de manière chronique des circuits de croissance et de survie, facilitant la transformation d’une cellule normale en cellule cancéreuse.
Comment le stress oxydatif façonne le comportement tumoral
Une fois la tumeur établie, les ROS continuent de modeler sa biologie. Un stress oxydatif modéré active de nombreuses voies de croissance qui encouragent la division cellulaire, la néovascularisation, l’invasion des tissus voisins et la résistance à la chimiothérapie. Les ROS peuvent reprogrammer l’usage des sucres, des graisses et des acides aminés par les cellules cancéreuses, orientant les carburants vers des voies qui produisent davantage de pouvoir antioxydant et des éléments de construction pour de nouvelles cellules. Ils influencent aussi les décisions de destin cellulaire : selon l’intensité et le contexte, les ROS peuvent basculer l’équilibre vers des signaux de survie ou vers l’une des formes de mort cellulaire programmée, y compris l’apoptose classique et des formes plus récentes comme la ferroptose, la nécroptose et la cuproptose. Cela fait des ROS à la fois des complices de la progression tumorale et des déclencheurs potentiels de l’autodestruction tumorale.
Réécrire l’immunité et la réponse aux médicaments
La revue souligne que les ROS n’agissent pas seulement à l’intérieur des cellules cancéreuses — ils remodelent le voisinage tumoral. Un stress oxydatif élevé peut épuiser ou tuer les lymphocytes T et les cellules tueuses naturelles qui combattent le cancer, tout en favorisant des cellules suppressives qui protègent la tumeur des attaques. Les ROS aident également les tumeurs à augmenter des signaux « ne me tuez pas » tels que les protéines de point de contrôle, atténuant l’effet des immunothérapies. En parallèle, des ROS modérés peuvent favoriser la résistance aux médicaments en stimulant des pompes d’efflux et des réponses de stress, permettant aux cellules cancéreuses d’expulser la chimiothérapie ou de réparer les dégâts qu’elle provoque. Pourtant, dans d’autres conditions, pousser les ROS au-delà d’un seuil critique peut démanteler ces défenses et resensibiliser les tumeurs au traitement.
Transformer une faiblesse redox en stratégie thérapeutique
Parce que les cellules cancéreuses marchent sur une corde raide entre l’utilisation des ROS et leur intoxication, les auteurs considèrent l’équilibre des ROS comme un levier thérapeutique. Une stratégie générale consiste à réduire les ROS nocifs ou à renforcer les antioxydants, principalement pour la prévention ou pour protéger les tissus sains pendant le traitement. Une autre consiste à faire l’inverse dans les tumeurs : inhiber les systèmes antioxydants ou augmenter la production de ROS jusqu’à ce que les cellules cancéreuses franchissent un seuil létal, en particulier en combinaison avec la radiothérapie, des médicaments ciblés ou l’immunothérapie. Une troisième approche vise à laisser intact le niveau de ROS mais à bloquer les interrupteurs sensibles aux ROS — protéines de signalisation, enzymes métaboliques ou voies de mort cellulaire — dont les tumeurs dépendent. À travers ces idées ressort le thème de la personnalisation : différents cancers portent différentes « signatures redox », si bien que les thérapies futures pourraient nécessiter des tests sanguins ou tissulaires de dommages oxydatifs, de capacité antioxydante et de gènes liés aux ROS pour choisir le traitement redox adapté à chaque patient.
Ce que cela signifie pour les patients
En termes simples, cet article soutient que les ROS ne sont ni purement mauvaises ni purement bonnes ; ce sont des outils puissants que les cellules, et les cancers, utilisent. Les cellules cancéreuses ont tendance à fonctionner plus près d’un point de bascule de stress oxydatif que les cellules saines, ce qui peut créer une fenêtre thérapeutique. Toutefois, comme les antioxydants et les pro-oxydants peuvent à la fois aider ou nuire selon la dose, le moment et le type de tumeur, l’usage généralisé de suppléments ou de médicaments augmentant les ROS est risqué. Les auteurs concluent que l’avenir réside dans des thérapies et des diagnostics soigneusement conçus qui lisent l’état redox de chaque tumeur puis ajustent les ROS et les systèmes antioxydants juste ce qu’il faut — soit en les abaissant pour protéger les tissus normaux, soit en les augmentant pour pousser les cellules cancéreuses au-delà de leur point de rupture.
Citation: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Mots-clés: espèces réactives de l’oxygène, stress oxydatif, métabolisme du cancer, thérapie redox, microenvironnement tumoral