Clear Sky Science · fr
Analyse de concordance des profils ADN et ARN : l'étude IMPACT2 du MD Anderson en oncologie de précision
Pourquoi cette recherche compte pour les patients atteints de cancer
Le traitement du cancer est de plus en plus guidé par le profil génétique de chaque tumeur. Les médecins utilisent déjà des tests ADN pour repérer des mutations ciblables par des médicaments spécifiques, mais ces tests ne disent pas tout du comportement d’une tumeur. Cette étude du MD Anderson Cancer Center pose une question pratique : si l’on examine aussi l’ARN — les « copies actives » des gènes qui indiquent lesquels sont effectivement activés ou désactivés — peut‑on mieux comprendre le cancer d’un patient et ses chances de survie ?
Deux couches d’information : ADN et ARN
Chaque cellule cancéreuse porte des altérations de son ADN, mais l’ADN est surtout un plan relativement statique. L’ARN, en revanche, reflète ce que la cellule fait activement à un instant donné. Dans l’essai IMPACT2, plus de 800 patients atteints de cancers avancés ont vu leurs tumeurs profilées génétiquement. Pour 253 d’entre eux, les chercheurs disposaient à la fois de données ADN et ARN. Ils ont comparé quels gènes étaient altérés au niveau ADN (par exemple mutations ou copies supplémentaires) et quels gènes présentaient des niveaux d’ARN anormalement élevés ou faibles, afin de déterminer à quelle fréquence ces deux couches racontaient la même histoire et si ces informations étaient liées à la durée de survie des patients.
Quand modifications génétiques et activité concordent
L’équipe a d’abord recherché des événements « concordants » : des cas où un même gène était anormal au niveau de l’ADN et de l’ARN. Parmi les 253 patients, 50 présentaient au moins une telle correspondance, pour un total de 58 événements répartis sur 23 gènes. La plupart impliquaient des copies en excès ou manquantes d’un gène qui montrait également des niveaux d’ARN plus élevés ou plus faibles, et cette concordance était la plus nette pour des oncogènes et suppresseurs tumoraux connus tels que CDKN2A, AR, ESR1, KRAS, PIK3CA, AKT2, TP53 et CCND1. Ces résultats confortent l’idée que, pour certains gènes clés du cancer, des altérations structurelles de l’ADN se traduisent effectivement par une augmentation ou une diminution de l’activité génique, renforçant leur intérêt comme cibles thérapeutiques.
Relations cachées révélées par les signaux ARN
Au‑delà des correspondances un à un, les chercheurs ont testé plus de 12 000 paires de gènes pour voir si une altération ADN d’un gène était systématiquement associée à des niveaux d’ARN anormaux dans un autre. Ils ont identifié 123 paires significatives. Beaucoup se regroupaient au sein d’un réseau majeur de croissance et de survie connu sous le nom de voie PI3K/AKT, cible fréquente de médicaments dirigés. Un schéma particulièrement notable reliait des altérations du gène suppresseur TP53 à des signaux ARN hyperactifs de VEGFA, un gène qui aide les tumeurs à former de nouveaux vaisseaux sanguins. Cette relation pourrait contribuer à expliquer pourquoi certains patients dont les tumeurs présentent des altérations de TP53 répondent au bevacizumab, un médicament qui bloque la néovascularisation, et illustre comment les données ARN peuvent révéler des interactions gène–gène cliniquement pertinentes que l’ADN seul peut manquer.
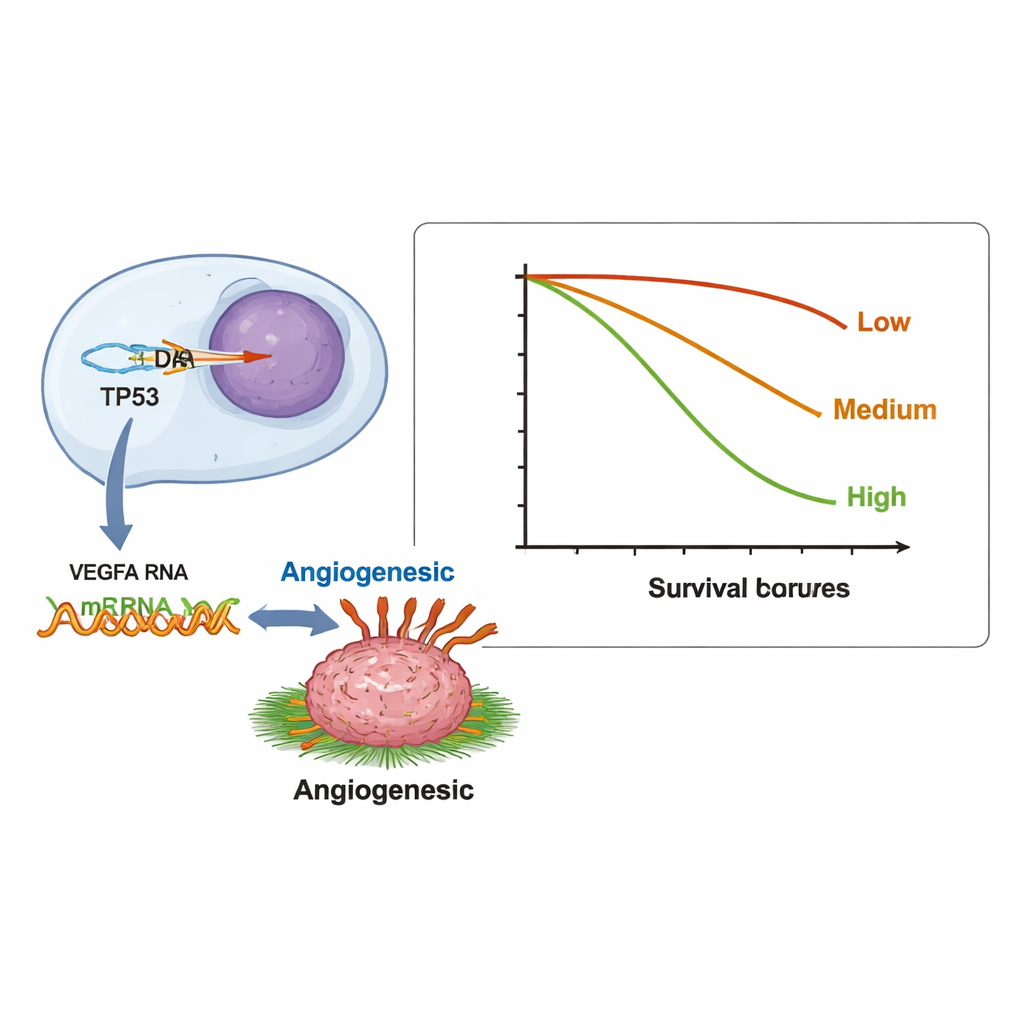
Charge d’activité génique et survie des patients
Les investigateurs se sont également demandé si la quantité globale d’activité génique anormale dans une tumeur — ce qu’ils appellent la charge transcriptionnelle tumorale, ou TTB — était liée à la durée de survie des patients. Ils ont compté le nombre de gènes présentant des niveaux d’ARN altérés chez chaque patient et les ont classés en faibles (0–2 gènes), intermédiaires (3–5) et élevés (6 ou plus). Les patients du groupe élevé avaient une survie médiane de 6,7 mois, contre 9,8 et 11,9 mois dans les groupes inférieurs. Autrement dit, les tumeurs présentant de nombreux gènes dysfonctionnels au niveau de l’ARN avaient tendance à être plus agressives. Les tumeurs dépourvues de PD‑L1, un marqueur souvent utilisé pour sélectionner les patients pour l’immunothérapie, avaient également tendance à présenter davantage de gènes à expression anormale, suggérant un lien possible entre une perturbation génique étendue et un microenvironnement tumoral résistant à l’attaque immunitaire.
Ce que cela signifie pour les soins du cancer à venir
Cette étude montre que le profilage ARN apporte une information utile et complémentaire aux tests ADN chez des patients réels atteints de cancers avancés. Pour certains gènes, les altérations de l’ADN et l’activité ARN se correspondent et confirment des cibles thérapeutiques connues ; pour d’autres, les motifs ARN dévoilent de nouvelles relations susceptibles d’orienter le choix des médicaments, comme le lien entre TP53 et VEGFA. Surtout pour les patients, une forte charge d’activité génique anormale s’est associée à une survie plus courte, ce qui suggère que des mesures basées sur l’ARN pourraient aider les cliniciens à évaluer l’agressivité d’une tumeur et à affiner le pronostic. Bien que le test ARN ne soit pas encore utilisé routinièrement pour sélectionner les thérapies, ces résultats soutiennent son potentiel comme étape suivante en oncologie de précision, en particulier à mesure que des études de plus grande envergure et de meilleurs outils d’analyse facilitent l’intégration du profilage transcriptomique dans la pratique clinique quotidienne.
Citation: Schmidt, S.T., Baysal, M.A., Fu, S. et al. Concordance analysis of DNA and RNA profiling: The MD Anderson IMPACT2 study in precision oncology. Sig Transduct Target Ther 11, 68 (2026). https://doi.org/10.1038/s41392-026-02580-0
Mots-clés: onco‑précision, profilage ARN, séchage de l'ADN, charge transcriptionnelle tumorale, biomarqueurs du cancer