Clear Sky Science · fr
Les sous-types moléculaires consensuels du carcinome épidermoïde de l’œsophage
Pourquoi cette recherche compte pour les patients
Le carcinome épidermoïde de l’œsophage est un cancer agressif de la gorge avec peu d’options de traitement personnalisées et une survie généralement mauvaise. Les médecins savent que tous les tumeurs ne se comportent pas de la même façon, mais jusqu’à présent il n’existait pas de méthode claire et unifiée pour classer ces cancers en groupes biologiquement pertinents. Cette étude rassemble de nombreux fils de données génétiques et d’imagerie pour définir quatre principaux types de ce cancer et montre qu’une simple image de lame de microscope peut souvent révéler le type dont souffre un patient. Cela ouvre la voie à des traitements plus précis, évitant en partie l’approche par essais‑erreurs.
Remettre de l’ordre dans un paysage tumoral confus
Au cours de la dernière décennie, différentes équipes de recherche ont proposé au moins sept façons de diviser ce cancer sur la base de mutations d’ADN, de variations du nombre de copies, d’activité génique ou d’autres mesures moléculaires. Chaque système utilisait des données et des méthodes différentes, conduisant à des sous‑types qui se recoupent mais ne sont pas identiques, ce qui complique leur utilisation en pratique clinique. Les auteurs ont d’abord réanalysé un groupe bien caractérisé de 152 patients chinois pour lesquels plusieurs couches de données étaient disponibles, y compris le séquençage du génome entier, l’expression génique, la méthylation de l’ADN et les profils de microARN. En utilisant une méthode appelée similarity network fusion, ils ont combiné toutes ces données en une image unique et identifié quatre sous‑types multi‑omiques. Ils ont ensuite construit un « réseau des sous‑types » statistique qui reliait leurs nouveaux groupes à 21 classifications publiées antérieurement, révélant de fortes connexions entre les études.
Quatre personnalités biologiques principales de la tumeur
À partir de ce réseau, l’équipe a extrait quatre sous‑types moléculaires consensuels, nommés ECMS1 à ECMS4, chacun présentant un comportement distinct. ECMS1, le type métabolique (MET), montre une activité élevée dans les voies qui traitent les médicaments et les nutriments et une activation fréquente du gène NFE2L2, qui peut favoriser la résistance à la chimiothérapie et à la radiothérapie. ECMS2, le type classique (CLS), est dominé par une forte activité du cycle cellulaire et des signaux de croissance, et comporte souvent des copies supplémentaires du gène ERBB2 (HER2). ECMS3, le type immunitaire (IM), présente une charge mutationnelle globale plus faible mais une activation marquée du système immunitaire, notamment des niveaux élevés de la voie de point de contrôle PD‑1. ECMS4, le type mésenchymateux (MES), montre des signes de remodelage tissulaire, d’angiogenèse et d’une mobilité/invasion cellulaires accrues, des caractéristiques associées à un pronostic plus défavorable.
Lier les sous‑types au pronostic et aux choix thérapeutiques
Lorsque les chercheurs ont confronté ces quatre groupes aux données cliniques des patients, des schémas clairs sont apparus. Les patients porteurs de tumeurs mésenchymateuses ECMS4 présentaient le risque de récidive le plus élevé et les pires survies globale et sans maladie. Le groupe immunitaire ECMS3, malgré son environnement immunitaire actif, répondait mal à la chimioradiothérapie standard mais montrait un taux de bénéfice plus élevé avec un médicament d’immunothérapie anti‑PD‑1. Les tumeurs classiques ECMS2 semblaient plus sensibles aux chimiothérapies courantes telles que le cisplatine et les taxanes, et leur amplification fréquente de HER2 suggère qu’elles pourraient bénéficier de traitements ciblant HER2. Les tumeurs métaboliques ECMS1, enrichies en activité NFE2L2 et en certains récepteurs de facteurs de croissance, pourraient être mieux traitées par des médicaments ciblant ces voies métaboliques et de signalisation. En bref, les quatre sous‑types suggèrent des points faibles différents et des réponses probables distinctes aux thérapies.
Apprendre à un ordinateur à repérer des indices moléculaires sur des lames de routine
Parce que le profilage moléculaire complet est coûteux et indisponible dans de nombreux hôpitaux, l’équipe s’est demandé si des lames de pathologie ordinaires colorées à l’hématéine et à l’éosine (H&E) pouvaient faire office de substitut. Ils ont entraîné un système d’apprentissage profond sur des dizaines de milliers d’extraits d’images annotés pour reconnaître des éléments tissulaires de base tels que les cellules tumorales, le stroma, les lymphocytes, les glandes et le muscle. À partir d’images de lames entières, ils ont ensuite calculé des « caractéristiques d’organisation spatiale » – la proportion de chaque type de tissu, leur agencement et leur degré de mélange ou de séparation. Ces motifs dérivés des images reflétaient la biologie des quatre sous‑types : par exemple, le type immunitaire ECMS3 montrait plus de lymphocytes et de structures normales, tandis que le type mésenchymateux ECMS4 présentait davantage de stroma de soutien. À partir de ces caractéristiques, ils ont construit un classificateur basé sur l’image, appelé imECMS, capable d’assigner des lames à MET, CLS, IM ou MES avec une bonne précision dans plusieurs cohortes indépendantes de patients.
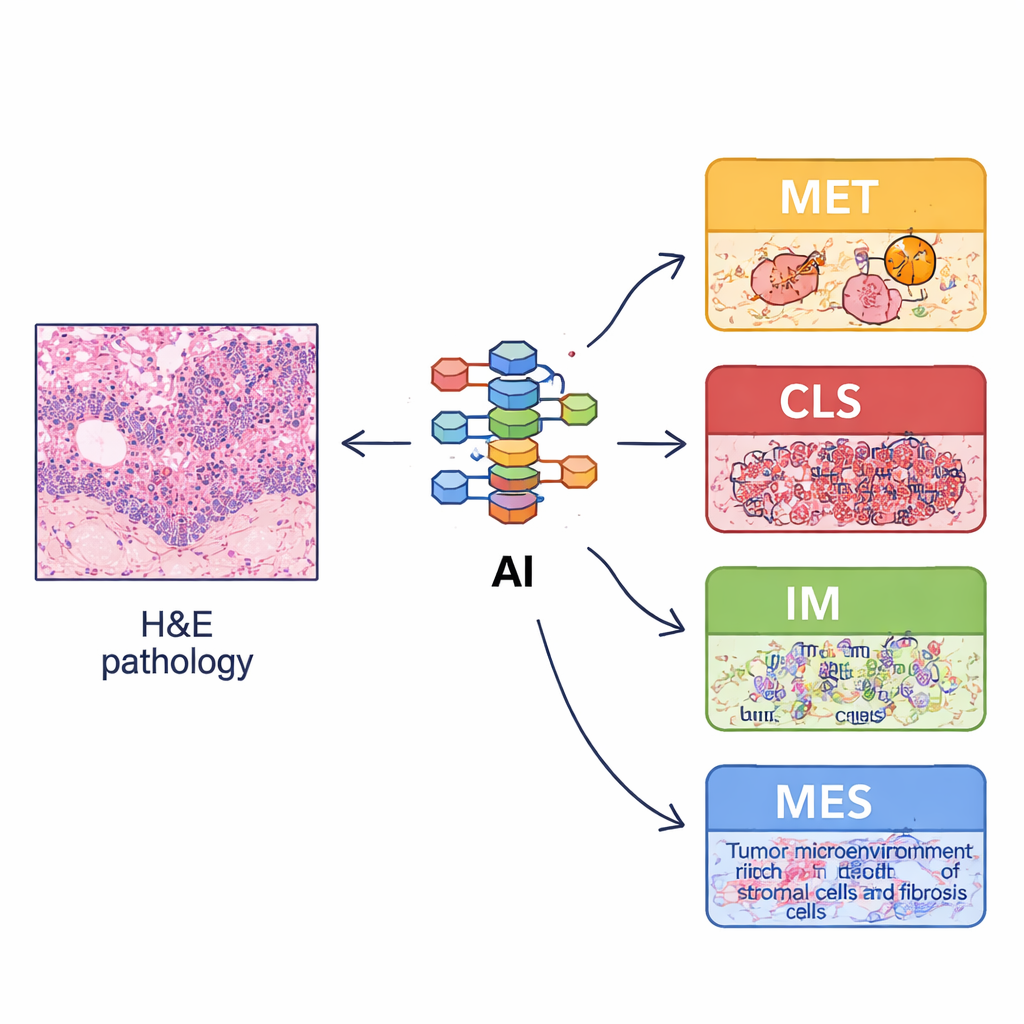
Ce que cela signifie pour les soins futurs
Pour les non‑spécialistes, la conclusion est que cette étude transforme un cancer apparemment uniforme en quatre maladies biologiquement distinctes, chacune avec son évolution probable et ses meilleures stratégies thérapeutiques. Plus important encore, elle montre qu’une grande partie de ces informations peut être extraite automatiquement d’images microscopiques standard que chaque patient possède déjà, sans nécessiter un séquençage coûteux. Après validation complémentaire sur des populations plus larges et plus diverses, les systèmes ECMS et imECMS pourraient aider les médecins à assortir les patients atteints d’un carcinome épidermoïde de l’œsophage aux traitements dont ils ont le plus de chances de bénéficier, tout en les épargnant d’options peu susceptibles d’être efficaces.
Citation: Cui, H., Zhu, Z., Xu, E. et al. The consensus molecular subtypes of esophageal squamous cell carcinoma. Sig Transduct Target Ther 11, 65 (2026). https://doi.org/10.1038/s41392-026-02577-9
Mots-clés: cancer de l’œsophage, sous-types tumoraux, oncologie de précision</keyword-oncology> <keyword>pathologie par apprentissage profond, immunothérapie