Clear Sky Science · fr
L’hyperglutaminolyse entraîne la sénescence et le vieillissement via l’activation de l’axe arginine-mTORC1
Pourquoi cette recherche est importante pour le vieillissement en bonne santé
Le vieillissement n’est pas seulement une question de rides et de cheveux gris : il reflète la perte progressive par les cellules de tout l’organisme de leur capacité à réparer et à se renouveler. Cette étude pose une question apparemment simple mais aux implications majeures : la manière dont nos cellules métabolisent l’acide aminé glutamine contribue-t‑elle réellement à les pousser vers la sénescence ? Les auteurs mettent au jour une chaîne métabolique jusque-là masquée qui relie le traitement de la glutamine à un interrupteur de croissance puissant, mTORC1, et montrent qu’une stimulation excessive de cette voie peut accélérer activement le vieillissement cellulaire chez la mouche et la souris.
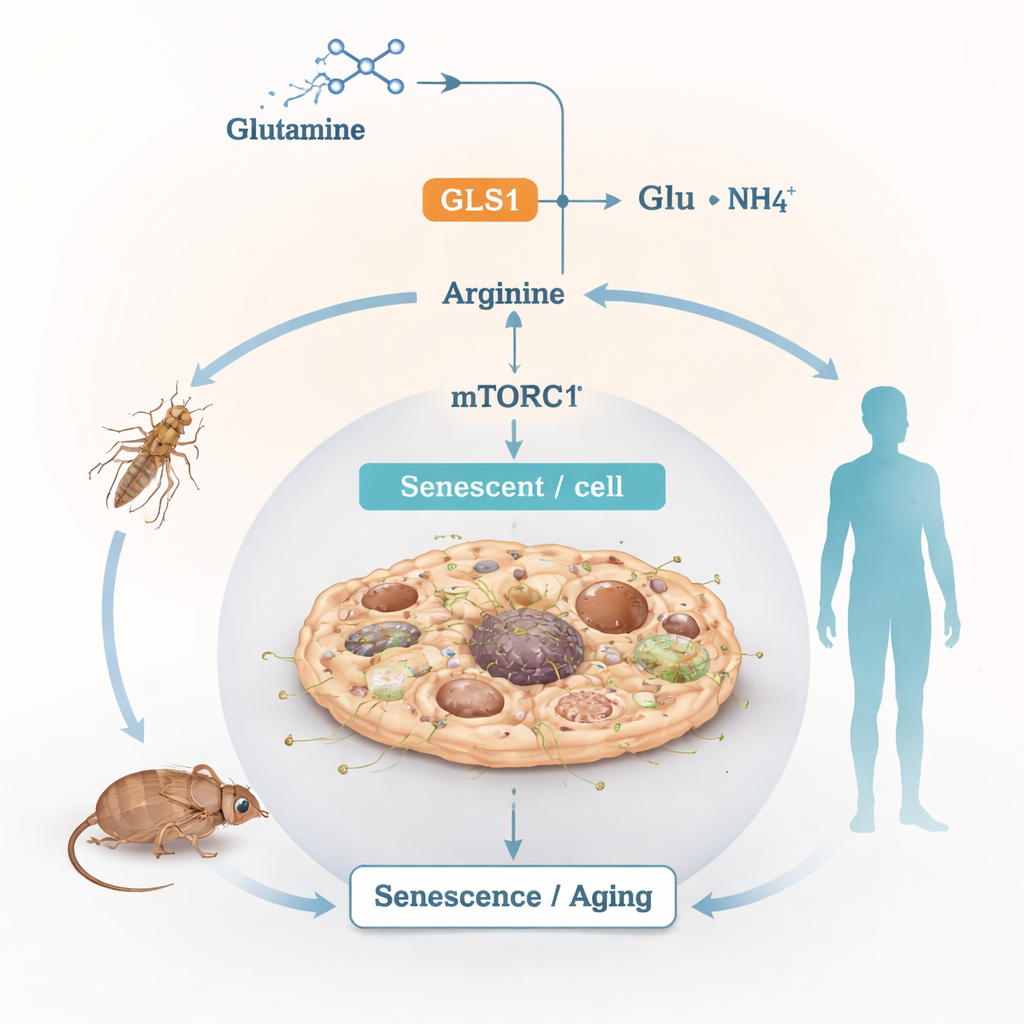
Une ligne d’alimentation qui chauffe trop
La glutamine est l’acide aminé libre le plus abondant dans notre sang et nos tissus. Les cellules l’utilisent comme carburant polyvalent et comme élément de construction, en la dégradant via un processus appelé glutaminolyse. La première étape est assurée par une enzyme nommée GLS1, qui convertit la glutamine en glutamate et en ammonium ; ces produits alimentent ensuite la production d’énergie, les défenses antioxydantes et la synthèse d’autres acides aminés. Si cette dégradation est cruciale pour la vie normale, les auteurs se sont demandé ce qui se passe lorsqu’elle devient de manière chronique hyperactive dans le contexte du vieillissement et du stress.
Découverte de « l’hyperglutaminolyse » dans les cellules et organismes âgés
Grâce à un profilage avancé des métabolites, l’équipe a comparé des cellules jeunes et proliférantes à des cellules sénescentes — des cellules âgées ayant cessé de se diviser et sécrétant des facteurs inflammatoires. Ils ont constaté que de nombreux acides aminés étaient augmentés, la glutamine occupant le centre du réseau réorganisé. Les cellules sénescentes consommaient davantage de glutamine, présentaient des niveaux et une activité supérieurs de GLS1, et accumulaient plus de glutamate et d’ammonium. Des changements similaires ont été observés au niveau des organismes entiers : des mouches âgées et des souris âgées montraient une activité GLS élevée dans plusieurs tissus. Les auteurs ont qualifié cet état partagé d’accélération de la dégradation de la glutamine « d’hyperglutaminolyse », suggérant qu’il s’agit d’une caractéristique conservée du vieillissement plutôt que d’un simple effet secondaire.
Réduire la dégradation de la glutamine ralentit les signes du vieillissement
Si l’hyperglutaminolyse accompagne le vieillissement, contribue‑t‑elle réellement à le provoquer ? Pour le tester, les chercheurs ont bloqué la glutaminolyse de plusieurs manières : en diminuant la glutamine dans le milieu de culture, en inhibant GLS avec des médicaments, ou en réduisant génétiquement GLS1. Dans des cellules stressées ou vieillies par réplication, ces interventions ont réduit des marqueurs classiques de sénescence tels que la coloration SA-β-gal, l’inhibiteur du cycle cellulaire p16, et les signaux inflammatoires du « SASP ». Chez la mouche, soit l’invalidation génétique de GLS, soit de faibles doses d’inhibiteurs de GLS ont prolongé la durée de vie, amélioré la capacité d’escalade (test de vigueur) et réduit la fuite intestinale liée à l’âge. Il est important de noter que lorsque la glutaminolyse était limitée dès le début de l’exposition au stress, l’effet ne résultait pas principalement de l’élimination des cellules âgées, mais de la prévention de leur entrée en sénescence.
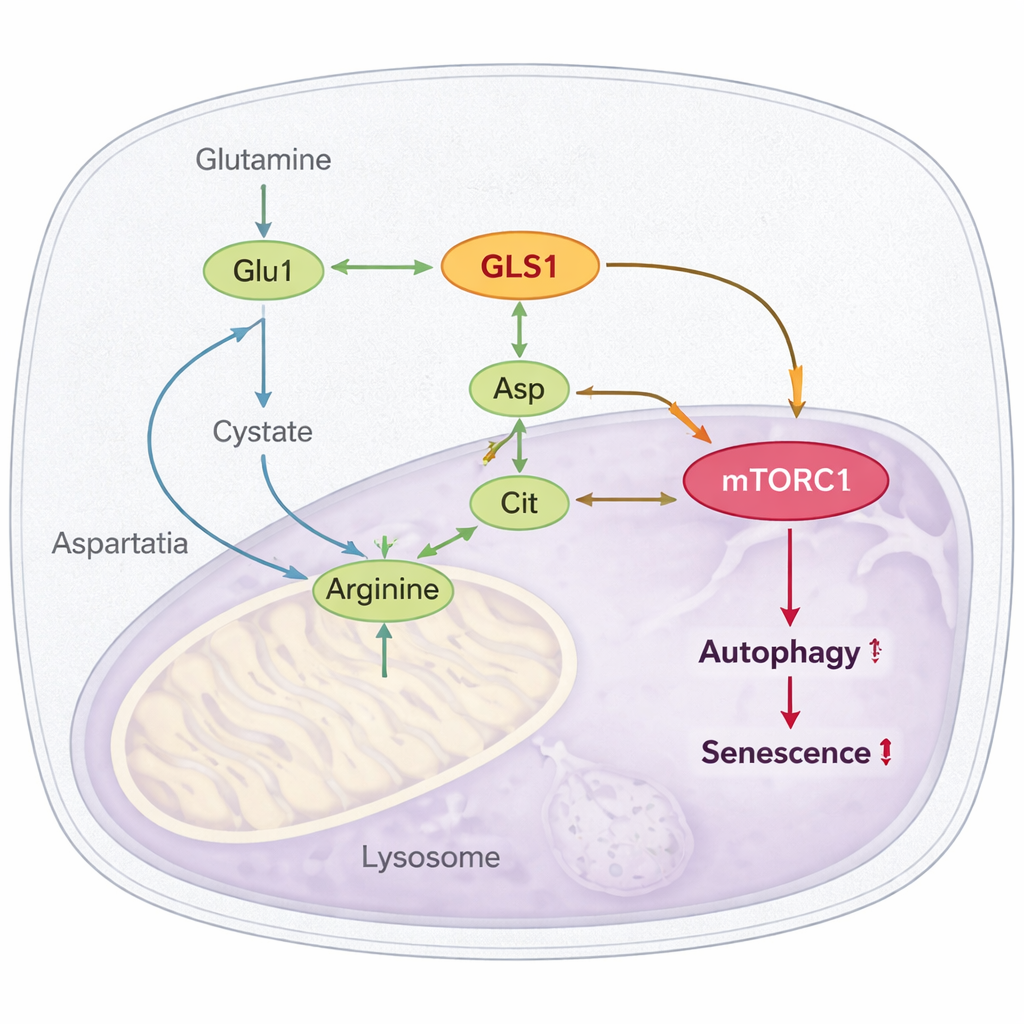
Un circuit caché : de la glutamine à l’arginine puis à mTORC1
La découverte la plus frappante est la façon dont cette voie hyperactive se connecte à mTORC1, un régulateur maître qui, lorsqu’il est activé de façon persistante, favorise le vieillissement et bloque le recyclage cellulaire (autophagie). Les auteurs montrent que l’hyperglutaminolyse augmente la production d’arginine, un autre acide aminé qui active directement mTORC1. Le glutamate et l’ammonium générés à partir de la glutamine alimentent la production d’aspartate et de citrulline, qui sont ensuite combinés pour former l’arginine. Dans les cellules et les mouches âgées, les niveaux d’arginine et de ses précurseurs augmentent ; bloquer GLS ou abaisser l’expression d’une enzyme clé de synthèse de l’arginine (ASL) réduit l’arginine et atténue l’activité de mTORC1. Ils démontrent en outre que la protéine détectrice d’arginine CASTOR1 est requise pour cet effet : lorsque CASTOR1 est désactivée, l’inhibition de la glutaminolyse n’apaise plus mTORC1 ni n’améliore l’autophagie, et la réduction de la sénescence disparaît.
Quand trop de bonnes choses accélère le vieillissement
Pour savoir si la simple stimulation de cette voie peut accélérer le vieillissement cellulaire, l’équipe a submergé des cellules autrement saines de glutamine, d’arginine ou de combinaisons de métabolites intermédiaires pendant des semaines. Le résultat a été une augmentation nette des marqueurs de sénescence et des gènes inflammatoires. Chez la mouche, une supplémentation à long terme en glutamine ou en arginine a réduit la durée de vie médiane et maximale. Pris ensemble, les travaux décrivent une cascade complète : une dégradation excessive de la glutamine (hyperglutaminolyse) amplifie la production d’arginine, laquelle est détectée par CASTOR1, maintient mTORC1 anormalement actif, supprime le nettoyage cellulaire et favorise la sénescence et le vieillissement de l’organisme.
Ce que cela signifie pour les stratégies anti‑âge futures
Pour le grand public, cette étude reconfigure le métabolisme de la glutamine comme une arme à double tranchant : nécessaire à la santé, mais potentiellement nuisible lorsqu’il est chroniquement surexcité à l’âge moyen et avancé. En cartographiant une route concrète de la catabolisme de la glutamine à la suractivation de mTORC1, les auteurs mettent en évidence de nouveaux points d’intervention — tels que les enzymes GLS1 et ASL ou l’étape de détection de l’arginine — qui pourraient être modulés pour ralentir le déclin lié à l’âge sans couper complètement un métabolisme vital. Bien qu’il soit beaucoup trop tôt pour traduire ces conclusions en conseils diététiques ou en traitements, le travail apporte une pièce importante au puzzle de la façon dont le traitement quotidien des nutriments peut orienter nos cellules vers la résilience ou vers un vieillissement accéléré.
Citation: Chen, H., Huang, N., Xu, W. et al. Hyperglutaminolysis drives senescence and aging through arginine-mTORC1 axis activation. Sig Transduct Target Ther 11, 64 (2026). https://doi.org/10.1038/s41392-026-02576-w
Mots-clés: métabolisme du glutamine, sénescence cellulaire, signalisation mTORC1, biosynthèse de l’arginine, interventions contre le vieillissement