Clear Sky Science · fr
La protéine nucléaire 1 du virus Epstein–Barr exogène induit une résistance tumorale pilotée par ADAR1 contre l’immunothérapie
Pourquoi un virus courant compte pour le traitement du cancer
De nombreux cancers sont aujourd’hui traités par des immunothérapies qui libèrent le système immunitaire de l’organisme. Pourtant, la plupart des patients n’en bénéficient pas, car leurs tumeurs apprennent à se camoufler contre l’attaque immunitaire. Cette étude révèle comment un virus très répandu, le virus Epstein–Barr (EBV), aide les tumeurs à désactiver leurs défenses immunitaires et à résister à ces traitements puissants — et comment un nouveau type de molécule conçue pourrait réactiver ces défenses.
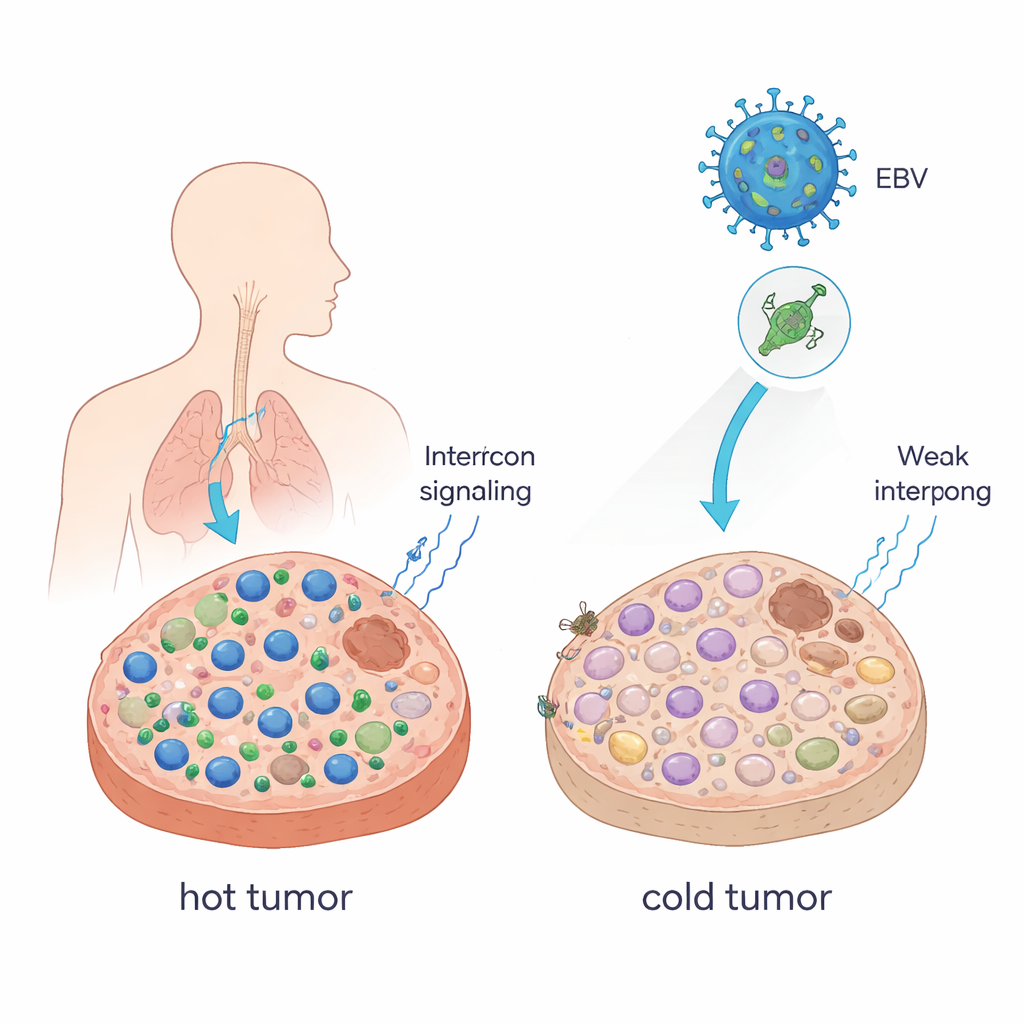
Transformer des tumeurs « chaudes » en tumeurs « froides »
Les médecins décrivent souvent les tumeurs comme « chaudes » lorsqu’elles sont riches en lymphocytes T cytotoxiques, et « froides » lorsque ces cellules sont rares. Les tumeurs chaudes répondent généralement bien aux inhibiteurs de points de contrôle immunitaire (ICB) tels que les anticorps anti–PD-1 ; les tumeurs froides souvent non. Les auteurs montrent qu’une seule protéine d’EBV, appelée EBNA1, peut pousser les tumeurs vers cet état plus froid et évasif. Lorsqu’ils ont forcé des cellules tumorales de souris à produire EBNA1 et les ont implantées dans des souris au système immunitaire intact, les tumeurs sont devenues plus volumineuses, contenaient moins de cellules CD8+ et de cellules tueuses naturelles, et comportaient davantage de macrophages immunosuppresseurs. Les signaux appelés interférons — messagers clés qui mobilisent les cellules immunitaires — étaient également fortement réduits. Dans des échantillons de patients atteints d’un carcinome du nasopharynx, un cancer étroitement lié à EBV, les tumeurs exprimant EBNA1 présentaient de la même façon moins de cellules CD8+ que les tissus normaux.
Un raccourci viral vers la machinerie de contrôle de l’ARN de la cellule
Pour comprendre comment EBNA1 reconfigure le microenvironnement tumoral, les chercheurs ont recherché des protéines humaines qui interagissent physiquement avec elle. Ils se sont focalisés sur une protéine appelée IGF2BP3, qui lit des marques chimiques (m6A) sur les ARNm et peut en augmenter la stabilité ou la traduction en protéines. EBNA1 se liait fortement à IGF2BP3 dans plusieurs types cellulaires, y compris des cellules cancéreuses EBV-positives. Des données issues de tumeurs de patients montraient que des niveaux élevés d’IGF2BP3 s’accompagnaient d’une activité réduite des gènes liés aux interférons et d’une moindre infiltration de cellules T CD8+, suggérant que cette alliance virus–hôte pourrait atténuer l’immunité antitumorale.
Augmentation d’un éditeur d’ARN qui étouffe les signaux de danger
Une analyse plus approfondie a mis en évidence une cible clé de cette interaction : ADAR1, une enzyme qui édite l’ARN double brin en convertissant certaines lettres « A » en « I ». Cette édition peut rendre l’ARN ressemblant à du viral à l’intérieur des cellules moins détectable par les senseurs internes, réduisant les réponses en interférons. Les auteurs ont trouvé qu’EBNA1, IGF2BP3 et un facteur de traduction nommé EIF4G1 forment un complexe tripartite sur l’ARNm d’ADAR1. Ce complexe augmente l’étiquetage m6A, recrute la machinerie de traduction et stimule sélectivement la production de protéine ADAR1 sans augmenter les niveaux d’ARNm. En conséquence, les cellules tumorales réalisent plus d’éditions d’ARN dans des éléments génétiques répétitifs situés près de gènes liés aux interférons. Ces modifications réduisent le pool d’ARN double brin non édité qui alerterait normalement des senseurs tels que MDA5 et PKR, atténuant la production d’interférons et aidant les tumeurs à se cacher de l’attaque immunitaire.
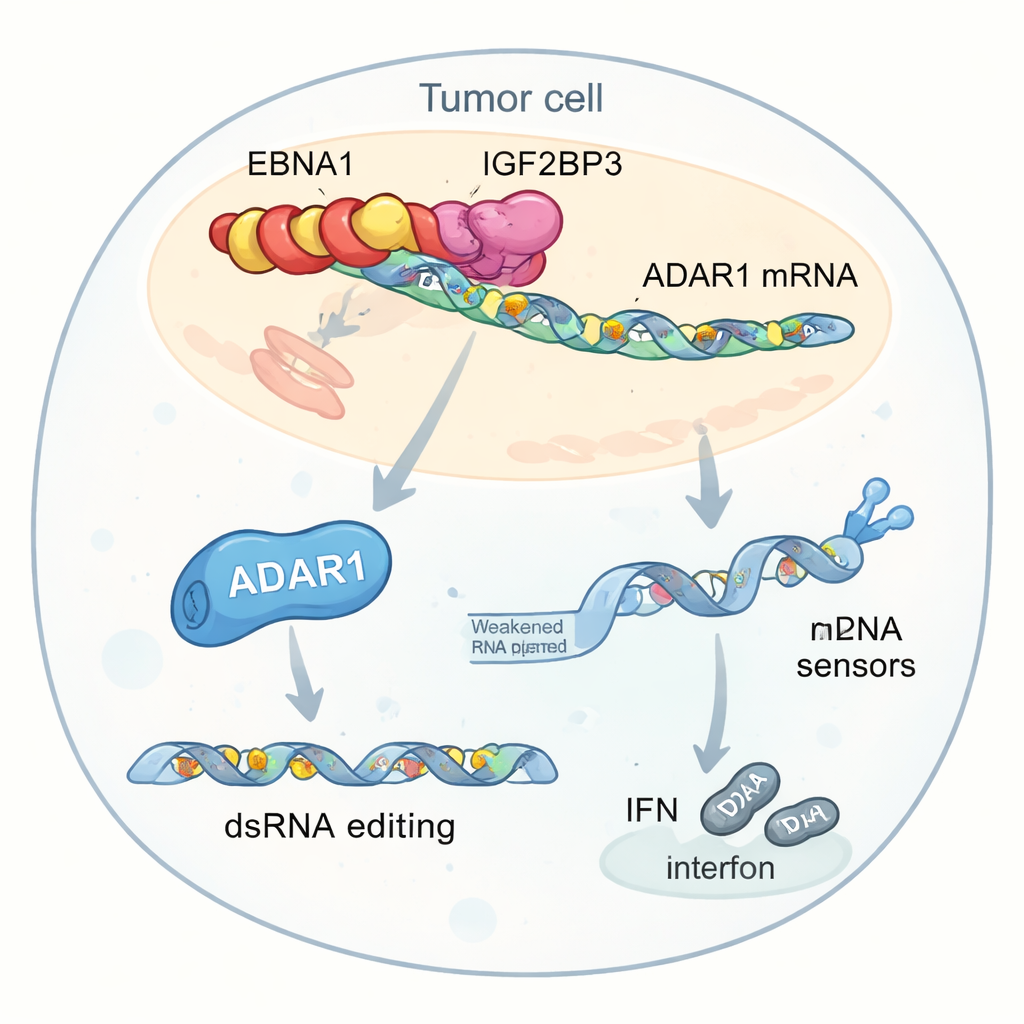
Moins d’interféron, immunothérapie affaiblie
Quand des cellules tumorales exprimant EBNA1 ont été exposées à des lymphocytes T et à des anticorps anti–PD-1 en laboratoire, elles étaient plus difficiles à tuer que des cellules témoins et libéraient moins d’interféron. Même traitées directement avec de l’interféron, les cellules porteuses d’EBNA1 étaient moins sensibles, et leurs senseurs d’ARN internes étaient moins fortement activés. Réduire les niveaux d’ADAR1 a partiellement renversé ces effets, restaurant l’activité des senseurs et la signalisation par interféron. Des expériences génétiques et de séquençage ont confirmé que les cellules exprimant EBNA1 présentaient davantage d’événements d’édition A-to-I dans des régions d’ARN spécifiques, en particulier après stimulation par l’interféron, soutenant l’idée que la stimulation virale d’ADAR1 aide à neutraliser les signaux de danger qui déclencheraient autrement de fortes réponses immunitaires.
Un dégradaeur conçu qui ranime l’attaque immunitaire
L’équipe s’est ensuite demandé si dépouiller les tumeurs d’EBNA1 pourrait restaurer leur vulnérabilité à l’immunothérapie. Ils ont conçu une molécule PROTAC, EP-1215, qui marque EBNA1 pour destruction par le système d’élimination de la cellule. À faibles doses, EP-1215 dégradait efficacement EBNA1 et réduisait les niveaux de protéine ADAR1. Dans des expériences chez la souris, EP-1215 seul avait un impact limité sur les tumeurs EBNA1-positives, et l’anti–PD-1 seul était également faible. Mais combinés, les deux traitements réduisaient fortement la taille des tumeurs, augmentaient l’infiltration des cellules T CD8+ et stimulaient les lymphocytes T producteurs d’interféron. Dans des modèles murins humanisés portant des cellules immunitaires humaines et des tumeurs liées à EBV, la combinaison surpassait à nouveau les traitements isolés, sans toxicité hépatique ou rénale évidente.
Ce que cela signifie pour les soins oncologiques futurs
Pour les non-spécialistes, le message est qu’un virus courant peut silencieusement reprogrammer les cellules cancéreuses pour atténuer leurs systèmes d’alarme internes, en éteignant des signaux chimiques qui attireraient et activeraient autrement les cellules immunitaires. EBNA1 fait cela en détournant un lecteur d’ARN de l’hôte (IGF2BP3) et un facteur de traduction (EIF4G1) pour surproduire l’éditeur d’ARN ADAR1, qui édite les structures d’ARN mêmes que les senseurs immunitaires sont conçus pour reconnaître. En dégradant EBNA1 avec un PROTAC sur mesure comme EP-1215, les auteurs ont pu restaurer ces signaux de danger et rendre des tumeurs résistantes à nouveau sensibles aux médicaments anti-points de contrôle existants. Si des stratégies similaires s’avèrent sûres et efficaces chez l’humain, cibler des complices viraux tels qu’EBNA1 pourrait offrir une nouvelle manière de convertir des tumeurs froides liées à EBV en cibles « chaudes » que les immunothérapies modernes pourront enfin atteindre.
Citation: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Mots-clés: Virus Epstein-Barr, résistance à l’immunothérapie, ADAR1, édition de l’ARN, carcinome du nasopharynx