Clear Sky Science · fr
Mécanisme moléculaire de la fusion membranaire dépendante du cholestérol lors de l’entrée du SARS-CoV-2
Pourquoi le cholestérol compte pour un virus respiratoire
Le virus responsable de la COVID-19, le SARS-CoV-2, pénètre dans nos cellules en fusionnant son enveloppe externe avec les membranes cellulaires. Cet article pose une question apparemment simple mais aux grandes implications : dans quelle mesure le cholestérol — une substance lipidique mieux connue pour son rôle dans les maladies cardiovasculaires — module-t-il cette étape de fusion ? Les auteurs montrent que le cholestérol dans la membrane virale ne se contente pas d’ajuster l’efficacité d’infection ; il organise en fait les protéines spike du virus en plateformes d’ancrage puissantes qui facilitent et fiabilisent l’entrée.
Construire un modèle minimal de l’entrée virale
Pour disséquer ce processus, les chercheurs ont reconstitué la rencontre virus–cellule dans une éprouvette en utilisant de petites bulles lipidiques appelées liposomes. Un jeu de liposomes portait la protéine spike du SARS-CoV-2 et représentait la membrane virale ; l’autre portait le récepteur ACE2, mimant la surface des cellules hôtes. Lorsqu’ils furent mélangés et activés par des enzymes spécifiques qui « coupent » la spike pour la rendre prête à fusionner, ces membranes artificielles ont fusionné, permettant à un colorant fluorescent de passer d’une bulle à l’autre. Ce système simplifié a permis à l’équipe d’ajuster précisément la composition lipidique — y compris le taux de cholestérol — de chaque côté et d’observer la fusion étape par étape. 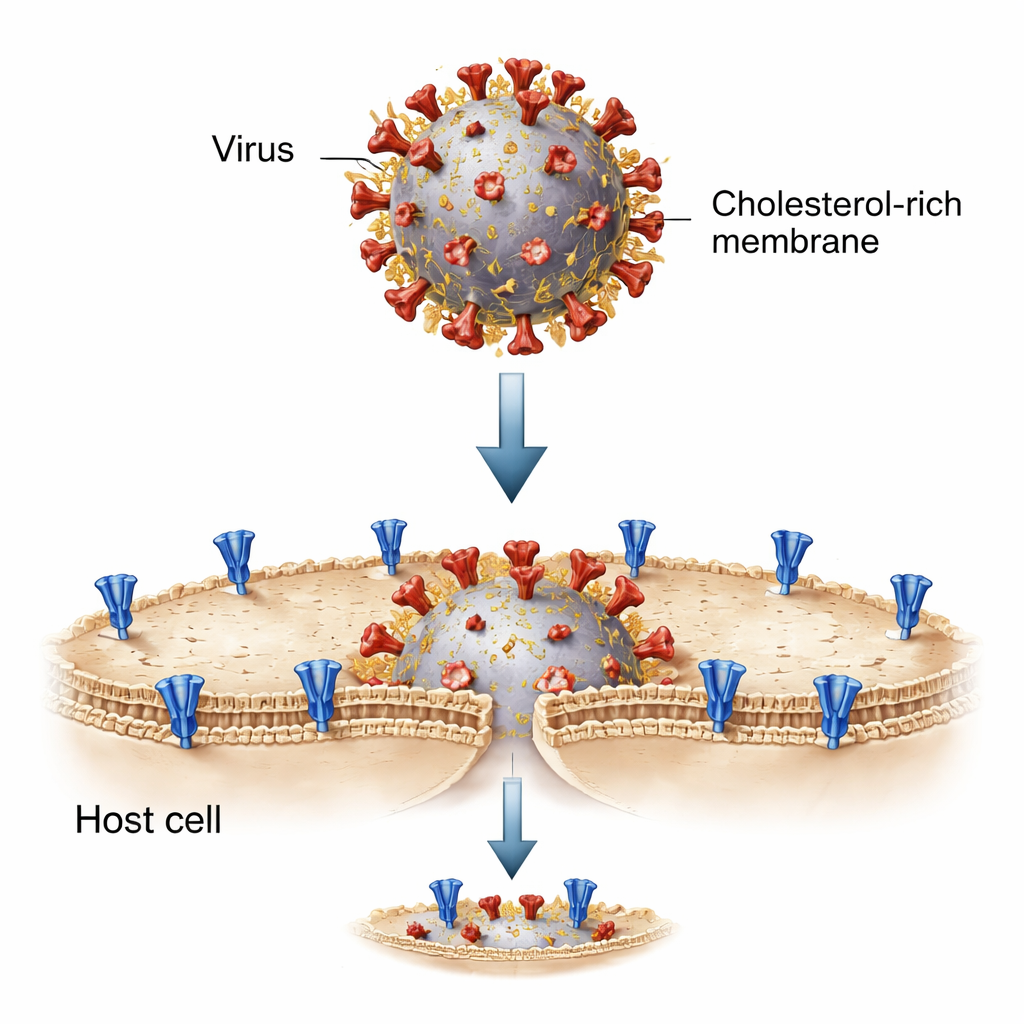
Le cholestérol favorise davantage l’ancrage que la fusion
En faisant varier la quantité de cholestérol, l’équipe a découvert que l’ajout de cholestérol dans la membrane porteuse de la spike augmentait la fréquence de fusion, mais pas de la manière qu’on pourrait attendre. Un taux élevé de cholestérol ne modifiait pas de façon spectaculaire la probabilité que deux membranes déjà appariées fusionnent réellement. En revanche, il augmentait fortement la fréquence à laquelle les vésicules portant la spike s’ancrent d’abord sur les vésicules porteuses d’ACE2. L’imagerie à l’échelle d’une seule particule a montré beaucoup plus d’événements d’ancrage réussis lorsque la spike se trouvait dans des membranes riches en cholestérol, tandis que la probabilité qu’une paire appariée fusionne complètement restait globalement constante. Il est intéressant de noter que charger l’autre côté (celui avec ACE2) en cholestérol apportait peu d’avantage et qu’à des niveaux très élevés cela gênait même la fusion, ce qui suggère que c’est le cholestérol viral — et non celui de l’hôte — qui est le principal moteur.
Des membranes modèles aux cellules vivantes
Les chercheurs ont ensuite vérifié si le même schéma se retrouvait dans des cellules vivantes. Ils ont modifié génétiquement des cellules humaines pour qu’elles expriment soit la spike soit ACE2 et ont observé la formation de larges structures fusionnées, ou syncytia, lorsqu’elles étaient mises en contact. L’élimination du cholestérol des cellules exprimant la spike a presque aboli la formation de syncytia, tandis que la restauration du cholestérol a rétabli la fusion. Dans des expériences parallèles avec des « pseudovirus » SARS-CoV-2 (particules virales inoffensives utilisant la spike pour entrer dans les cellules), la déplétion du cholestérol membranaire viral réduisait fortement l’infection, et son réapprovisionnement l’augmentait de manière dépendante de la dose. En revanche, modifier seulement le cholestérol des cellules exprimant ACE2 produisait peu de changement. Tous les tests convergent vers le même message : le cholestérol dans la membrane contenant la spike est essentiel pour une entrée efficace.
Amas de spike : l’arme secrète du cholestérol
Pourquoi le cholestérol du côté viral serait-il si déterminant ? L’imagerie à haute résolution des membranes cellulaires a révélé que les protéines spike tendent à former des amas denses lorsque le cholestérol est abondant, mais restent plus dispersées lorsqu’il est appauvri. Des mesures monomoléculaires ont approfondi ces observations en montrant que ces amas contiennent davantage de copies de la spike dans des conditions riches en cholestérol. Les auteurs ont relié cet effet à une région riche en cystéines (RRC) à l’extrémité de la queue de la spike, à l’intérieur de la membrane virale. Ce segment est modifié par la palmitoylation — un type d’ancrage lipidique qui favorise les domaines riches en cholestérol. Lorsque l’équipe a tronqué la queue de la spike ou a muté les dix cystéines pour bloquer la palmitoylation, la spike ne s’est plus agrégée avec le cholestérol, et le gain d’ancrage et de fusion induit par le cholestérol a disparu. 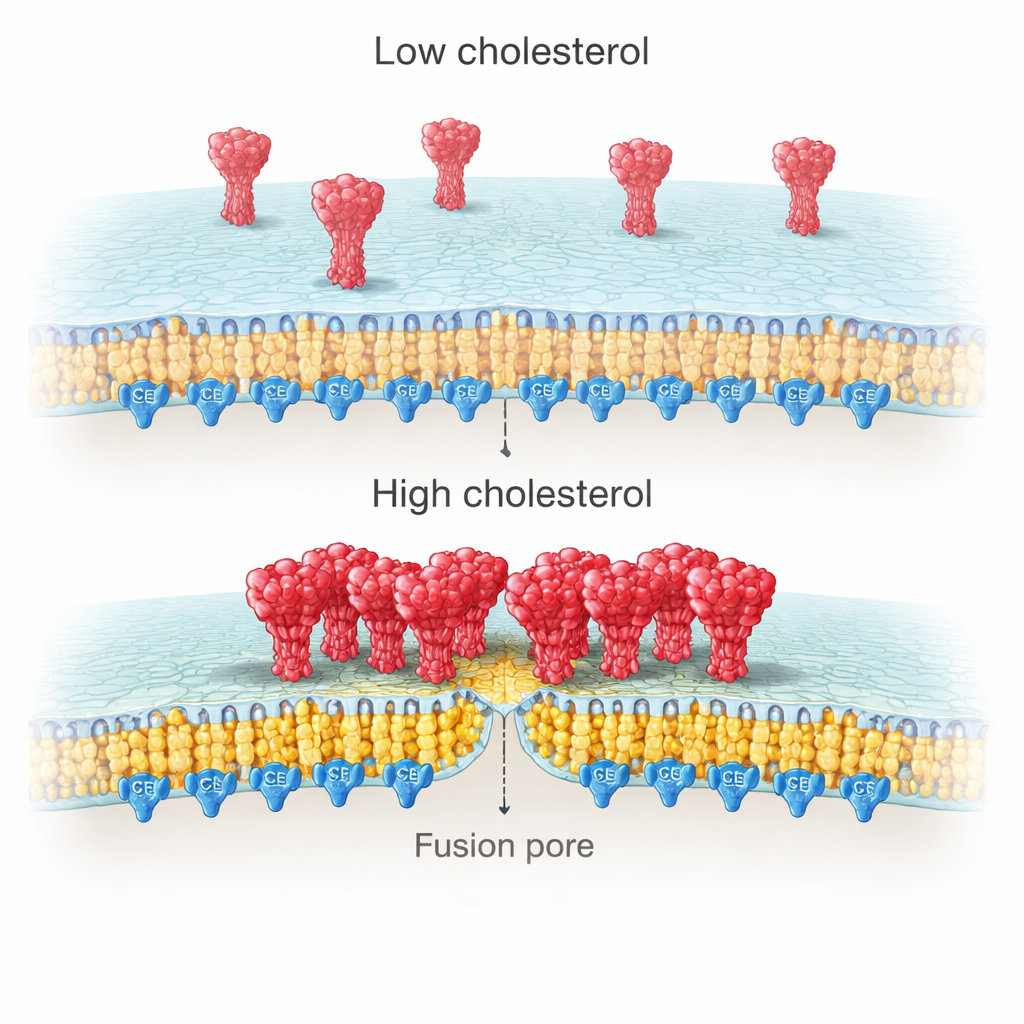
Comment cela pourrait aider les traitements futurs
En résumé, l’étude conclut que le cholestérol transforme la membrane virale en une plateforme de fusion en rassemblant de nombreuses protéines spike en amas serrés via leur région de queue palmitoylée. Ces amas s’ancrent plus efficacement sur l’ACE2 des cellules hôtes, augmentant les chances qu’une rencontre donnée aboutisse à une fusion et à une infection réussies. Pour les non-spécialistes, l’idée clé est que le cholestérol n’est pas un simple composant passif de l’enveloppe virale ; il est un organisateur actif de la machinerie spike. Cela fait de la queue riche en cystéines, sensible au cholestérol, et des enzymes qui la palmitoylent, des cibles prometteuses pour des stratégies antivirales à large spectre susceptibles d’être efficaces contre différentes variantes de coronavirus.
Citation: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Mots-clés: cholestérol, spike du SARS-CoV-2, fusion membranaire, entrée virale, palmitoylation