Clear Sky Science · fr
PKC-eta favorise les métastases du cancer du sein en régulant la voie de signalisation Hippo–YAP
Pourquoi cette recherche est importante
Le cancer du sein triple négatif (TNBC) est l’une des formes les plus dangereuses de cancer du sein car il se propage tôt et manque de traitements ciblés. Cette étude révèle comment une enzyme spécifique à l’intérieur des cellules cancéreuses, appelée PKC‑eta (PKCη), fonctionne comme un interrupteur maître qui aide les tumeurs à se détacher, migrer dans l’organisme et engendrer de nouvelles tumeurs. En comprenant ce mécanisme, les chercheurs identifient aussi un petit peptide naturel capable de l’éteindre, ouvrant la voie à une stratégie thérapeutique potentielle contre cette maladie agressive. 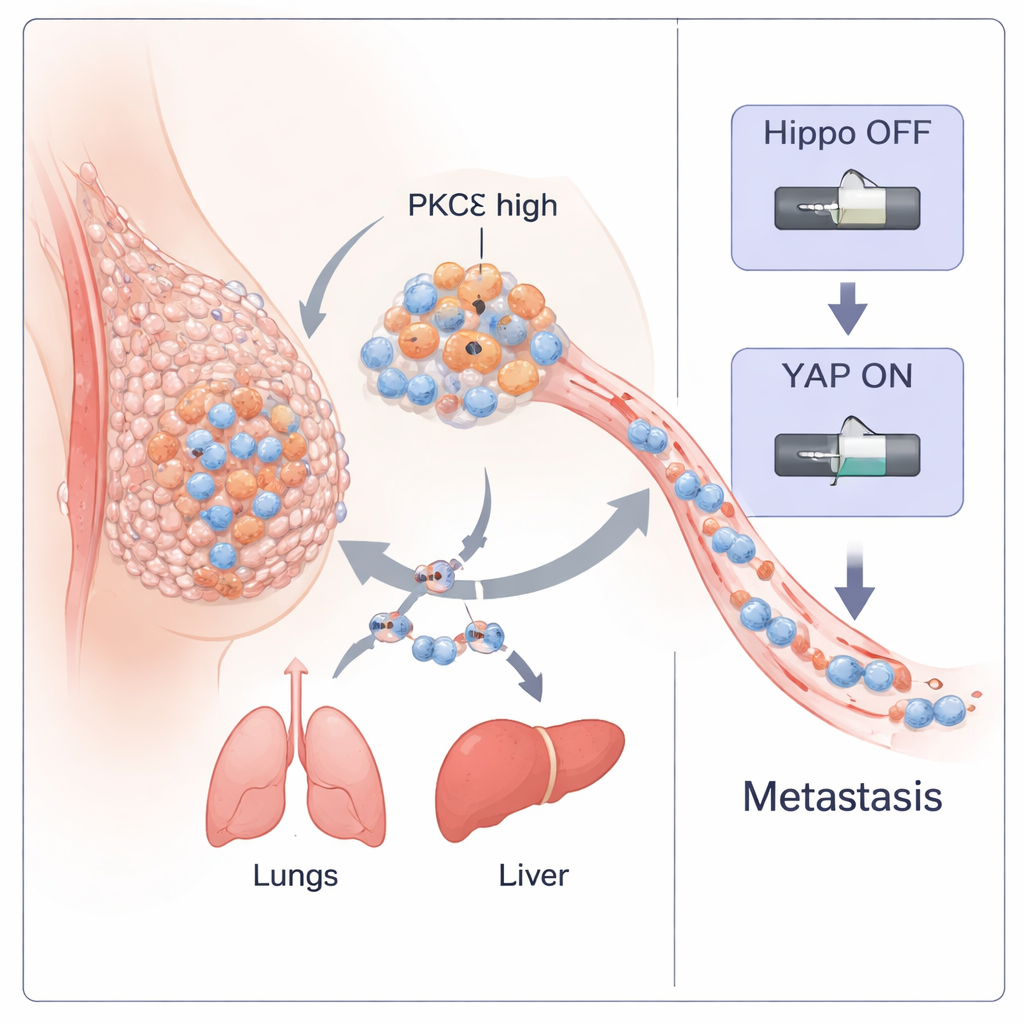
Un moteur caché dans les tumeurs agressives
L’équipe a commencé par explorer de larges bases de données de patientes atteintes de cancer du sein. Ils ont constaté que le gène codant PKCη (PRKCH) est particulièrement élevé dans un sous‑type tumoral dit « claudin‑low », qui chevauche fortement le TNBC et est riche en cellules de type souches, très mobiles. Dans plusieurs cohortes, les tumeurs présentant un fort niveau de PRKCH affichaient des signatures marquées de transition épithélio‑mésenchymateuse (EMT) — un processus où des cellules auparavant ordonnées relâchent leurs jonctions, changent de forme et deviennent plus invasives. Les niveaux de PRKCH étaient également plus élevés dans les échantillons métastatiques que dans les tumeurs primaires, et la coloration protéique des tissus humains TNBC montrait une PKCη active, perinucléaire, plus prononcée dans les cancers de grade élevé et avancés. Ensemble, ces observations suggèrent que PKCη est étroitement liée à l’agressivité et à la dissémination tumorale.
De la boîte de culture à la souris : preuve que PKCη alimente la dissémination
Pour tester la relation de cause à effet, les chercheurs ont utilisé l’édition génomique CRISPR pour supprimer PKCη dans deux lignées cellulaires TNBC hautement métastatiques, une murine (4T1) et une humaine (MDA‑MB‑231). En l’absence de PKCη, les cellules ont basculé vers un état plus « épithélial » : elles ont augmenté les protéines d’adhésion telles que l’E‑cadherine et EpCAM, et réduit les marqueurs mésenchymateux classiques comme la vimentine et la N‑cadherine. Ces cellules déficientes en PKCη formaient moins et plus petites colonies, migraient et envahissaient moins efficacement, étaient plus sensibles à la mort cellulaire en condition de détachement, et montraient une chute nette des caractéristiques de cellules souches cancéreuses, incluant moins de cellules CD44high/CD24low et ALDH‑positives ainsi qu’une capacité réduite à former des sphères. Injectées chez la souris, les cellules dépourvues de PKCη produisaient des tumeurs primaires plus petites et beaucoup moins de métastases aux poumons, au foie, au cerveau et dans d’autres organes ; les souris présentaient aussi une survie prolongée. La restauration de PKCη inversait ces effets, confirmant que l’enzyme favorise activement la progression et la dissémination du TNBC.
Comment PKCη détourne une voie de contrôle de la croissance
L’étude s’est ensuite penchée sur les mécanismes par lesquels PKCη exerce ce pouvoir pro‑métastatique. Les données patients ont révélé que les niveaux de PKCη évoluent en parallèle de YAP, une protéine régulatrice puissante contrôlée par la voie Hippo — un « frein » cellulaire qui limite normalement la croissance. Des niveaux élevés de PRKCH ou de YAP1 prédisaient de moins bons résultats pour les patientes, et des niveaux élevés des deux ensemble étaient associés à une survie sans métastases à distance particulièrement mauvaise. Dans les cellules TNBC, la suppression de PKCη réduisait les niveaux totaux de YAP et le faisait passer du noyau au cytoplasme, où il est inactif. Des expériences biochimiques ont montré que PKCη se lie physiquement à YAP et lui ajoute spécifiquement un groupe phosphate au site Ser128. Cette modification stabilise YAP et favorise son entrée dans le noyau pour activer des gènes qui pilotent l’EMT, le caractère stem‑like et les métastases. En l’absence de PKCη, YAP est phosphorylé à d’autres sites (Ser127 et Ser397) qui le font se lier aux protéines 14‑3‑3, le piègent dans le cytoplasme puis entraînent sa dégradation. PKCη augmente aussi PTEN — un frein naturel sur l’enzyme AKT — maintenant ainsi l’activité d’AKT faible et réprimant les kinases Hippo en amont qui, autrement, inactivent YAP. De cette façon, PKCη active YAP directement et empêche indirectement la remise en route du frein Hippo. 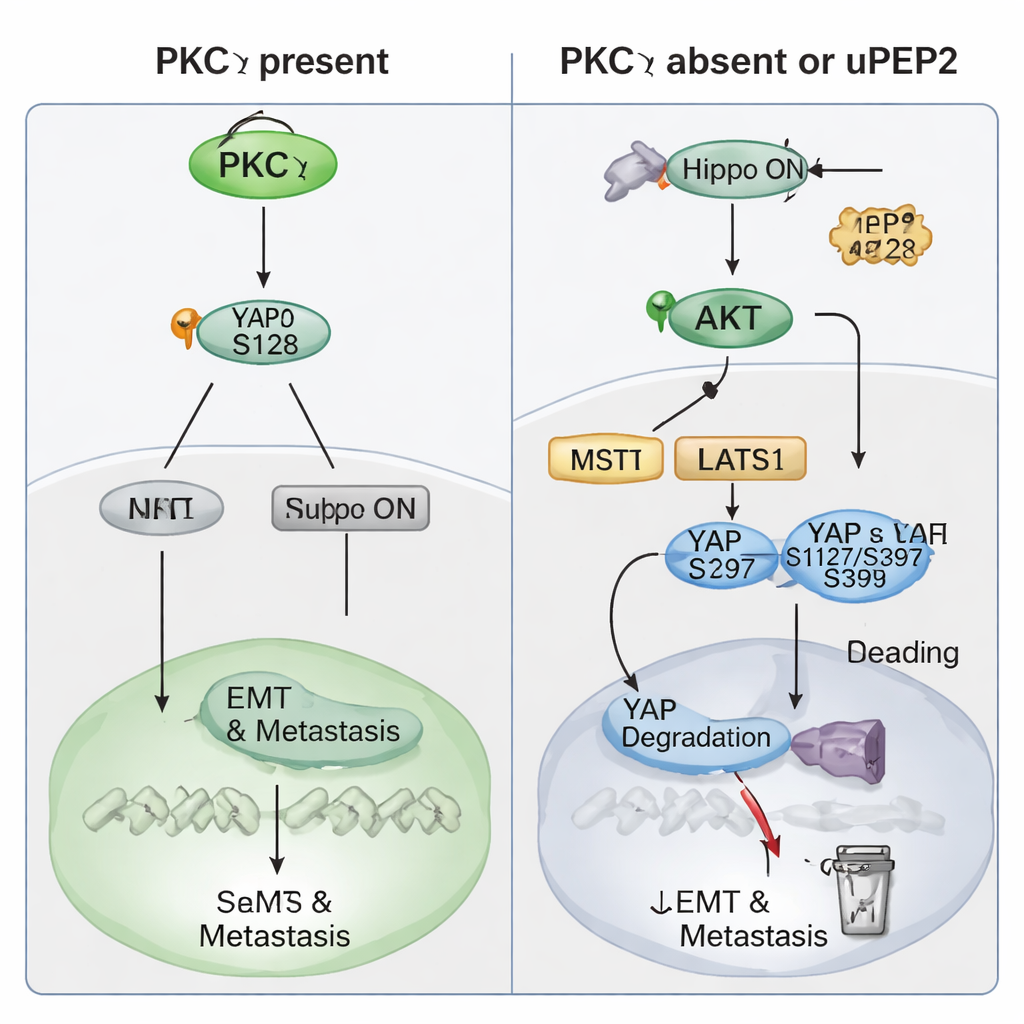
Un petit peptide qui désarme l’interrupteur cancéreux
De manière intrigante, le gène PKCη contient un court cadre de lecture en amont (uORF) qui code pour un micropeptide appelé uPEP2. Des travaux antérieurs ont montré que uPEP2 peut se lier et inhiber PKCη et des enzymes apparentées. Ici, le traitement des cellules TNBC avec uPEP2 synthétique imite les effets de la suppression de PKCη : la migration, l’invasion et les comportements de type souches ont tous diminué, les marqueurs EMT ont évolué vers un profil moins agressif, et les niveaux de YAP ont chuté tandis que ses marques de phosphorylation « off » augmentaient. Dans des tumeurs murines, uPEP2 réduisait PKCη et YAP dans les tumeurs primaires, augmentait l’inactivation de YAP et était associé à moins de micrométastases au foie et aux poumons. Mécaniquement, uPEP2 favorise la dégradation de PKCη, réactive la voie Hippo et pousse YAP vers la rétention cytoplasmique puis la dégradation.
Ce que cela signifie pour les traitements futurs
Pour le lecteur non spécialiste, le message clé est que les chercheurs ont identifié PKCη comme une pièce maîtresse qui aide les cancers du sein les plus agressifs à se détacher, migrer et coloniser des organes distants en désactivant un système naturel de contrôle de la croissance et en activant la « pédale d’accélérateur » YAP. En supprimant PKCη ou en utilisant le petit peptide naturel uPEP2 pour le dégrader, ils ont pu restaurer le frein Hippo, calmer YAP et réduire fortement les métastases dans des modèles précliniques. Bien que ce travail soit encore au stade expérimental et ait été réalisé sur des lignées cellulaires et des souris immunodéficientes, il met en lumière PKCη et son interaction avec YAP comme des cibles prometteuses pour de nouvelles thérapies du TNBC, et suggère que des médicaments de type uPEP2 pourraient un jour aider à prévenir ou limiter la propagation de ce cancer difficile à traiter.
Citation: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Mots-clés: cancer du sein triple négatif, PKC-eta, voie Hippo-YAP, transition épithélio‑mésenchymateuse, métastase cancéreuse