Clear Sky Science · fr
Arthrose : pathogenèse moléculaire et options thérapeutiques potentielles
Quand la douleur articulaire quotidienne devient une histoire touchant tout le corps
Des genoux endoloris ou des doigts raides sont souvent considérés comme une conséquence inévitable du vieillissement. Pourtant l’arthrose — la maladie articulaire la plus fréquente dans le monde — n’est pas seulement un « effet d’usure ». Cet article de synthèse lève le voile sur ce qui se passe réellement dans les articulations douloureuses, des nerfs de la douleur qui dysfonctionnent aux machines cellulaires surmenées, et explore une nouvelle génération de traitements qui vont bien au‑delà des simples analgésiques.
Une maladie fréquente aux coûts personnels lourds
L’arthrose touche près de 8 % de la population mondiale, des centaines de millions de personnes vivant avec une douleur chronique et une mobilité réduite. La maladie survient plus souvent chez les femmes, chez les personnes de plus de 55 ans, et chez celles en surpoids ou dont le travail ou le sport impose des contraintes répétées et importantes sur les articulations. Les soins standard actuels — exercice, perte de poids, orthèses, anti‑inflammatoires, infiltrations articulaires et, dans les cas sévères, prothèse articulaire — peuvent soulager les symptômes mais rarissimement arrêtent l’aggravation progressive de la maladie. Cet écart entre les besoins et les traitements disponibles a poussé les chercheurs à approfondir la façon dont l’arthrose débute et pourquoi elle fait si mal.
Pourquoi l’articulation fait mal : fils, substances chimiques et signaux
La douleur liée à l’arthrose ne s’explique pas par les radiographies seules : certaines personnes affichant des lésions modestes ressentent une grande douleur, tandis que d’autres avec des changements importants rapportent peu de douleur. L’article retrace le parcours de la douleur depuis l’articulation du genou jusqu’à la moelle épinière et le cerveau. Les terminaisons nerveuses de l’articulation — en particulier les fibres fines Aδ et C — baignent dans un mélange de médiateurs inflammatoires, dont des interleukines et le facteur de nécrose tumorale, ainsi que le facteur de croissance nerveuse. Ces substances activent des canaux spécifiques des terminaisons nerveuses qui laissent passer le sodium et le calcium, rendant les nerfs plus facilement excitable et plus souvent déclenchés. Avec le temps, les voies de la douleur dans la moelle épinière et le cerveau peuvent devenir hyper‑réactives, si bien qu’un mouvement normal ou un léger froid donne une sensation aiguë et brûlante.
La charge de travail cachée à l’intérieur des cellules articulaires
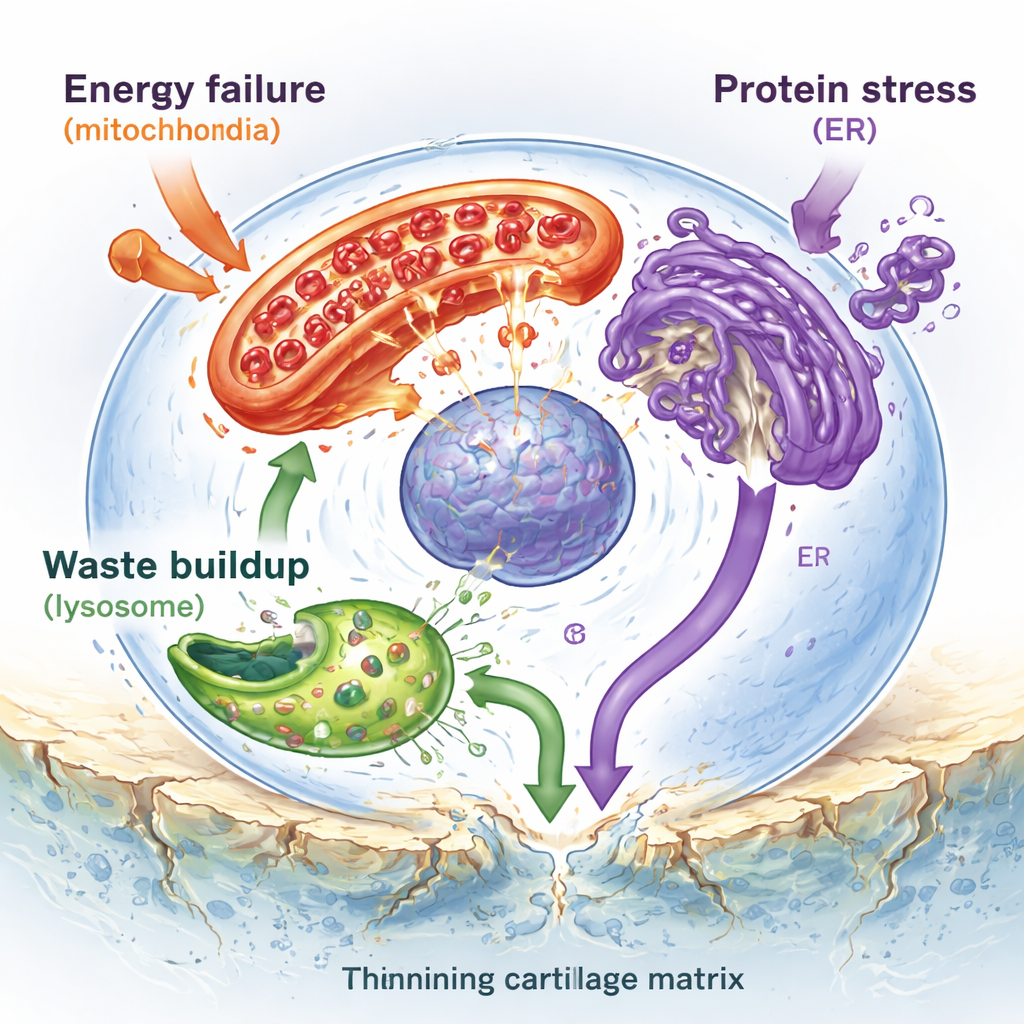
Au cœur du cartilage, les seules cellules résidentes — les chondrocytes — tentent de maintenir une matrice lisse et élastique qui permet aux os de glisser. Les auteurs montrent que ces cellules sont assiégées sur plusieurs fronts. Les mitochondries, les petites centrales énergétiques de la cellule, sont endommagées et moins efficaces, produisant trop peu d’énergie et trop de molécules réactives à l’oxygène qui abîment l’ADN et les protéines. Les lysosomes, centres de recyclage cellulaire, sont surchargés par des cristaux minéraux durs, fragilisant leurs membranes de sorte que des enzymes destructrices fuient dans la cellule et déclenchent la mort cellulaire. Le réticulum endoplasmique, un labyrinthe membranaire où se plient les nouvelles protéines, s’encombre de molécules mal repliées, déclenchant une « réponse au stress » chronique qui finit par pousser les cellules vers l’autodestruction. Ensemble, ces organites stressés alimentent l’inflammation et accélèrent la perte et la calcification du cartilage.
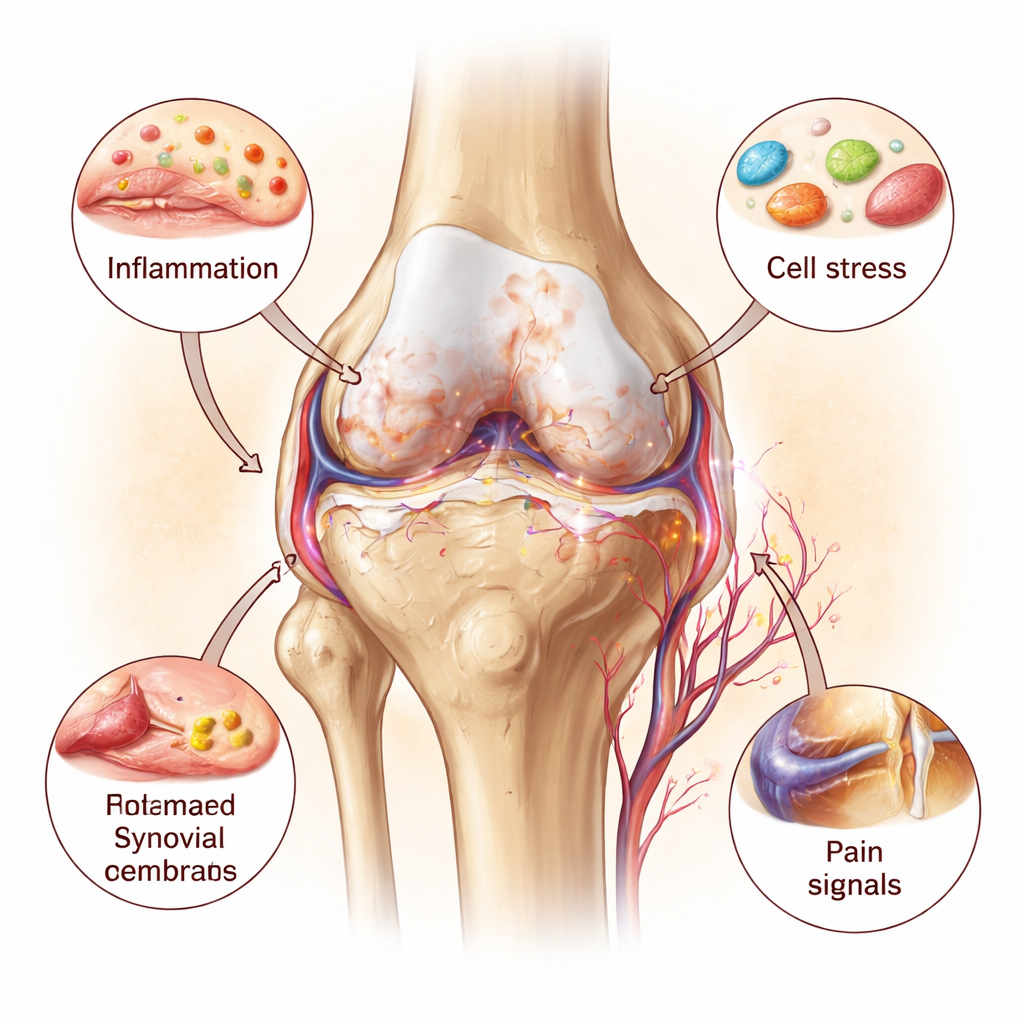
Inflammation : du carburant sur le feu
Les messagers inflammatoires sont les haut‑parleurs de ce processus. Trois en particulier — l’interleukine‑1, l’interleukine‑6 et le facteur de nécrose tumorale‑alpha — forment un cercle vicieux avec les lésions d’organites. Ils poussent les chondrocytes à produire des enzymes qui dégradent le cartilage et favorisent une croissance osseuse anormale sous la surface articulaire. En parallèle, les mitochondries blessées et les lysosomes poreux libèrent leurs propres signaux de détresse, qui activent davantage les senseurs immunitaires à l’intérieur de l’articulation. Vaisseaux sanguins et fibres nerveuses envahissent des zones de cartilage normalement silencieuses et sans nerfs, augmentant la sensibilité à la douleur. Cette vue globale de l’articulation présente l’arthrose comme une maladie inflammatoire lente mais auto‑entretenue, et non comme une simple usure mécanique passive du cartilage.
Nouvelles idées thérapeutiques : des canaux ioniques aux centrales cellulaires
Armés de cette cartographie mécanistique, les chercheurs testent de nouveaux médicaments et systèmes d’administration. Du côté de la douleur, des médicaments expérimentaux bloquent ou désensibilisent doucement des canaux nerveux tels que TRPV1 (le récepteur de la capsaïcine), TRPA1, TRPM3/8, et des canaux sodiques spécifiques (Nav1.7 et Nav1.8), ou neutralisent le facteur de croissance nerveuse pour empêcher l’hypersensibilité des nerfs. Du côté des traitements modifiant la maladie, des anticorps ciblés visent à réduire des cytokines inflammatoires clés, tandis que de petites molécules et des agents « sénolytiques » cherchent à restaurer un comportement cellulaire plus sain. Un domaine particulièrement prometteur est la thérapie dirigée vers les organites : des composés qui stimulent le nettoyage mitochondrial (mitophagie), stabilisent l’acidité et les membranes lysosomales, ou soulagent le stress du réticulum endoplasmique. Des nanoparticules sophistiquées, des liposomes et des exosomes conçus sont en cours de développement pour cibler les cellules du cartilage et même des organites spécifiques, délivrant les médicaments précisément là où ils sont nécessaires.
Ce que cela signifie pour les personnes vivant avec l’arthrose
L’article conclut que l’arthrose doit être envisagée et traitée comme un désordre biologique complexe impliquant un métabolisme cellulaire perturbé, une inflammation chronique de bas grade et un câblage douloureux inadapté. Bien que nombre des médicaments et systèmes d’administration proposés en soient encore aux premiers tests en laboratoire ou chez l’animal, ils dessinent un avenir où le traitement sera à la fois multimodal et personnalisé : atténuer la douleur en calmant des nerfs hyperactifs, tout en protégeant ou en rajeunissant les cellules de l’articulation et leurs machines internes. Pour les patients, cela pourrait signifier à terme des thérapies qui non seulement rendent le mouvement moins douloureux, mais ralentissent ou possiblement inversent les dommages structurels que l’on considère aujourd’hui souvent comme inévitables.
Citation: Zhang, Y., Han, Y., Sun, Y. et al. Osteoarthritis: molecular pathogenesis and potential therapeutic options. Sig Transduct Target Ther 11, 81 (2026). https://doi.org/10.1038/s41392-025-02556-6
Mots-clés: arthrose, douleur articulaire, cartilage, inflammation, mitochondries