Clear Sky Science · fr
Découverte et développement d'antiviraux : défis et orientations futures
Pourquoi nous avons toujours besoin de meilleurs médicaments antiviraux
La pandémie de COVID-19 a montré à quelle vitesse un nouveau virus peut bouleverser la vie quotidienne — et combien nous dépendons encore de bons médicaments lorsque les vaccins ne suffisent pas. Cet article de synthèse revient sur plus de 60 ans de développement d'antiviraux et se demande : comment construire des défenses plus rapides, plus intelligentes et plus larges contre les menaces virales à venir ? Il explique, en termes accessibles, comment les chercheurs découvrent, conçoivent et administrent des antiviraux, ce qu'ils ont appris du COVID-19 et comment des outils comme l'intelligence artificielle et la nanotechnologie pourraient changer la donne.
Des premiers antiviraux à l'arsenal d'aujourd'hui
La médecine antivirale est un domaine relativement jeune. Le premier médicament approuvé, l'idoxuridine dans les années 1960, a montré qu'altérer les éléments constitutifs de l'ADN pouvait ralentir la réplication virale, mais il endommageait aussi les cellules saines et ne pouvait être utilisé que pour l'œil. Plus tard est arrivé l'acyclovir, médicament phare contre l'herpès, activé principalement à l'intérieur des cellules infectées, le rendant à la fois puissant et sûr. Dans les années 1980, le zidovudine est devenu le premier traitement contre le VIH, ouvrant la voie aux thérapies combinées modernes qui transforment aujourd'hui le VIH en une affection chronique gérable. Au fil des décennies, une meilleure chimie et la conception assistée par ordinateur ont permis d'introduire des médicaments plus précis contre la grippe, les hépatites B et C, le VIH et, plus récemment, le SARS‑CoV‑2. La revue retrace cette chronologie et montre comment chaque avancée a introduit une nouvelle manière de déjouer les virus.
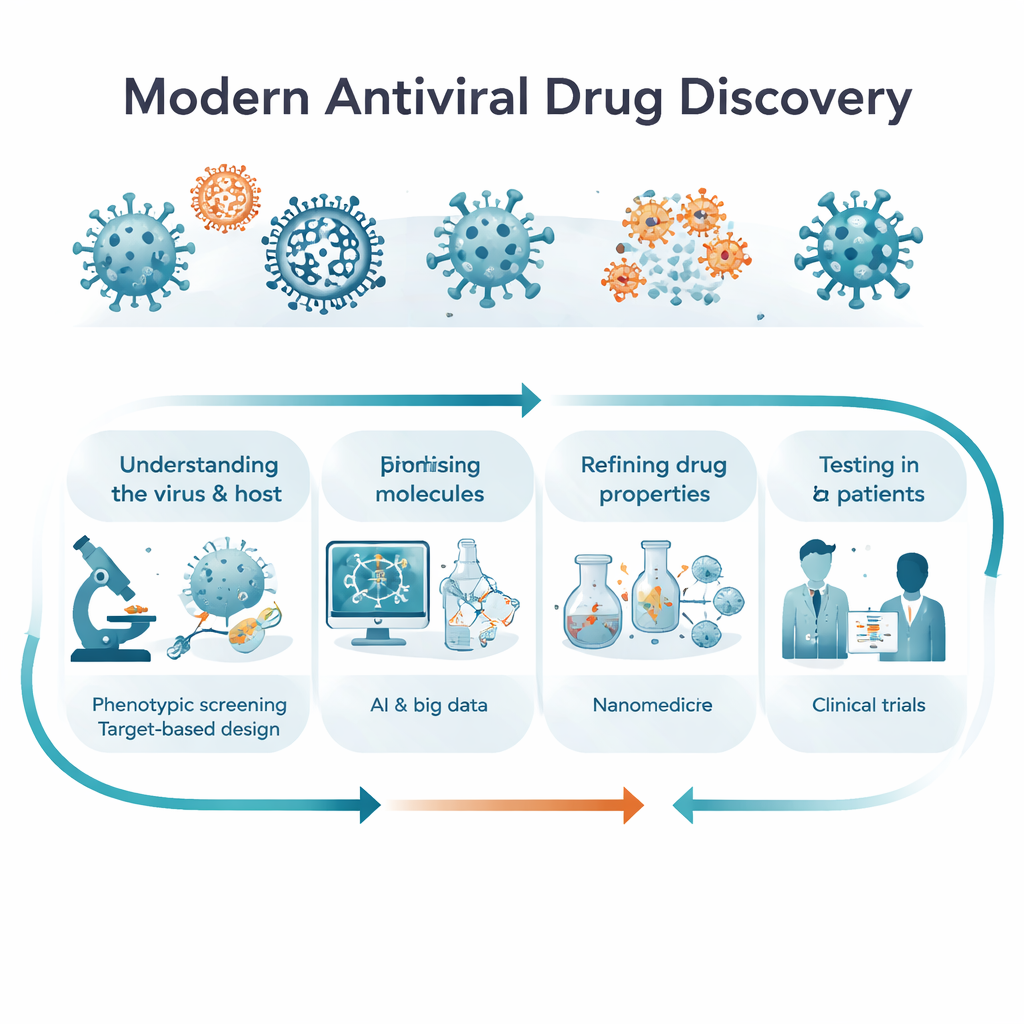
Deux manières de trouver un bon médicament : observer les cellules ou viser des cibles
Les chercheurs suivent généralement deux voies complémentaires pour découvrir de nouveaux antiviraux. Dans la découverte « phénotypique », ils ne partent pas d'une protéine spécifique ; au lieu de cela, ils exposent des cellules infectées ou des organismes modèles à des milliers de molécules et se demandent simplement : lesquelles contrôlent le virus et maintiennent les cellules en vie ? Cela peut révéler des médicaments surprenants, de première classe, y compris des composés agissant sur plusieurs voies. Dans la découverte « fondée sur une cible », les scientifiques identifient d'abord une protéine virale ou humaine cruciale pour l'infection — comme une polymerase, une protéase ou un signal immunitaire — puis conçoivent des molécules pour bloquer ou moduler cette cible. L'article explique en quoi ces stratégies diffèrent, pourquoi chacune est importante à différents stades de la recherche, et comment les projets futurs sont susceptibles de les combiner, passant aisément de l'observation large à la compréhension moléculaire précise.
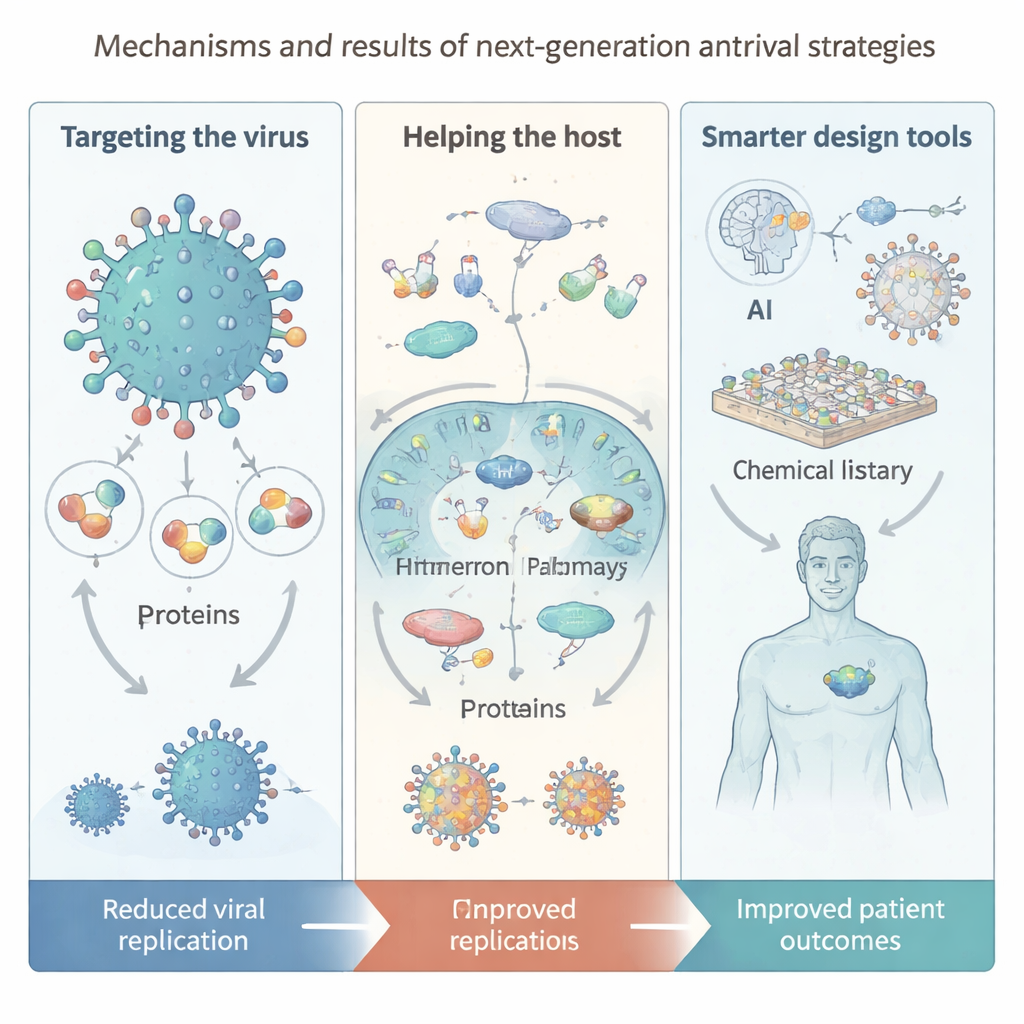
Frapper le virus — et son système d'appui — là où ça fait mal
Les antiviraux modernes font bien plus que simplement encombrer une enzyme virale unique. La revue décrit le cycle de vie viral, de l'entrée dans la cellule à la copie du génome et à la libération, et met en lumière les types de médicaments qui interfèrent à chaque étape. Certains composés se lient directement aux enzymes ou protéines structurelles virales. D'autres agissent en ciblant des facteurs hôtes dont les virus dépendent — tels que des récepteurs à la surface cellulaire, des enzymes métaboliques clés ou des voies de l'immunité innée comme les interférons et les récepteurs de type toll. En agissant sur ces protéines « auxiliaires » de l'hôte, ces médicaments peuvent réduire la probabilité qu'un virus à mutation rapide échappe au traitement. Les auteurs décrivent aussi des idées émergentes, comme de petites molécules qui perturbent des « gouttelettes » membraneless à l'intérieur des cellules où les virus s'assemblent, ou qui dégradent sélectivement protéines et ARN viraux au lieu de simplement les bloquer.
Concevoir de meilleures molécules : forme, propriétés et distribution
Transformer un « hit » initial en médicament utile implique plus que maximiser la puissance. Les chimistes ajustent la forme et la charge des molécules pour qu'elles s'ajustent à leurs cibles comme des clés dans des serrures, souvent guidés par des structures protéiques haute résolution et des simulations. Ils modifient aussi la solubilité dans l'eau, la stabilité et le métabolisme pour s'assurer que le médicament atteigne le bon tissu, reste actif suffisamment longtemps et évite une toxicité excessive. L'article donne des exemples de la façon dont de petits changements — comme l'ajout d'une chaîne latérale ou la formation d'un sel — peuvent renforcer l'activité contre des souches résistantes du VIH ou des coronavirus tout en améliorant la sécurité. Il explique également les promédicaments, formes inactives ou moins actives conçues pour être converties dans l'organisme, et les systèmes de délivrance ciblée tels que les étiquettes sucrées ciblant le foie et les nanoparticules lipidiques qui transportent en sécurité des ARNm ou des médicaments d'acide nucléique fragiles à l'intérieur des cellules.
Nouveaux outils : intelligence artificielle, bibliothèques gigantesques et nanotechnologie
Un thème majeur de la revue est la manière dont la technologie reshape la découverte antivirale. L'intelligence artificielle aide désormais à prédire les structures protéiques, à explorer d'immenses bibliothèques « virtuelles » contenant des milliards de molécules possibles, et à proposer de nouveaux composés ou combinaisons médicamenteuses. Les bibliothèques codées par ADN et les plateformes de peptides macrocycliques permettent un criblage ultra-rapide d'espaces chimiques énormes, tandis que des systèmes automatisés de synthèse et de purification accélèrent la boucle construire‑tester. Côté délivrance, la nanotechnologie fournit des particules semblables à des virus, des polymères intelligents et des « nanozymes » capables d'endommager directement les enveloppes virales ou de renforcer les réponses immunitaires. Pourtant, les auteurs mettent en garde : les modèles d'IA dépendent toujours de données de haute qualité, de nombreuses molécules générées sont difficiles à synthétiser ou à tester, et des enjeux de sécurité, d'équité et de vie privée doivent être traités à mesure que ces outils deviennent centraux.
Vers où se dirige la découverte d'antiviraux
Pour le lecteur non spécialiste, le message clé de l'article est à la fois sobre et porteur d'espoir. Les virus mutent rapidement, et aucune pilule unique ne fonctionnera pour toujours ni contre toutes les menaces. Mais en tirant les leçons du COVID‑19, en approfondissant notre compréhension des interactions virus‑hôte et en combinant chimie intelligente, biologie avancée, IA et nanotechnologie, les scientifiques construisent une boîte à outils antivirale plus agile. Les traitements futurs seront probablement plus larges, mieux tolérés et conçus pour viser non seulement le virus, mais aussi les « points faibles » vulnérables du processus d'infection. Une collaboration continue entre disciplines, industries et pays sera essentielle pour transformer ces avancées scientifiques en médicaments abordables et pratiques avant l'arrivée de la prochaine pandémie.
Citation: Du, S., Hu, X., Li, P. et al. Antiviral drug discovery and development: challenges and future directions. Sig Transduct Target Ther 11, 69 (2026). https://doi.org/10.1038/s41392-025-02539-7
Mots-clés: découverte de médicaments antiviraux, thérapeutiques COVID-19, antiviraux ciblant l'hôte, intelligence artificielle en conception de médicaments, nanotechnologie en médecine