Clear Sky Science · fr
Micronoyaux : origines, tests, mécanismes, maladies et traitements
Bulles cachées à l’intérieur de nos cellules
Au cœur de nos cellules, de petites bulles d’ADN « satellites » appelées micronoyaux se révèlent bien plus que de simples curiosités au microscope. Autrefois considérées comme des résidus inoffensifs de la division cellulaire, ces petites sphères remplies d’ADN sont aujourd’hui associées au développement du cancer, à des réactions immunitaires et même à de potentielles nouvelles thérapies. Comprendre ce qui crée les micronoyaux, ce qui leur arrive et comment ils affectent notre matériel génétique redessine la manière dont les scientifiques envisagent les dommages du génome et les maladies.
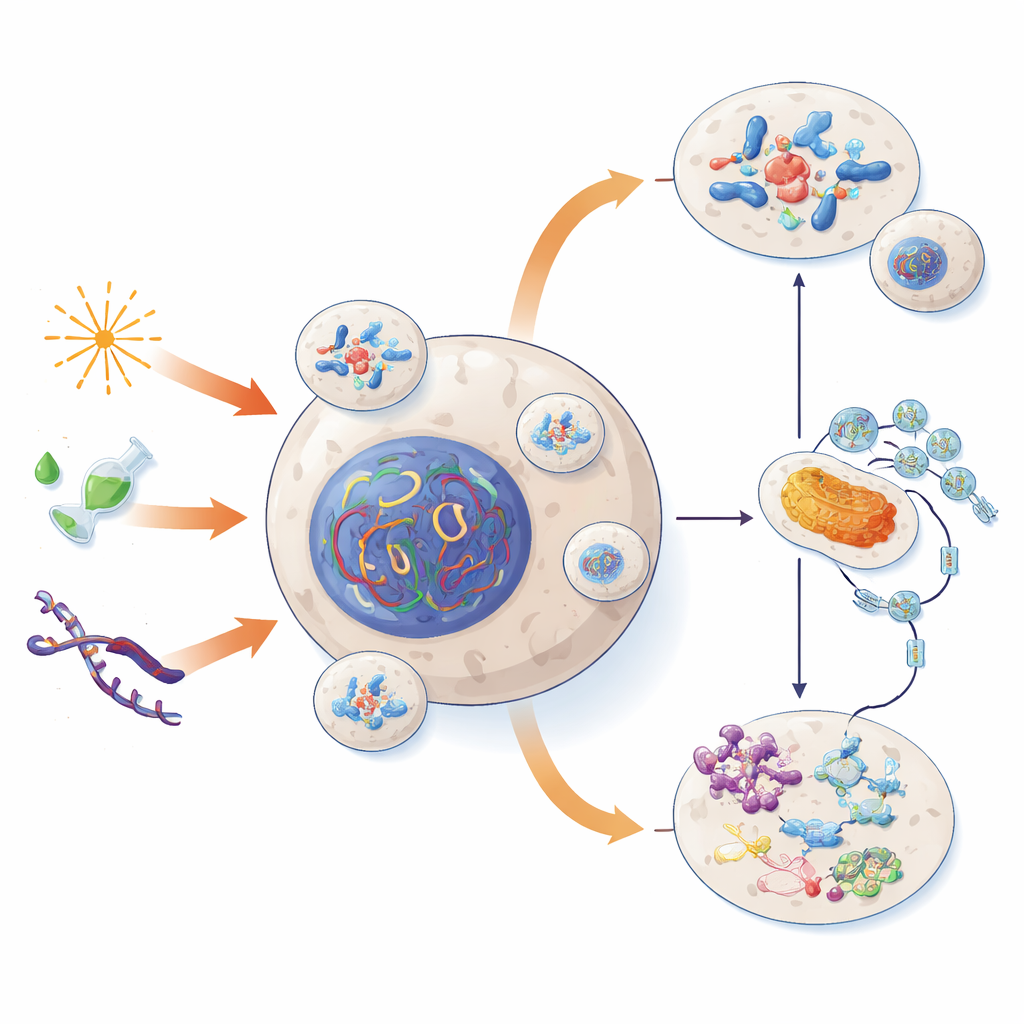
Comment naissent ces petites bulles d’ADN
Les micronoyaux apparaissent généralement lorsqu’un problème survient pendant la division cellulaire. Normalement, les chromosomes s’alignent puis sont tirés de façon égale dans les deux nouvelles cellules. Mais si la machinerie de division est défaillante ou si l’ADN est endommagé, un chromosome entier ou un fragment peut rester en retard et se sceller dans une coque séparée à l’extérieur du noyau principal. Des blessures causées par des radiations ou des produits chimiques toxiques, des extrémités chromosomiques usées (télomères) ou des erreurs dans les « crochets » protéiques qui séparent les chromosomes peuvent tous provoquer ce mauvais tri. Dans certains cas, le noyau bourgeonne même des fragments d’ADN pendant les phases calmes entre deux divisions, formant des micronoyaux sans qu’il y ait une division complète de la cellule.
Quel destin pour ces îlots d’ADN égarés
Une fois formés, les micronoyaux peuvent suivre plusieurs trajectoires, chacune ayant des conséquences différentes pour la cellule. Certains sont réabsorbés dans le noyau principal lors de divisions ultérieures, réintégrant discrètement leur ADN — parfois avec des modifications subtiles et durables de l’activité génique. D’autres persistent comme corps séparés et ne sont transmis qu’à une seule des deux cellules filles, augmentant la diversité génétique dans un tissu. Certains micronoyaux sont digérés par des mécanismes d’« auto-nettoyage » cellulaires, tandis que d’autres sont expulsés physiquement de la cellule. Mais le destin le plus spectaculaire est peut-être la rupture : leur enveloppe fragile se rompt souvent, déversant de l’ADN endommagé dans le cytoplasme et l’exposant à des forces destructrices.
De chromosomes brisés au chaos
Lorsque qu’un micronoyau se rompt ou que son ADN est copié de façon incorrecte, le chromosome piégé peut être pulvérisé en plusieurs dizaines ou centaines de fragments. Ces fragments sont ensuite recollés à la hâte et de manière sujette à erreur, un phénomène connu sous le nom de chromothripsis. Au lieu d’une accumulation lente de petites mutations sur des années, une cellule peut subir un bouleversement génétique massif et localisé en une seule crise. Des gènes importants peuvent être perdus, mélangés ou copiés en grand nombre. Des fragments d’ADN circulaires supplémentaires peuvent se former et transporter plusieurs gènes favorisant la croissance, conférant à la cellule de puissants avantages. Que ce changement aide ou nuise à la cellule dépend des gènes affectés, mais dans de nombreux cancers, ces événements favorisent la croissance tumorale, la dissémination ou la résistance aux traitements.
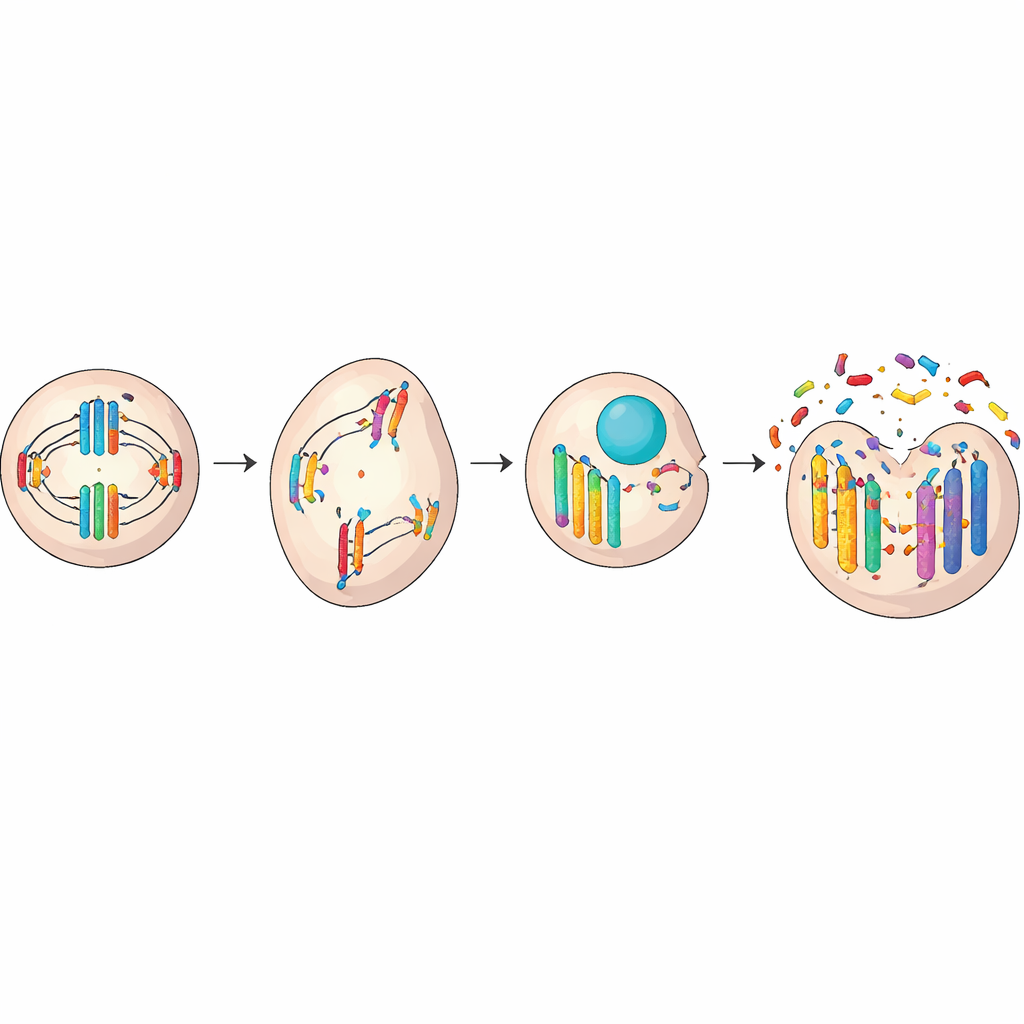
Signaux qui réveillent le système immunitaire
L’ADN libéré par la rupture des micronoyaux joue aussi le rôle de signal d’alarme. Nos cellules conservent normalement leur ADN à l’intérieur du noyau, si bien que de l’ADN libre dans le cytoplasme ressemble à celui d’un virus ou d’une bactérie. Une protéine détectrice appelée cGAS peut se lier à cet ADN errant et activer un partenaire nommé STING, déclenchant des réponses inflammatoires et antivirales. Dans des situations saines, cela aide à éliminer les cellules endommagées ou dangereuses. Mais dans de nombreux cancers avancés, les cellules tumorales trouvent des moyens d’atténuer ou de reconfigurer ce système d’alarme. Au lieu de provoquer une attaque immunitaire, des signaux chroniques de faible intensité issus de micronoyaux fréquents peuvent aider les cellules cancéreuses à devenir plus invasives et à mieux échapper aux défenses de l’organisme.
Mesurer et exploiter les micronoyaux
Parce que les micronoyaux marquent visiblement les dommages de l’ADN, ils sont devenus des outils utiles en médecine et en santé publique. Des tests de coloration simples sur des cellules sanguines, des cellules de la muqueuse buccale ou des globules rouges peuvent révéler l’ampleur du stress génétique subi par une personne à cause de la pollution, d’expositions professionnelles, du tabagisme ou de maladies. Les personnes atteintes de certains cancers, d’insuffisance cardiaque, de maladies rénales ou de troubles héréditaires de réparation de l’ADN présentent souvent un nombre accru de micronoyaux. Les chercheurs utilisent désormais des méthodes d’imagerie et de tri à haut débit pour purifier les micronoyaux, inventorier leurs contenus protéiques et d’ADN, et cartographier comment différents types de stress laissent en eux des empreintes épigénétiques et structurelles distinctes.
Nouveaux risques et nouvelles opportunités
Les micronoyaux se trouvent à la croisée des chemins entre dommage et défense : ils peuvent à la fois provoquer un remaniement dangereux du génome et activer la protection immunitaire. Certaines thérapies expérimentales contre le cancer augmentent délibérément les erreurs de ségrégation chromosomique ou bloquent des voies spécifiques de réparation de l’ADN pour forcer les cellules tumorales à former des micronoyaux, dans l’espoir de déclencher de fortes réactions immunitaires ou de pousser des cellules instables au-delà de leurs limites. Pourtant, cette stratégie est délicate, car les mêmes processus peuvent aussi générer des clones plus agressifs et résistants aux traitements. Les auteurs concluent que les micronoyaux ne sont ni purement nuisibles ni purement bénéfiques. Ce sont plutôt des indicateurs et des agents de changement puissants dont l’impact global dépend du contexte. Pour transformer les micronoyaux en alliés sûrs contre la maladie, les scientifiques devront développer de meilleures méthodes pour mesurer, contrôler et orienter sélectivement leur formation et leur devenir dans l’organisme.
Citation: Duan, H., Peng, X., Qin, S. et al. Micronuclei: origins, assays, mechanisms, diseases and treatments. Sig Transduct Target Ther 11, 114 (2026). https://doi.org/10.1038/s41392-025-02538-8
Mots-clés: micronoyaux, instabilité du génome, chromothripsis, cGAS-STING, biomarqueurs du cancer