Clear Sky Science · fr
Cellules T CD4 cytotoxiques : origine, fonctions biologiques, maladies et cibles thérapeutiques
Quand les cellules auxiliaires deviennent des tueuses
Le système immunitaire est le plus souvent décrit en rôles simples : certaines cellules repèrent les problèmes, d’autres mènent le combat. Cet article se concentre sur un groupe surprenant qui brouille cette ligne — les cellules T CD4 cytotoxiques. Longtemps connues principalement comme des cellules « aides » qui coordonnent les défenses, certaines cellules CD4 peuvent elles-mêmes se transformer en effectrices armées. Comprendre comment ces cellules métamorphosées apparaissent, ce qu’elles font et comment elles contribuent à des maladies telles que le cancer, les infections virales, les troubles auto-immuns et les maladies cardiaques pourrait ouvrir de nouvelles voies pour renforcer l’immunité ou calmer l’inflammation nuisible. 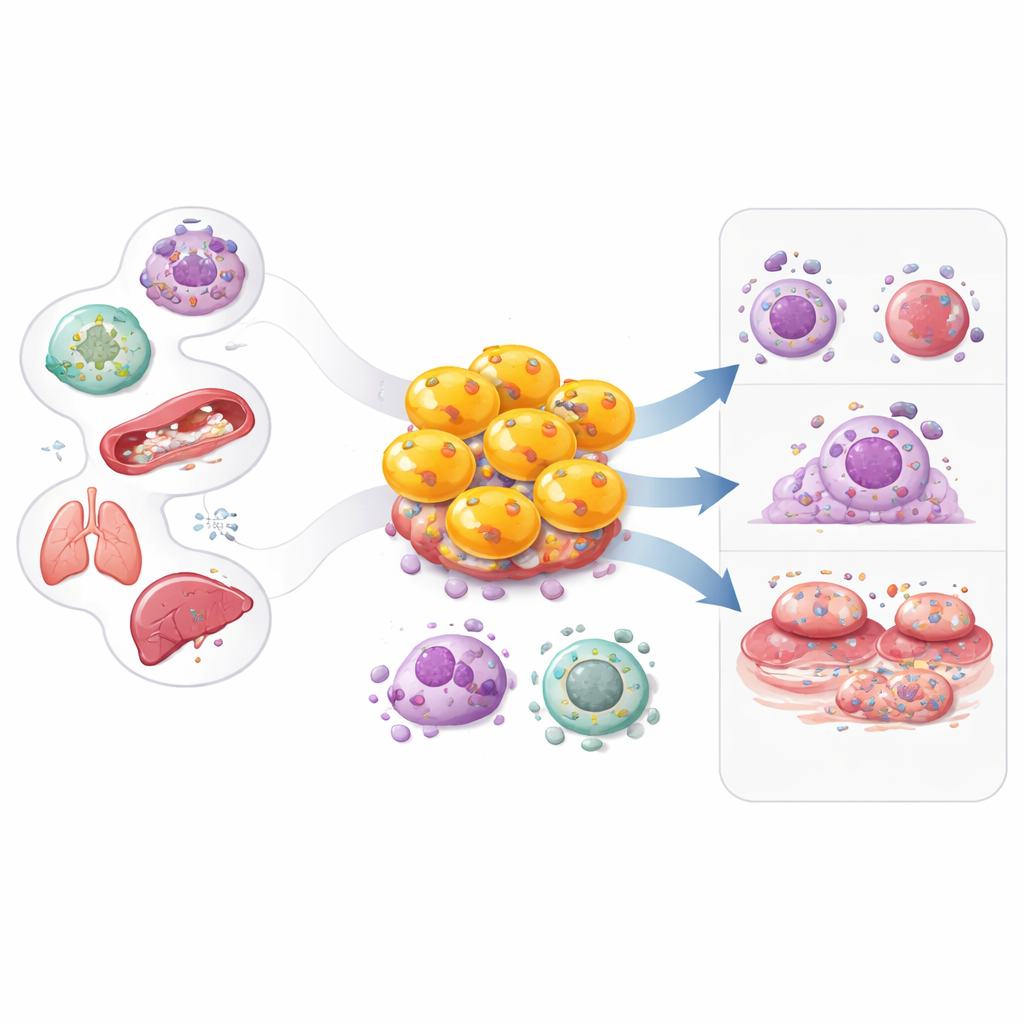
Comment est né ce défenseur flexible
Les premières études, à la fin des années 1970 et dans les années 1980, ont montré qu’une fraction des cellules T CD4 pouvait tuer directement d’autres cellules présentant les bons signaux immunitaires, un comportement proche de celui des cellules T CD8 « tueuses » classiques. Au départ, beaucoup de chercheurs ont mis ces observations sur le compte d’artéfacts de culture. Au fil des décennies, des modèles animaux de grippe et des études chez des personnes atteintes de polyarthrite rhumatoïde, de maladies cardiaques, d’infections virales chroniques et de cancer ont confirmé que les cellules T CD4 cytotoxiques existent et ont une importance clinique. Les outils modernes, comme la cytométrie en flux et le séquençage ARN unicellulaire, ont depuis cartographié leur diversité, révélant que ces cellules s’étendent dans les infections chroniques, les tumeurs, le vieillissement et plusieurs maladies inflammatoires, où elles peuvent persister longtemps.
D’où viennent ces aides tueuses
La revue explique que les cellules T CD4 cytotoxiques émergent probablement par deux voies principales. Une hypothèse est qu’elles ressemblent en partie aux cellules NK (natural killer) car elles partagent de nombreux récepteurs de surface et molécules cytotoxiques, ce qui suggère une voie de développement apparentée. Cependant, des preuves croissantes privilégient une autre interprétation : la plupart de ces cellules commencent comme des CD4 auxiliaires ordinaires — en particulier des cellules de type Th1 — qui, sous une exposition antigénique chronique et des signaux inflammatoires forts, se « reprogramment » en un état différencié terminal et cytotoxique. Ce basculement est contrôlé par un réseau d’indices externes (comme les interleukines 2, 7 et 15) et de commutateurs internes (notamment Runx3, T-bet, Eomes, Blimp-1 et Hobit) qui activent ensemble les gènes codant pour la perforine, les granzymes et les ligands inducteurs de mort.
Comment elles tuent et modulent l’inflammation
Sur le plan fonctionnel, les cellules T CD4 cytotoxiques agissent par deux principales voies d’attaque. Par la voie des granules, elles forment un contact étroit avec une cellule cible et libèrent des paquets contenant la perforine et les granzymes, qui perforent la membrane et déclenchent la mort cellulaire programmée de l’intérieur. Par la voie des ligands de mort, elles exposent à leur surface des molécules telles que le ligand Fas et TRAIL, qui engagent les récepteurs correspondants sur les cellules cibles pour lancer un programme suicidaire intracellulaire. Au-delà du meurtre direct, ces cellules sécrètent des messagers inflammatoires comme l’interféron-gamma, le facteur de nécrose tumorale et des facteurs de croissance qui recrutent et activent d’autres cellules immunitaires, remodelent les vaisseaux sanguins et modifient le comportement tissulaire local. Contrairement aux auxiliaires classiques, elles résistent souvent aux « freins » habituels, tels que les cellules T régulatrices, et sont moins sujettes à l’apoptose, ce qui leur permet de s’accumuler dans les maladies chroniques. 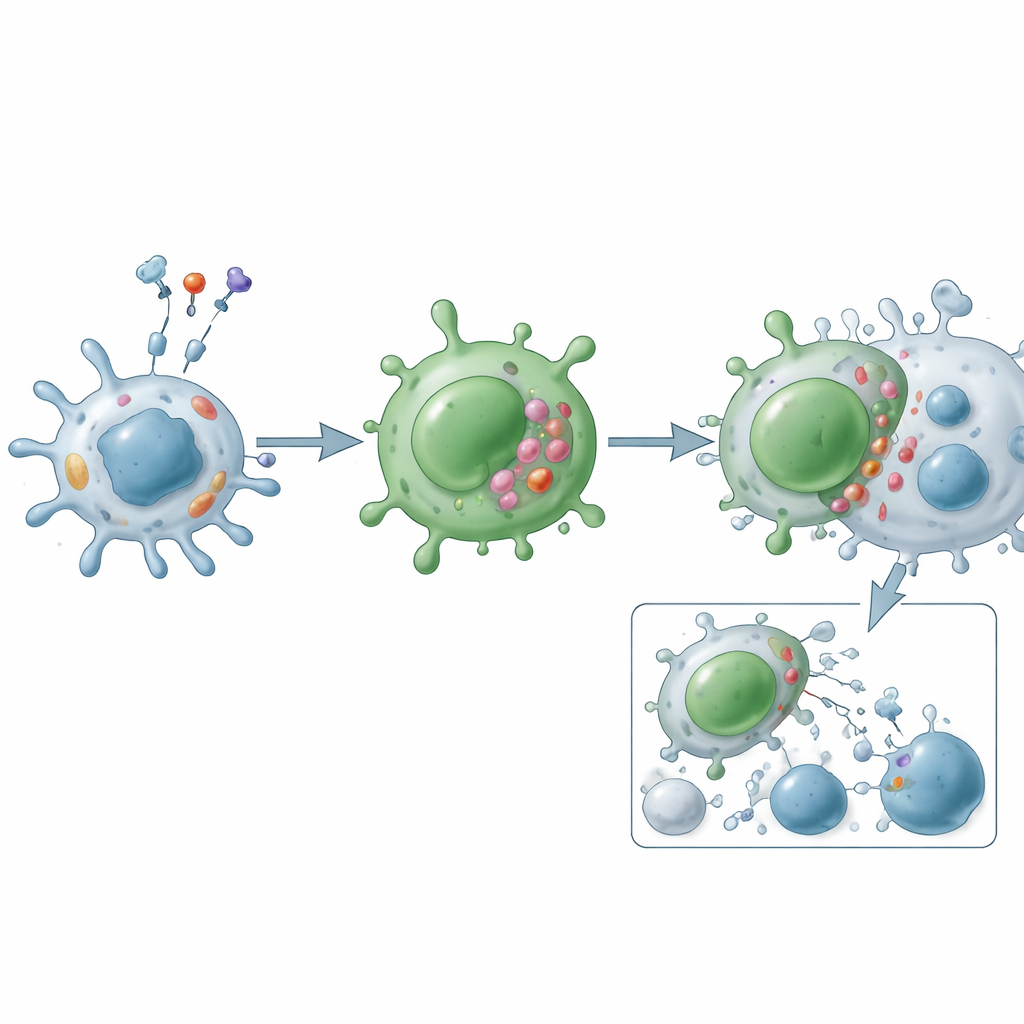
Alliées contre l’infection et le cancer, ennemies dans l’auto-immunité et les maladies cardiaques
Ce comportement à double tranchant se manifeste dans de nombreuses conditions. Dans les hépatites chroniques B, le VIH et la COVID-19, les cellules T CD4 cytotoxiques contribuent au contrôle viral lorsque les CD8 effecteurs sont épuisés, et leur présence peut s’associer à un meilleur contrôle ou à la récupération. Dans les tumeurs solides et les hémopathies malignes, elles peuvent reconnaître directement les cellules tumorales présentant les bons marqueurs ou signaux de stress et améliorer potentiellement les réponses aux immunothérapies comme les inhibiteurs de points de contrôle et les traitements par CAR-T. En parallèle, ces mêmes mécanismes peuvent causer des dommages : dans le lupus, la polyarthrite rhumatoïde, les maladies inflammatoires de l’intestin, la maladie coronarienne, la fibrillation auriculaire, l’artérite à cellules géantes et le rejet de greffe, des populations accrues de cellules T CD4 cytotoxiques infiltrent les tissus, endommagent vaisseaux ou organes et amplifient l’inflammation persistante, souvent en corrélation avec un pronostic plus mauvais.
Transformer un outil risqué en thérapie
Parce que les cellules T CD4 cytotoxiques peuvent être protectrices ou destructrices, l’article met en avant des stratégies thérapeutiques émergentes qui cherchent à affiner, plutôt qu’à effacer, cette population. Une approche consiste à atténuer leur activité néfaste à l’aide d’inhibiteurs sélectifs ciblant des récepteurs co-stimulateurs (comme OX40 ou 4-1BB), des cytokines inflammatoires, des canaux ioniques ou des voies de survie. Une autre consiste à exploiter leur pouvoir cytotoxique dans des thérapies cellulaires adoptives, y compris des lymphocytes génétiquement modifiés et des CAR-T, où les cellules CD4 cytotoxiques montrent souvent une meilleure persistance que des produits composés uniquement de CD8. Une troisième stratégie propose de rediriger des CD4 tueuses à longue durée de vie, spécifiques de virus, vers des tumeurs au moyen de vaccins ou de peptides dérivés de pathogènes présentés par les cellules cancéreuses. Ensemble, ces axes de recherche positionnent les cellules T CD4 cytotoxiques non pas seulement comme une curiosité biologique, mais comme un levier central pour des traitements futurs capables de stimuler de manière plus précise la défense contre les infections et le cancer tout en réduisant l’inflammation destructrice des tissus.
Un nouveau levier pour les thérapies immunitaires futures
Pour le grand public, le message clé est que les cellules T CD4 « aides » sont beaucoup plus polyvalentes qu’on ne le pensait : certaines peuvent basculer en tueuses pleinement armées qui nous protègent contre les infections persistantes et le cancer, mais contribuent aussi à l’auto-immunité, aux dégâts vasculaires et au rejet de greffe. La revue soutient que savoir suivre ces cellules, prévoir quand elles aideront ou nuiront, et ajuster leur comportement avec des médicaments ou des thérapies conçues pourrait transformer la prise en charge d’un large éventail de maladies chroniques — de l’hépatite et du VIH à l’arthrite, la colite, les maladies cardiaques et la leucémie. Plutôt que de simplement monter ou baisser l’activité immunitaire, les thérapies futures pourraient de plus en plus viser à orienter des types cellulaires puissants comme les cellules T CD4 cytotoxiques vers des cibles bénéfiques et loin de nos propres tissus.
Citation: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
Mots-clés: cellules T CD4 cytotoxiques, plasticité des cellules immunitaires, inflammation chronique, immunothérapie du cancer, maladie auto-immune