Clear Sky Science · fr
IFFO1 inhibe le cancer du sein en coordonnant la fission mitochondriale et la synthèse des acides gras via l’axe LaminA/C-PGC1α
Pourquoi cette recherche est importante
Le cancer du sein reste l’une des principales causes de mortalité par cancer chez les femmes, en grande partie parce que certains tumeurs continuent de croître, de se propager et d’échapper aux traitements actuels. Cette étude met au jour un « frein » cellulaire jusqu’ici sous-estimé, nommé IFFO1, qui ralentit le cancer du sein en maîtrisant deux moteurs centraux de la progression tumorale : les usines énergétiques de la cellule, les mitochondries, et sa capacité à synthétiser et stocker des lipides. Comprendre ce frein offre un nouvel angle thérapeutique potentiel qui pourrait être applicable à plusieurs sous‑types de cancer du sein.
Un gardien caché au sein des cellules mammaires
Les chercheurs ont commencé par analyser des prélèvements de 30 femmes atteintes d’un cancer du sein, ainsi que de larges bases de données publiques sur le cancer. Ils ont constaté que les niveaux de la protéine IFFO1 étaient systématiquement plus faibles dans les tissus tumoraux que dans les tissus mammaires normaux adjacents. Plus le stade du cancer était avancé, moins IFFO1 était présent, et les patientes dont les tumeurs exprimaient des niveaux plus élevés d’IFFO1 présentaient une survie prolongée. Dans des cellules de cancer du sein en culture, forcer l’expression d’IFFO1 réduisait nettement leur capacité à croître, à se diviser et à migrer — des comportements nécessaires à l’expansion et à la dissémination tumorales. IFFO1 atténuait également un programme cellulaire connu sous le nom de transition épithélio‑mésenchymateuse, qui aide les cellules cancéreuses à se détacher et à envahir d’autres tissus.
Calmer des usines énergétiques hyperactives
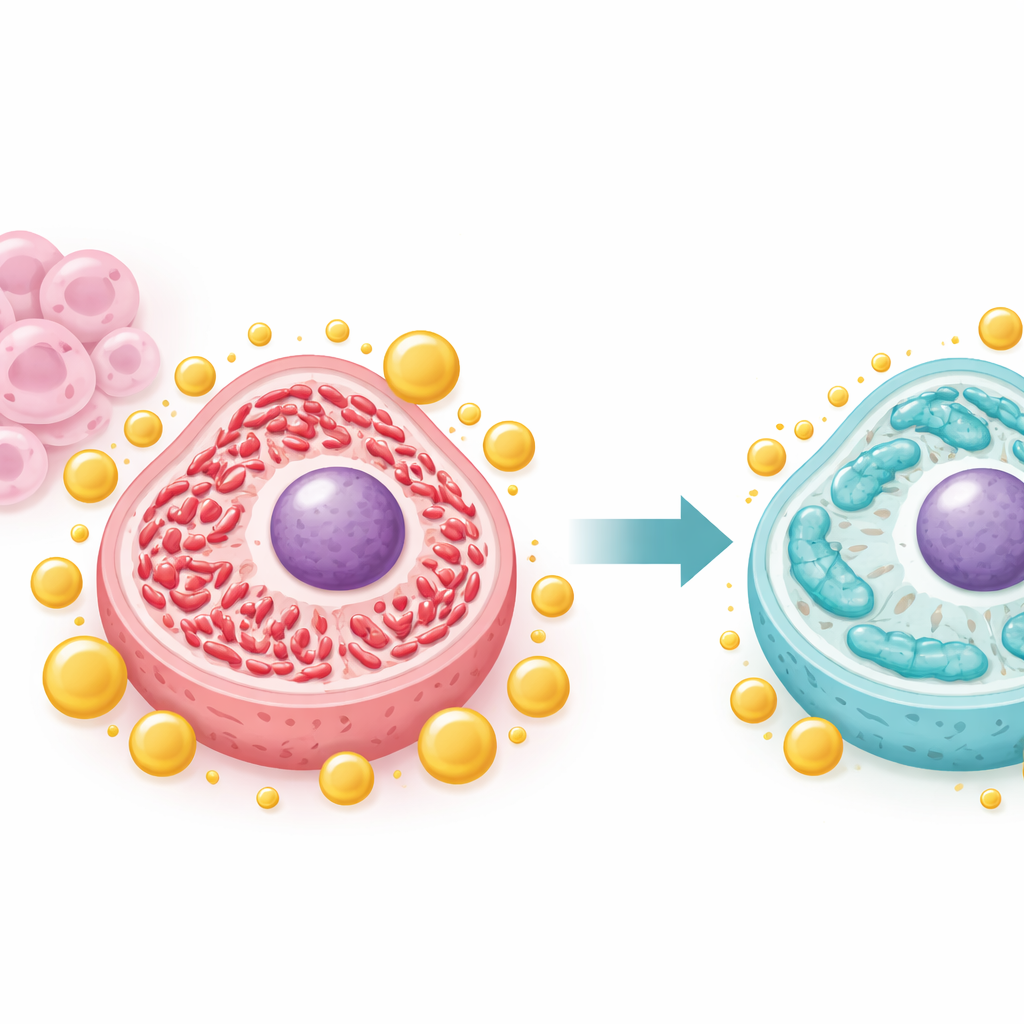
Les cellules cancéreuses reconfigurent souvent leurs mitochondries, ces petites centrales énergétiques, pour soutenir une croissance rapide. L’équipe a montré qu’IFFO1 déplace cet équilibre d’un état fortement fragmenté (« fission ») vers un état plus allongé (« fusion ») associé en général à des mitochondries plus saines et plus stables. Lorsque IFFO1 était abondant, des protéines clés de la fission comme Drp1 et Fis1 diminuaient, tandis que les protéines de fusion augmentaient. La microscopie a révélé des mitochondries plus longues et moins fragmentées, et les mesures d’ADN mitochondrial et de production d’énergie retombaient depuis les niveaux anormalement élevés observés dans les cellules agressives. Ces changements suggèrent qu’IFFO1 empêche les mitochondries d’adopter une configuration hyperactive qui soutient la croissance tumorale incontrôlée.
Couper la ligne d’approvisionnement en lipides
Les tumeurs à croissance rapide n’ont pas seulement besoin d’énergie ; elles ont aussi besoin d’un apport constant en lipides pour construire de nouvelles membranes et des molécules de signalisation. L’étude montre qu’IFFO1 freine aussi cet accélérateur métabolique. Dans les cellules surexprimant IFFO1, les protéines centrales de la lipogenèse — notamment FASN, SREBP‑1, SCD1 et d’autres — étaient réduites. Des tests enzymatiques ont confirmé une activité de synthèse lipidique plus faible, et des dosages chimiques ont montré des baisses d’acides gras libres, de triglycérides et de cholestérol. Des sondes d’imagerie révélant les réserves lipidiques ont mis en évidence moins de gouttelettes lipidiques et une moindre accumulation de graisses neutres dans les cellules cancéreuses. Inversement, l’augmentation de la protéine de fission Drp1 avait l’effet contraire en stimulant la production de lipides, tandis que le silence de Drp1 la réduisait — soutenant un lien direct entre la morphologie mitochondriale et l’approvisionnement en lipides dans le cancer.
Une chaîne de signalisation du noyau aux mitochondries
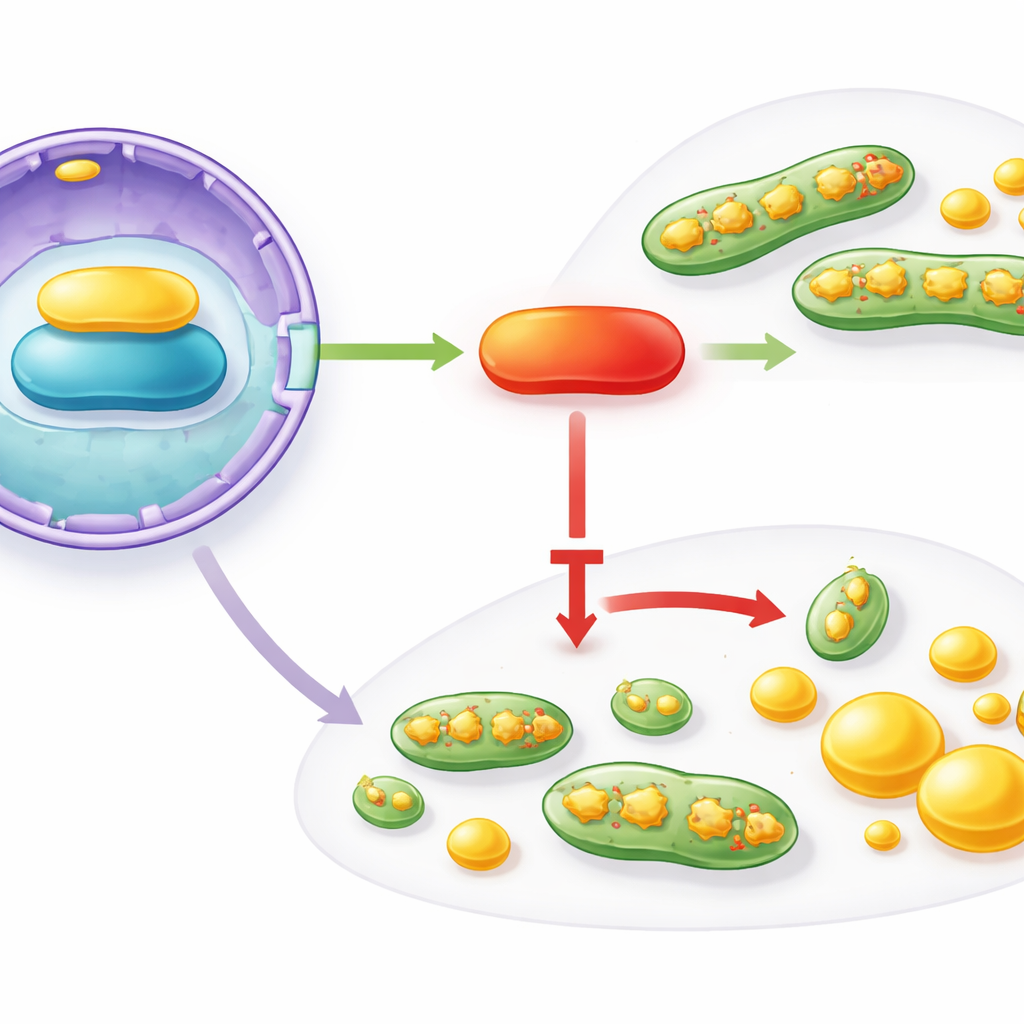
Comment IFFO1 orchestre‑t‑il ces larges changements ? Les auteurs ont tracé une chaîne d’interactions qui commence au noyau cellulaire et se termine aux mitochondries et à la machinerie lipogénique. IFFO1 se lie physiquement à une protéine structurale de l’enveloppe nucléaire appelée Lamin A/C et en augmente les niveaux. Lamin A/C soutient à son tour l’activité de PGC1α, un régulateur maître qui contrôle la santé mitochondriale et le métabolisme. Dans les tissus et cellules de cancer du sein, Lamin A/C et PGC1α étaient également réduits, reflétant la perte d’IFFO1. Lorsque les scientifiques ont surexprimé artificiellement IFFO1, Lamin A/C et PGC1α augmentaient, la fission mitochondriale diminuait et la synthèse lipidique faiblissait. L’inhibition de Lamin A/C annulait ces bénéfices, mais la restauration de PGC1α les rétablissait, identifiant ainsi un axe fonctionnel IFFO1 → Lamin A/C → PGC1α qui restreint les modifications mitochondriales et lipidiques favorisant la tumeur.
Tester le frein chez l’animal
Pour vérifier si ces effets cellulaires se traduisent par une réduction tumorale in vivo, l’équipe a implanté des cellules de cancer du sein humain avec ou sans surexpression d’IFFO1 chez des souris. Les tumeurs surexprimant IFFO1 croissaient plus lentement, pesaient moins au terme de l’expérience et montraient moins de signes d’accumulation lipidique. Dans un modèle distinct où des cellules cancéreuses étaient injectées dans la circulation pour coloniser les poumons, les cellules surexprimant IFFO1 formaient nettement moins de nodules tumoraux pulmonaires. Les analyses tissulaires chez ces souris confirmaient les observations in vitro : Lamin A/C et PGC1α plus élevés, fission mitochondriale réduite et synthèse lipidique diminuée.
Ce que cela signifie pour les traitements futurs
Pris ensemble, ces travaux présentent IFFO1 comme un suppresseur de tumeur multi‑niveau qui relie l’échafaudage structural de la cellule, ses centrales énergétiques et sa machinerie de fabrication des lipides. En stabilisant Lamin A/C et en augmentant PGC1α, IFFO1 empêche les mitochondries de se fragmenter excessivement et coupe la surproduction de lipides dont les cellules cancéreuses dépendent. Pour un public non spécialiste, le message clé est que cette protéine agit comme un frein interne sur la puissance et les éléments de construction qui alimentent la croissance et la dissémination du cancer du sein. Des médicaments qui élèveraient les niveaux d’IFFO1 ou imiteraient ses effets sur l’axe Lamin A/C–PGC1α pourraient un jour offrir de nouvelles options, en particulier pour les formes agressives ou résistantes au traitement du cancer du sein.
Citation: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Mots-clés: cancer du sein, dynamique mitochondriale, synthèse des acides gras, métabolisme tumoral, voie PGC1α