Clear Sky Science · fr
Le contrôle oncogénique de la synthèse des nucléotides
Pourquoi les cellules cancéreuses tiennent tant aux éléments de construction
Le cancer est souvent décrit comme des cellules qui ne cessent de se diviser. Mais pour se copier, ces cellules ont besoin d’un apport constant de petites briques appelées nucléotides, qui composent l’ADN et l’ARN et alimentent aussi de nombreux processus cellulaires. Cette revue explique comment les gènes oncogènes réorganisent la chimie cellulaire pour maintenir une production élevée de nucléotides, comment les tumeurs basculent entre différentes façons d’obtenir ces molécules, et comment les cliniciens peuvent exploiter ces astuces avec des médicaments anciens et nouveaux.
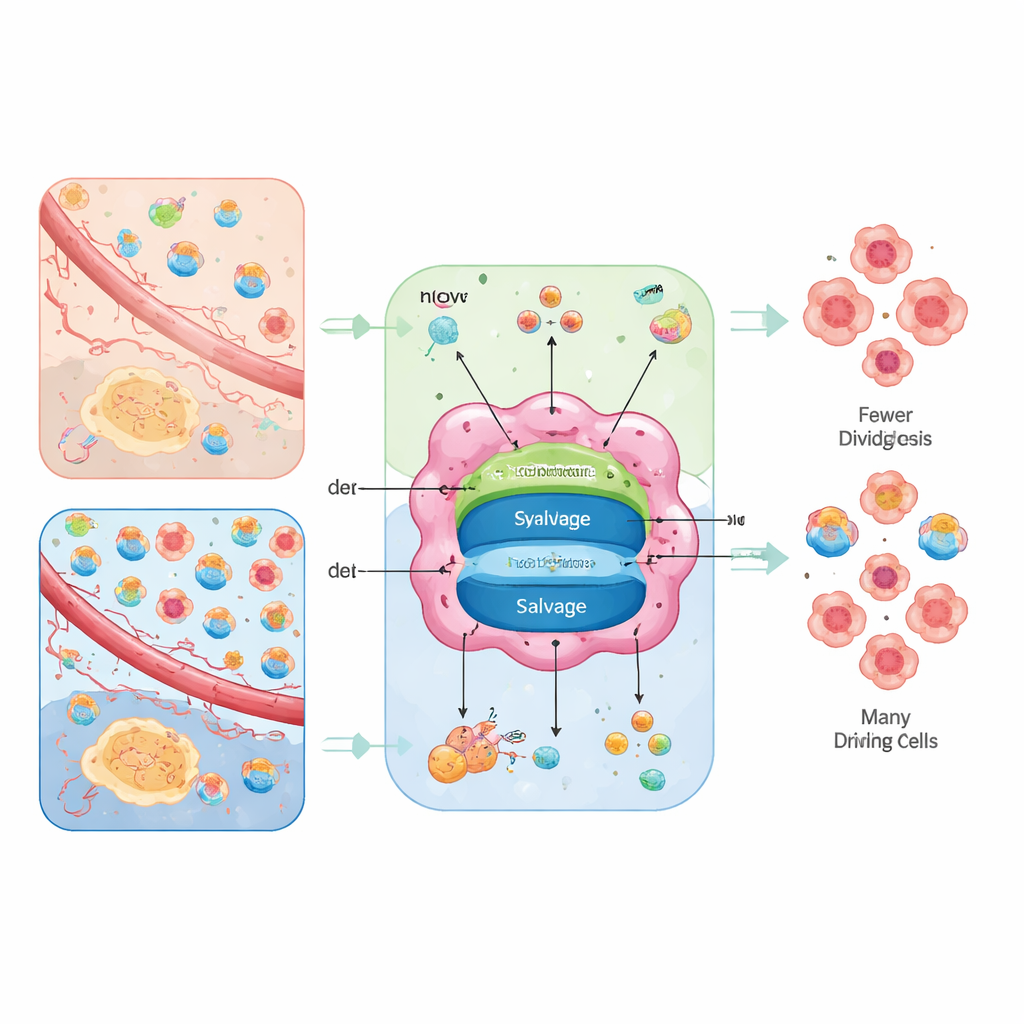
Deux routes vers les mêmes briques
Les cellules peuvent fabriquer des nucléotides à partir de rien ou les recycler. La voie « à partir de zéro », appelée synthèse de novo, assemble les noyaux à partir de nutriments de base comme le glucose, les acides aminés, le dioxyde de carbone et le bicarbonate, via des réactions multi‑étapes gourmandes en énergie. La voie de recyclage, dite de sauvetage, récupère des bases et nucléosides dégradés provenant de l’extérieur ou des déchets cellulaires et les reconvertit en nucléotides utilisables à un coût énergétique bien moindre. Les tumeurs utilisent les deux options, mais l’équilibre entre elles dépend de leur approvisionnement interne en énergie et de ce que le tissu environnant fournit.
Comment l’environnement tumoral oriente le choix
Les auteurs présentent l’approvisionnement en nucléotides comme un problème de « routage façonné par l’environnement ». Dans les régions mal alimentées où les acides aminés sont présents mais où les nucléosides libres se font rares, les cellules cancéreuses s’appuient fortement sur les voies de novo et deviennent vulnérables aux médicaments qui bloquent ces étapes. Dans les zones mieux perfusées, où le sang apporte beaucoup de nucléosides ou où les mitochondries sont déficientes, les tumeurs peuvent compter davantage sur la voie de sauvetage, devenant alors sensibles aux bloqueurs de transporteurs qui empêchent l’entrée des nucléosides. Quand les deux options sont disponibles, les tumeurs montrent une flexibilité métabolique et peuvent échapper à un médicament unique ; quand les deux sont fermées, les cellules s’arrêtent en phase de réplication de l’ADN, accumulent des dommages et peuvent mourir ou se différencier en états plus matures et moins agressifs.
Lignes de soutien cachées qui alimentent la production de nucléotides
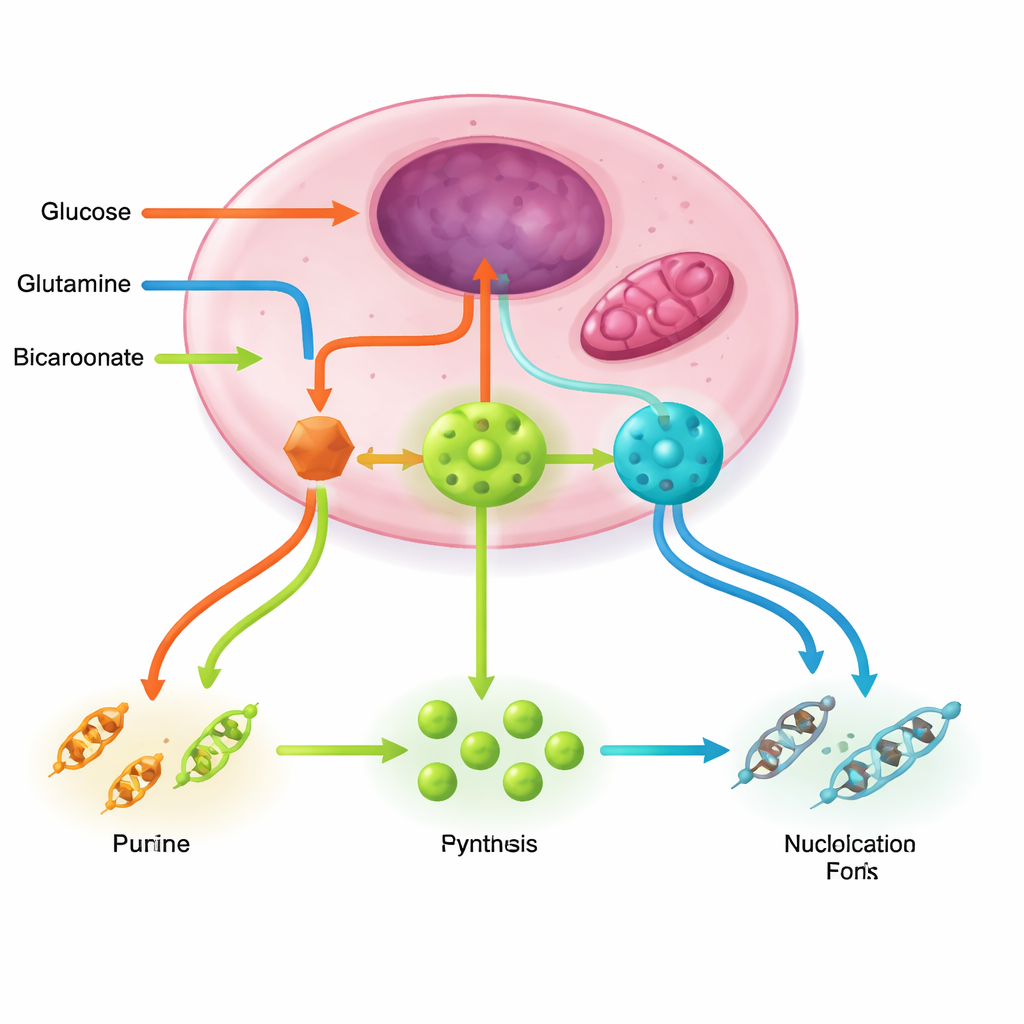
Maintenir les « usines » à nucléotides en activité nécessite plusieurs circuits d’appui. La voie des pentoses phosphate fournit l’épine dorsale sucrée et le pouvoir réducteur ; la glutamine et le cycle énergétique mitochondrial apportent l’azote et l’aspartate ; la chimie de la sérine, de la glycine et du folate fournit des unités à un seul carbone qui complètent les noyaux ; le bicarbonate introduit des carbones essentiels. Des oncogènes comme PI3K–AKT–mTORC1, RAS–MAPK et MYC stimulent ces voies de concert, augmentent les enzymes clés et assemble même des complexes multi‑enzymatiques qui canalisent efficacement des intermédiaires instables. En revanche, des capteurs de stress tels que LKB1–AMPK et p53 jouent normalement le rôle de freins, réduisant la production de nucléotides lorsque l’énergie ou l’intégrité de l’ADN est menacée — des freins que de nombreuses tumeurs désactivent.
Vieille chimiothérapie, nouvelle logique métabolique
Parce que les cellules à croissance rapide dépendent fortement des nucléotides, certaines des premières chimiothérapies ont ciblé cette faiblesse. Des médicaments classiques tels que le méthotrexate, le 5‑fluorouracile, la cytarabine, la gemcitabine et divers analogues des purines bloquent l’usage du folate, inhibent des enzymes spécifiques ou se font passer pour des briques défectueuses qui empoisonnent l’ADN et l’ARN. La revue revisite ces traitements à travers le prisme du modèle de routage, expliquant pourquoi les effets secondaires et la résistance sont fréquents : les tissus non cancéreux ont aussi besoin de nucléotides, et les tumeurs peuvent souvent dévier le flux via la voie de sauvetage ou des voies parallèles lorsqu’un nœud est bloqué.
Stratégies de nouvelle génération et questions ouvertes
Les approches plus récentes visent une plus grande sélectivité en frappant les éléments du réseau les plus biaisés vers le cancer. Des médicaments expérimentaux sont développés contre des enzymes mitochondriales de la voie à un carbone comme MTHFD2, contre l’enzyme pyrimidinique DHODH, et contre des enzymes puriniques comme IMPDH et PAICS, souvent en combinaisons qui bloquent aussi les transporteurs de sauvetage. Les auteurs proposent des marqueurs pratiques — tels que le niveau des transporteurs, la densité vasculaire, l’état fonctionnel des mitochondries et l’expression d’enzymes métaboliques spécifiques — pour déterminer quelles tumeurs dépendent davantage de la synthèse de novo ou du sauvetage et pour associer les patients à des thérapies ciblant ces voies. En regardant vers l’avenir, ils soulignent des questions clés, notamment comment ces routes varient dans l’espace et le temps au sein des tumeurs réelles, comment les cellules immunitaires et stromales environnantes modulent la disponibilité des nucléotides, et comment concevoir des schémas médicamenteux tolérables qui exploitent le stress de réplication sans submerger les tissus normaux. Ensemble, ce travail soutient que comprendre et cibler le métabolisme des nucléotides pourrait transformer une exigence fondamentale de la division cellulaire en un levier puissant et personnalisé contre le cancer.
Citation: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Mots-clés: métabolisme des nucléotides, métabolisme du cancer, synthèse de novo, voies de recyclage, thérapies métaboliques