Clear Sky Science · fr
Profilage transcriptomique de cellules cancéreuses et hôtes en co-culture identifie l’hypoxie comme moteur de l’effet antiprolifératif des cellules musculaires squelettiques sur les cellules cancéreuses
Pourquoi certains tissus résistent à la propagation du cancer
Le cancer devient généralement mortel lorsque des cellules tumorales quittent leur site d’origine et s’implantent dans des organes distants. Curieusement, certains tissus, comme les poumons, sont des lieux d’atterrissage fréquents, tandis que d’autres, tels que le muscle squelettique, sont presque jamais colonisés malgré leur forte proportion dans la masse corporelle. Cette étude pose une question simple mais importante pour les patients et les médecins : qu’est-ce qui rend le muscle si mauvais terrain pour la croissance des cellules cancéreuses, et la compréhension de cette défense naturelle pourrait-elle modifier notre approche du traitement des métastases ?
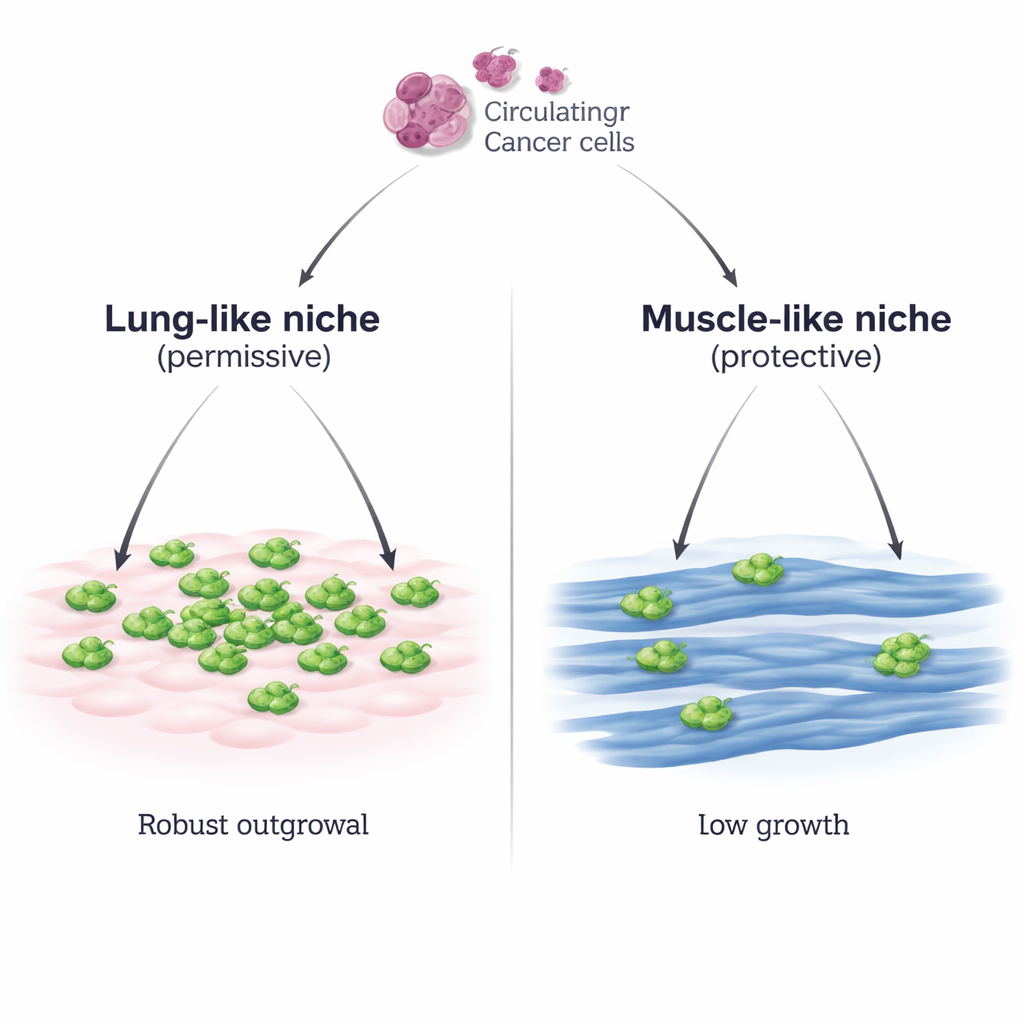
Deux quartiers pour les cellules tumorales voyageuses
Les chercheurs ont mis au point un système de laboratoire contrôlé qui reproduit deux environnements différents qu’une cellule de cancer du sein pourrait rencontrer : un environnement de type pulmonaire constitué de cellules du tissu conjonctif pulmonaire (MLg), et un environnement de type musculaire composé de fibres musculaires squelettiques matures (myotubes C2C12). Ils ont déposé des cellules de cancer du sein de souris au-dessus de chaque couche et observé la suite. Sur les cellules de type pulmonaire, les cellules cancéreuses s’attachaient bien puis se multipliaient rapidement, formant des foyers denses. Sur les cellules musculaires, elles s’attachaient tout autant, mais leur croissance restait clairsemée et lente, même lorsque le nombre initial de cellules cancéreuses était fortement augmenté ou lorsqu’une seconde lignée de cancer du sein était utilisée. Une autre lignée musculaire squelettique (Sol8) a montré la même capacité à freiner la croissance tumorale, ce qui souligne qu’il s’agit d’une propriété générale des cellules musculaires et non d’une particularité d’un type cellulaire unique.
Comment les cellules cancéreuses et hôtes réorganisent leur activité
Pour comprendre ce qui se passait à l’intérieur des cellules, l’équipe a isolé les cellules cancéreuses et les cellules hôtes de ces co-cultures mixtes et séquencé leur ARN, un indicateur des gènes activés ou réprimés. Les cellules cancéreuses en contact avec les fibres musculaires ont subi des changements d’activité génique beaucoup plus étendus que celles poussant sur les cellules pulmonaires, suggérant que l’environnement musculaire les oblige à s’adapter fortement. Dans le contexte musculaire, les cellules cancéreuses ont activé des programmes liés à des caractéristiques de type musculaire, au métabolisme énergétique et, de manière surprenante, aux réponses à la faible teneur en oxygène (hypoxie). Parallèlement, les programmes géniques habituels qui favorisent une division cellulaire rapide étaient atténués. En revanche, les cellules cancéreuses sur cellules pulmonaires conservaient un profil fortement orienté vers la croissance et nécessitaient beaucoup moins de reprogrammation, ce qui est cohérent avec l’idée que le niche de type pulmonaire est permissif et facile à exploiter pour les cellules tumorales.
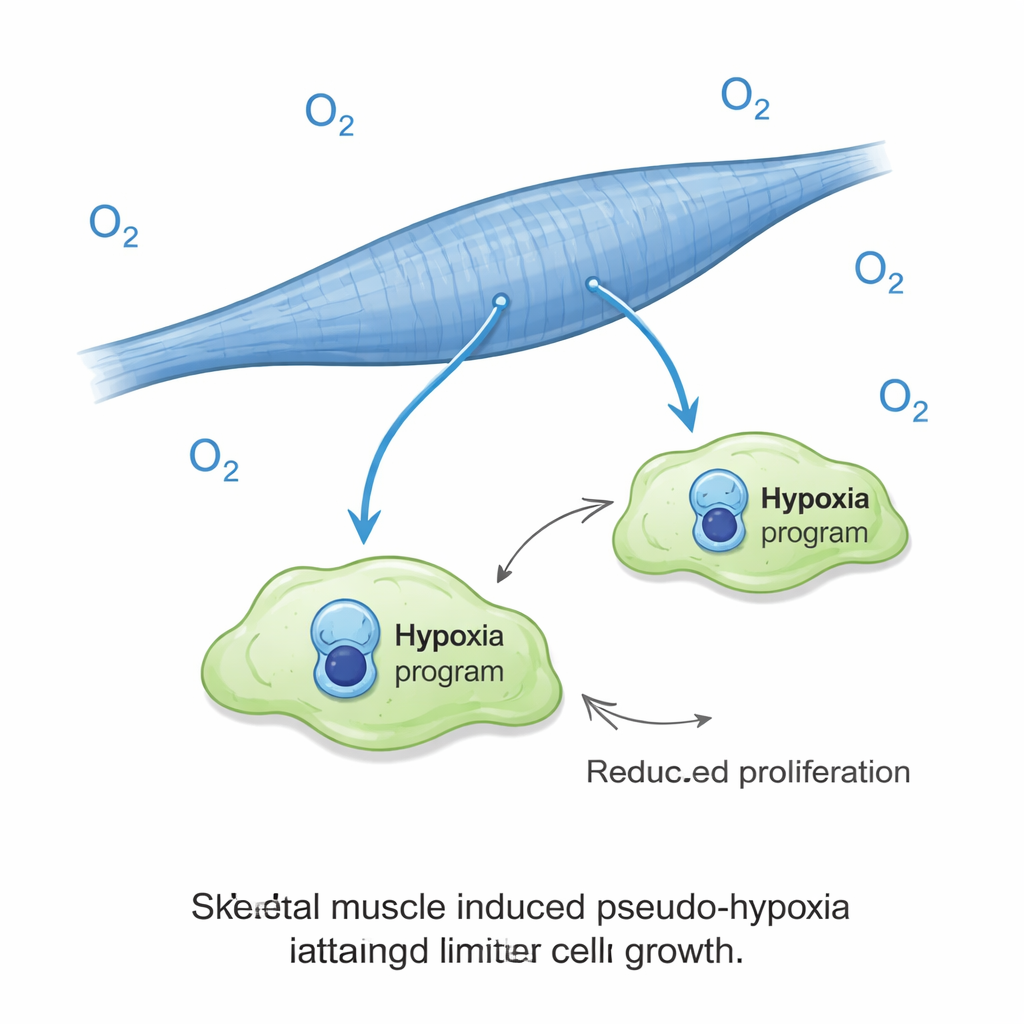
Un rôle surprenant des signaux de faible oxygène
Une des constatations les plus marquantes fut que les cellules cancéreuses sur fibres musculaires activaient une signature génique de type hypoxique alors même qu’elles étaient cultivées sous des niveaux normaux d’oxygène. Dans la plupart des tumeurs, l’hypoxie est un mauvais signe, généralement associée à un comportement agressif et à de mauvais pronostics. Ici, elle était liée à l’inverse : une faible croissance. Les scientifiques ont ensuite exposé les cultures à une réelle hypoxie et ont constaté que cela anéantissait presque l’expansion des cellules cancéreuses sur muscle, alors que cela stimulait la croissance des cellules cancéreuses dans les cultures de type pulmonaire. En d’autres termes, le même signal qui habituellement aide les tumeurs à prospérer est devenu un frein lorsque les cellules cancéreuses se trouvaient dans un environnement musculaire. Cet effet de l’oxygène ne semble pas s’expliquer par de simples variations de lactate, d’acidité ou de disponibilité en sucres dans le milieu de culture.
Plus que de simples facteurs sécrétés
L’équipe a également testé si des substances solubles libérées par les cellules musculaires pouvaient expliquer leur effet protecteur. L’ajout de lactate, la modification de l’acidité, le changement des niveaux de glucose, ou la mise en culture de cellules cancéreuses dans un milieu ayant déjà baigné des cellules musculaires n’ont pas reproduit la forte suppression observée en co-culture en contact direct. Cela suggère que le contact physique étroit, ou des signaux de très courte portée à la surface cellulaire, sont essentiels pour la façon dont les cellules musculaires poussent les cellules cancéreuses vers un état de faible prolifération, possiblement dormant. Fait intéressant, les cellules musculaires elles-mêmes restaient relativement stables dans leur activité génique face au cancer, tandis que les cellules pulmonaires étaient plus facilement reprogrammées, soulignant le muscle comme un tissu robuste « résistant aux métastases ».
Ce que cela signifie pour les patients et les thérapies
Dans l’ensemble, l’étude révèle que le muscle squelettique agit comme un habitat hostile qui contraint les cellules cancéreuses à un état de type hypoxique et de faible prolifération, même lorsque l’oxygène est abondant. Cela contribue à expliquer pourquoi le muscle est un site de métastase si rare. Cela envoie aussi un message de prudence pour le développement de médicaments : des thérapies visant à bloquer la signalisation liée à l’hypoxie dans tout l’organisme pourraient affaiblir involontairement cette défense naturelle liée au muscle, facilitant la croissance des cellules cancéreuses à des endroits où elles ne se développent normalement pas. Comprendre et préserver, voire imiter, les caractéristiques protectrices du tissu musculaire pourrait ouvrir de nouvelles voies pour prévenir ou contrôler la maladie métastatique.
Citation: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
Mots-clés: métastase cancéreuse, muscle squelettique, hypoxie, microenvironnement tumoral, dormance cancéreuse