Clear Sky Science · fr
L’absorption d’acides gras médiée par FABP4 favorise la sénescence des cellules T CD8+ via la peroxydation lipidique dans le microenvironnement riche en adipocytes du cancer de l’ovaire
Pourquoi les cellules graisseuses et immunitaires comptent dans le cancer de l’ovaire
Le cancer de l’ovaire se propage souvent dans la cavité abdominale, où il rencontre d’importants dépôts de graisse corporelle. Cet environnement adipeux n’est pas un simple décor passif — il influence activement le comportement des cellules immunitaires. En particulier, il peut affaiblir les cellules T CD8 « tueuses » censées attaquer les tumeurs. Cette étude examine comment des substances d’origine lipidique poussent ces cellules T vers un état de vieillissement fonctionnel et comment le blocage d’une protéine clé de transport des lipides pourrait aider à restaurer leur capacité anticancéreuse.
Un entourage riche en graisses qui vieillit les défenseurs immunitaires
Les cliniciens observent depuis longtemps que de nombreuses patientes atteintes d’un cancer de l’ovaire avancé accumulent du liquide dans l’abdomen et présentent des tumeurs nichées dans des tissus riches en graisse, comme l’épiploon. En analysant des données d’ARN unicellulaire de patientes et en examinant des échantillons tumoraux au microscope, les chercheurs ont constaté que les cellules T CD8 proches de ces dépôts adipeux montraient davantage de signes de vieillissement cellulaire, ou sénescence. Ces cellules T « vieillies » accumulent des pigments résiduels, arrêtent de se diviser et produisent des signaux inflammatoires au lieu de tuer les cellules cancéreuses. Dans des échantillons humains comme dans des modèles murins, les cellules T CD8 prélevées dans des zones tumorales riches en graisse et en liquide étaient nettement plus sénescentes que celles provenant des nœuds lymphatiques ou de la rate, établissant un lien direct entre le microenvironnement riche en adipocytes et le vieillissement des T cellules.
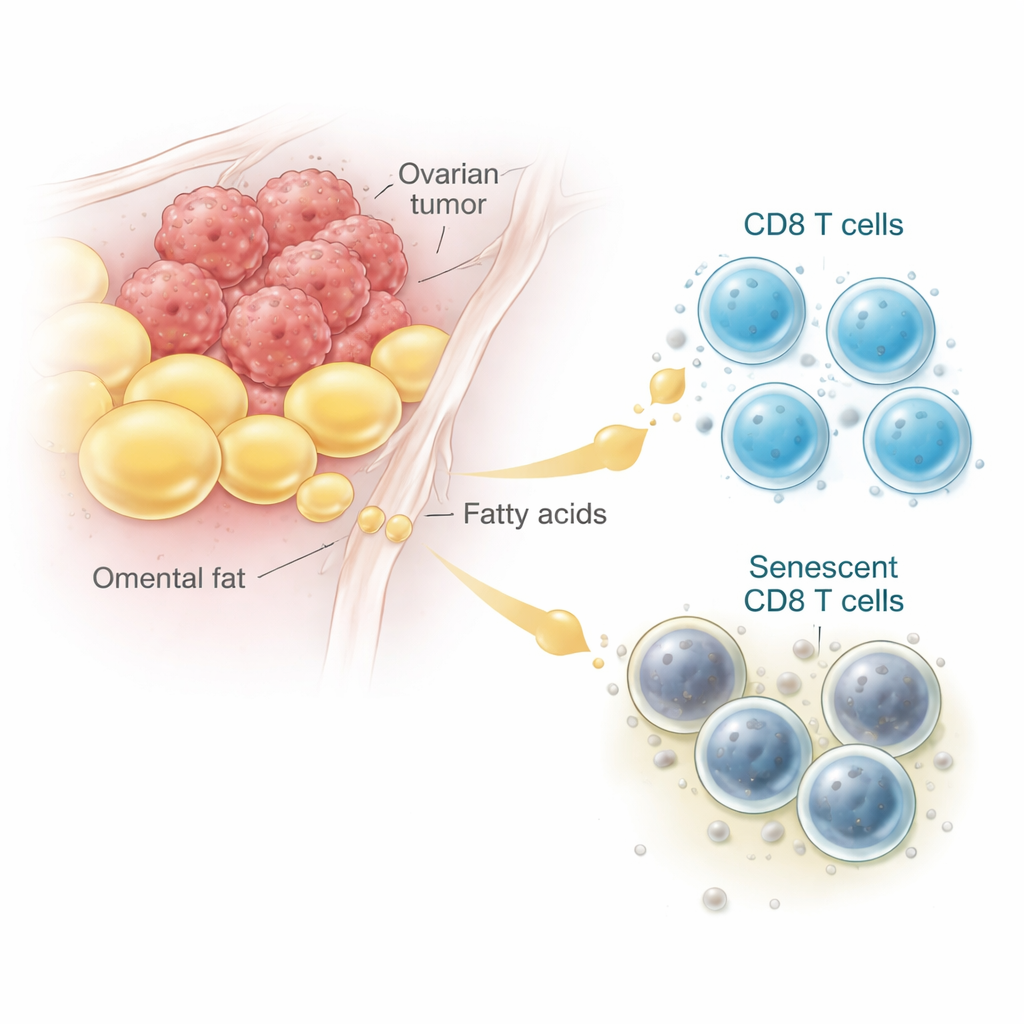
Comment un acide gras courant transforme un carburant utile en dommage
Pour comprendre l’effet des lipides sur les cellules T, l’équipe a recréé le contexte tumoral en laboratoire. Ils ont cultivé des cellules de cancer de l’ovaire avec des cellules T CD8 de souris, puis ajouté soit des extraits de tissu adipeux soit un acide gras spécifique, l’acide oléique, abondant dans le liquide péritonéal des cancers de l’ovaire. À des concentrations modérées à élevées, l’acide oléique a favorisé la sénescence de nombreuses cellules T CD8 — mais seulement en présence de cellules tumorales. Au lieu d’oxyder ces lipides entrants pour produire de l’énergie, les cellules T ont accumulé des lipides qui sont devenus chimiquement endommagés, un processus appelé peroxydation lipidique. Des analyses transcriptionnelles et lipidiques ont montré une augmentation des marqueurs de lipides oxydés et du stress, tandis que la production d’énergie à partir des lipides restait inchangée. En résumé, en présence de la tumeur, les lipides qui auraient dû servir de carburant sont détournés vers des réactions délétères qui vieillissent et désactivent les cellules T.
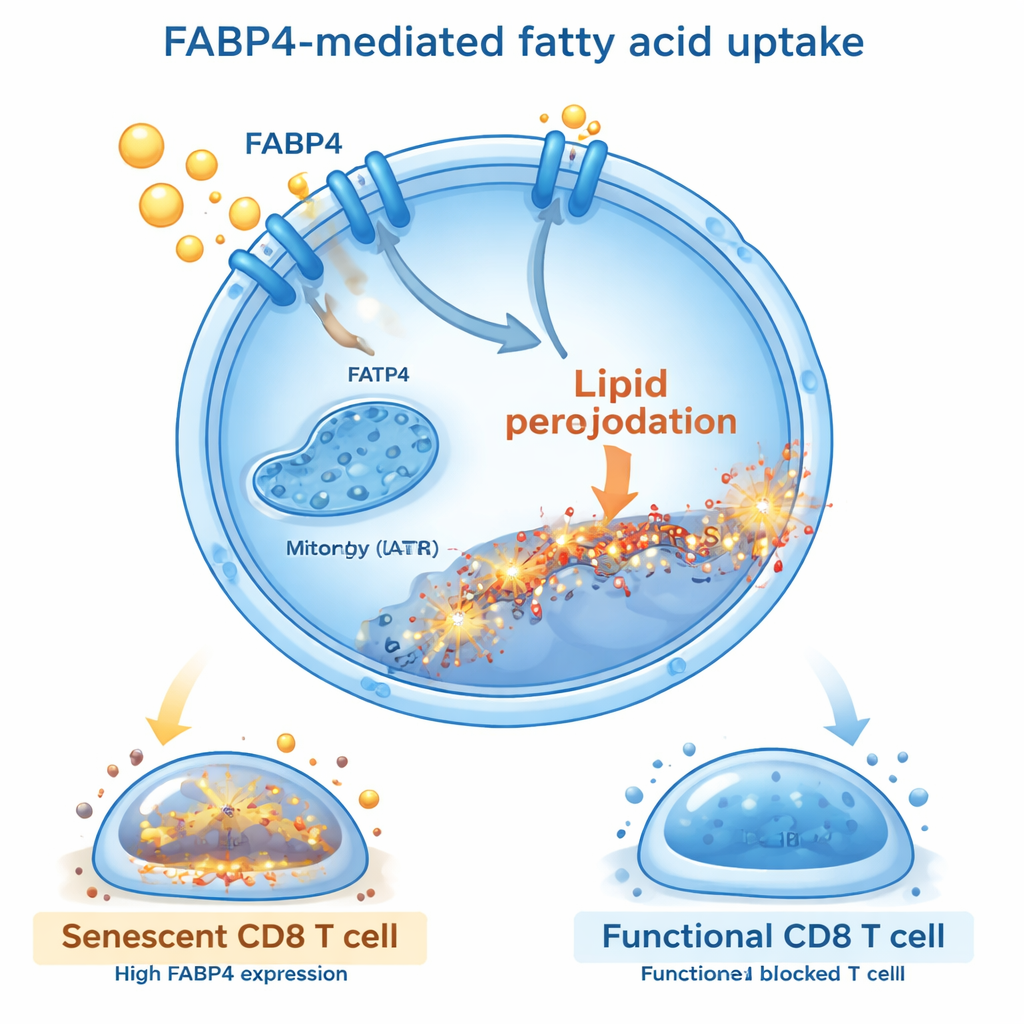
Le transporteur lipidique FABP4, un gardien clé
En approfondissant la question, les chercheurs ont cherché les molécules qui contrôlent cet afflux lipidique nocif. Ils ont constaté qu’une protéine de transport appelée FABP4 était fortement induite dans les cellules T CD8 exposées aux extraits de tissu adipeux ou à l’acide oléique. FABP4 agit comme une navette, transportant des acides gras à longue chaîne dans les cellules. Lorsqu’ils ont bloqué FABP4, soit par un petit inhibiteur moléculaire (BMS309403), soit par extinction génétique, les cellules T ont moins absorbé de lipides, ont présenté moins de peroxydation lipidique et étaient moins susceptibles de devenir sénescentes. Ces cellules T protégées se divisaient mieux, produisaient davantage de molécules tueuses comme l’interféron-gamma et la granzyme B, et libéraient moins de signaux suppressifs et inflammatoires. La restauration des niveaux de FABP4 annulait ces bénéfices, confirmant que ce transporteur est un commutateur central reliant l’entrée lipidique à la sénescence des cellules T.
Des expériences murines à une stratégie thérapeutique potentielle
L’équipe a ensuite testé le blocage de FABP4 chez des souris porteuses de cancers de l’ovaire disséminés dans l’abdomen. Le traitement par l’inhibiteur de FABP4 a réduit l’absorption lipidique et les dégâts lipidiques dans les cellules T CD8 prélevées dans le liquide abdominal, a diminué la proportion de cellules T sénescentes et a augmenté les niveaux de molécules effectrices clés. En combinant l’inhibiteur de FABP4 avec une chimiothérapie standard, les souris présentaient moins de nodules tumoraux visibles, des réponses T renforcées dans la rate, les nœuds lymphatiques et l’ascite, et une survie prolongée par rapport à celles traitées par chimiothérapie seule. Ces résultats suggèrent que cibler le métabolisme lipidique peut rendre les traitements existants plus efficaces en ravivant les premières lignes de défense immunitaires.
Ce que cela signifie pour les patientes
Pour un public non spécialisé, la conclusion est que dans le cancer de l’ovaire, ce n’est pas seulement la tumeur qui compte, mais aussi le voisinage graisseux dans lequel elle vit. Des molécules dérivées de la graisse, en particulier certains acides gras, peuvent vieillir prématurément les cellules T tueuses et les priver de leur capacité à attaquer le cancer. Ce travail identifie le transporteur lipidique FABP4 comme un élément clé de ce processus. En bloquant FABP4, au moins chez la souris, les chercheurs parviennent à réduire la sénescence des cellules T, à restaurer leur fonction cytotoxique et à améliorer l’effet de la chimiothérapie. Bien que des recherches supplémentaires soient nécessaires avant d’envisager une application clinique, l’étude ouvre une nouvelle voie : traiter non seulement la tumeur elle‑même, mais aussi les pièges métaboliques de son microenvironnement qui désarment le système immunitaire.
Citation: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
Mots-clés: cancer de l’ovaire, sénescence des cellules T, métabolisme des acides gras, microenvironnement tumoral, FABP4