Clear Sky Science · fr
Mutations génétiques courantes dans 103 lignées cellulaires authentifiées de cancer colorectal
Pourquoi ces lignées cellulaires cancéreuses sont importantes
Le cancer colorectal est l’un des cancers les plus fréquents dans le monde, et une grande partie de ce que nous savons sur son comportement et son traitement provient d’études réalisées sur des lignées cellulaires tumorales cultivées en laboratoire. Mais ces modèles peuvent dériver et évoluer avec le temps. Cette étude a vérifié et catalogué avec soin 103 lignées cellulaires de cancer colorectal largement utilisées, en cartographiant les principales mutations génétiques qui poussent la croissance tumorale. Le résultat est un « guide de terrain » détaillé qui aide les chercheurs à choisir le modèle adapté à la question étudiée, dans l’objectif de rendre les découvertes en laboratoire plus susceptibles de bénéficier aux patients futurs.
Un catalogue de modèles tumoraux
Les chercheurs ont rassemblé 103 lignées cellulaires de cancer colorectal qui, ensemble, reproduisent les principaux sous-types génétiques observés chez les patients. La plupart provenaient de tumeurs primitives du côlon ou du rectum, les autres venant de métastases. L’équipe a d’abord vérifié que chaque lignée cellulaire correspondait bien à son identité déclarée, en utilisant des marqueurs d’ADN de type « empreinte » appelés répétitions courtes en tandem. Ils ont ensuite utilisé un séquençage ciblé en profondeur, lisant des segments sélectionnés d’ADN en moyenne 575 fois, pour examiner 20 gènes connus pour leur importance dans le cancer colorectal. Cette grande profondeur a permis de détecter même des mutations relativement rares au sein d’une population cellulaire et d’estimer la fréquence de chaque mutation dans une lignée donnée.
Différents chemins vers le chaos génétique
Les cancers colorectaux peuvent emprunter des voies génétiques différentes au cours de leur développement. Environ quatre tumeurs sur cinq présentent une instabilité chromosomique, avec de larges segments d’ADN gagnés ou perdus. D’autres sont « hypermutés », accumulant de nombreux petits changements d’ADN. Cette étude a capturé les deux schémas. Seize lignées présentaient une instabilité des microsatellites, une forme d’hypermutation due à un défaut de réparation des mésappariements de l’ADN, entraînant des insertions et délétions fréquentes. Cinq autres présentaient des défauts dans le gène de relecture de l’ADN POLE, générant une lourde charge de changements d’une seule lettre. Les lignées non hypermutées restantes avaient moins de mutations mais davantage de variations importantes du nombre de copies d’ADN. Ces signatures distinctes ressemblaient étroitement à celles observées dans les tumeurs de patients réels.
Gènes moteurs clés et combinaisons dangereuses
Parmi les 20 gènes étudiés, les profils de mutations correspondaient aux grandes études cliniques sur le cancer colorectal. Les gènes suppresseurs de tumeur tels que APC, TP53 et SMAD4 étaient fréquemment atteints par des mutations tronquantes qui détruisent la protéine, tandis que des gènes classiquement promoteurs de cancer comme KRAS et BRAF portaient plus souvent des substitutions d’acides aminés uniques qui activent des voies de signalisation. Les lignées non hypermutées avaient tendance à porter une plus grande proportion de mutations clairement délétères, ou pathogènes, présentes dans la plupart ou la totalité des cellules de la culture. En revanche, les lignées hypermutées comportaient de nombreux changements « passagers » supplémentaires et davantage de mutations sous-clonales n’apparaissant que dans une fraction des cellules, reflet d’une évolution continue en culture.
Motifs cachés dans les interactions géniques
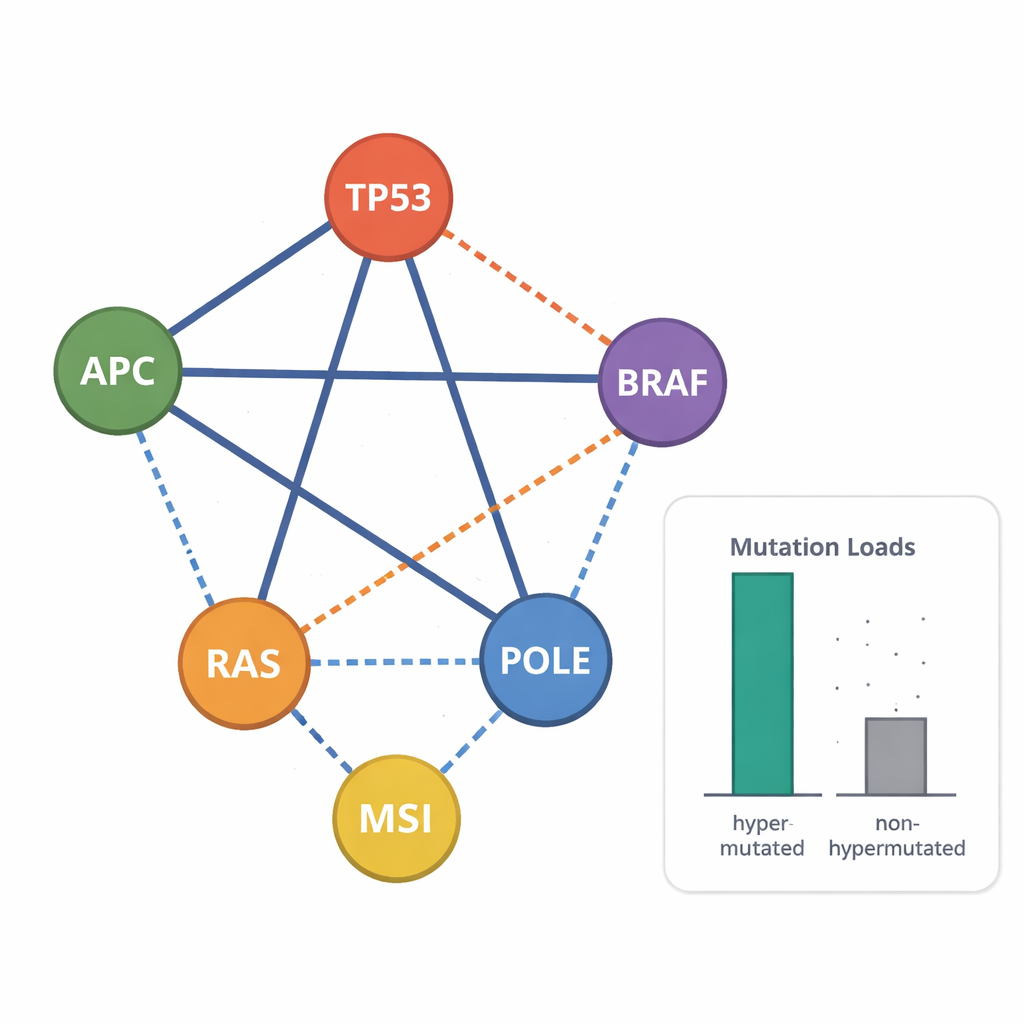
En examinant quelles mutations ont tendance à apparaître ensemble ou à s’éviter, les chercheurs ont identifié des combinaisons génétiques liées à des formes de maladie particulièrement agressives. Par exemple, la mutation hotspot courante BRAF p.V600 co-occurait rarement avec des mutations de KRAS ou NRAS, mais dans quelques lignées elle apparaissait aux côtés de mutations tronquantes de APC, faisant écho à un sous-type de mauvais pronostic observé chez des patients. De nombreuses lignées présentaient des altérations triples dans APC, TP53 et les gènes RAS, autre marqueur de tumeurs à haut risque. L’étude a également mis au jour un motif distinctif de « double-coup » dans APC : deux mutations tronquantes placées de sorte qu’au moins une région de liaison à la β-caténine demeure, cohérent avec un niveau « juste-assez » d’activation de la voie WNT favorable à la croissance tumorale. L’analyse du nombre de copies a montré des amplifications fréquentes de gènes liés à la croissance comme MYC et EGFR, et la perte de copies entières de gènes suppresseurs de tumeur, en particulier dans les lignées non hypermutées.
Ce que cela implique pour la recherche future
Pour les scientifiques qui conçoivent des expériences, le message est que toutes les lignées cellulaires de cancer colorectal ne se valent pas. Les modèles hypermutés sont génétiquement actifs et peuvent contenir de nombreux changements de bas niveau qui brouillent l’impact d’une mutation unique. À l’inverse, les lignées non hypermutées tendent à porter moins d’altérations mais plus fortes et plus homogènes. En fournissant une carte soigneusement validée des gènes altérés, de la nature de ces altérations et de la fréquence de chaque mutation dans chaque culture, ce travail permet aux chercheurs de choisir les modèles les plus appropriés pour tester des médicaments, explorer la biologie et développer de nouvelles approches ciblées ou d’immunothérapie pour le cancer colorectal.
Citation: Kranjec, C., Eilertsen, I.A., Nunes, L. et al. Common gene mutations in 103 authenticated colorectal cancer cell lines. Oncogenesis 15, 8 (2026). https://doi.org/10.1038/s41389-026-00599-0
Mots-clés: cancer colorectal, lignées cellulaires tumorales, mutations génétiques, sous-types tumoraux, oncologie de précision