Clear Sky Science · fr
Réorganisation du cytosquelette induite par une nouvelle fusion de kératines K6-K14 favorise la pluripotence tumorale et la plasticité cellulaire via la sélection cGAS-STING
Comment les cellules cancéreuses métamorphes déjouent leur environnement
Les cellules cancéreuses ne se contentent pas de croître de façon incontrôlée : elles apprennent aussi à plier et tordre leur « squelette » interne pour survivre, se cacher et se disséminer. Cette étude révèle comment un défaut structural spécifique dans des cellules de cancers de la tête et du cou peut briser leurs noyaux, déclencher une alarme de danger intrinsèque, les pousser en état de dormance, puis finalement leur permettre de réapparaître sous une forme plus agressive, invasive et ressemblant à des cellules souches. Comprendre cette voie mécanique de l’évolution tumorale pourrait ouvrir de nouvelles pistes pour bloquer les rechutes et les métastases.
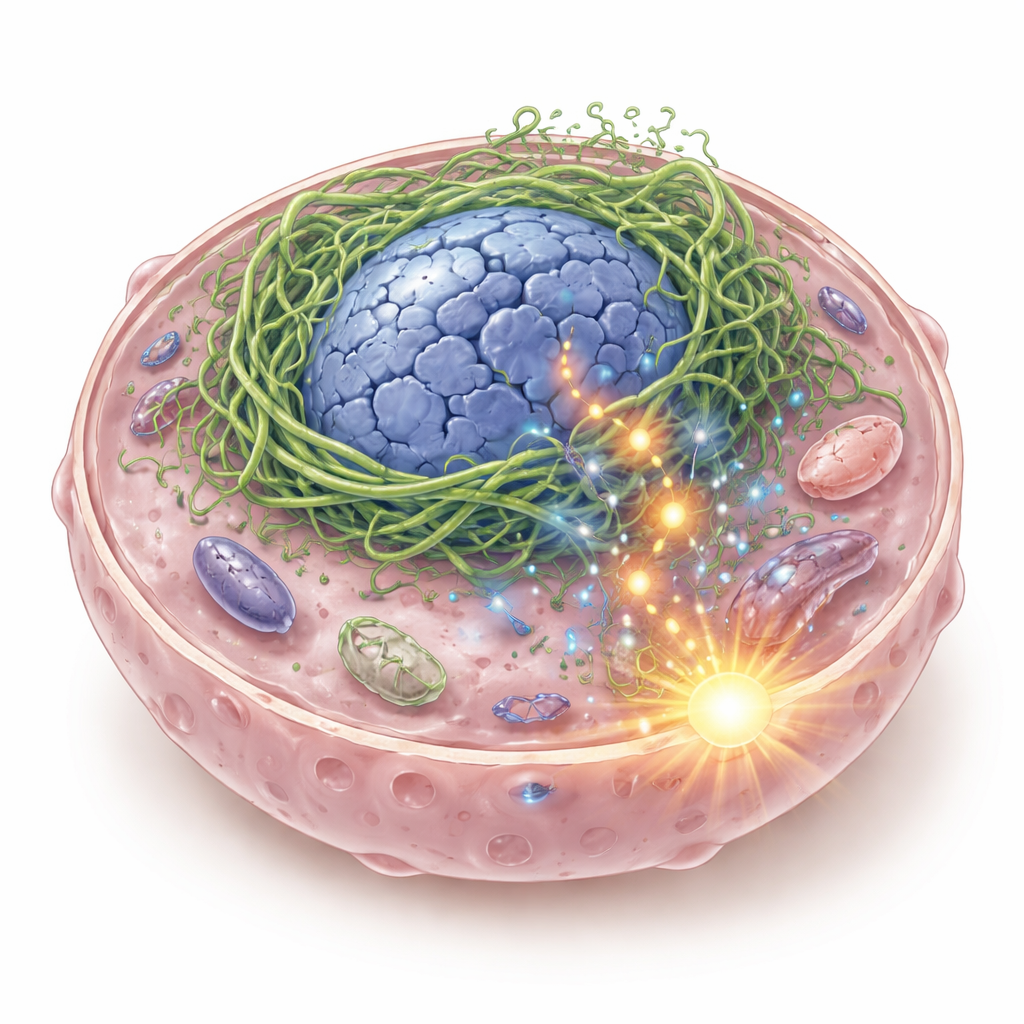
Un échafaudage intérieur brisé aux conséquences dangereuses
À l’intérieur de chaque cellule se trouve un échafaudage flexible constitué de filaments protéiques qui maintient la cellule et son noyau en forme et l’aide à percevoir les forces physiques. Les auteurs se sont intéressés aux kératines, une famille de protéines d’échafaudage courantes dans les tissus épithéliaux, notamment ceux tapissant la bouche et la gorge. Dans certains carcinomes épidermoïdes de la tête et du cou, ils ont découvert une kératine hybride appelée K6-K14/V5, formée par la fusion de deux gènes de kératine. Lorsque cette protéine de fusion est exprimée dans les cellules cancéreuses, elle ne forme pas un réseau de soutien régulier. Au contraire, elle s’agglutine étroitement autour du noyau, le déformant en structures creuses et difformes et provoquant des cassures d’ADN. Des fragments d’ADN fuient dans le cytoplasme, où ils sont détectés par un système de surveillance immunitaire nommé cGAS–STING, normalement activé en présence d’ADN viral.
De la pression sur la survie cellulaire à une survie masquée
L’effet immédiat de ces dommages nucléaires est préjudiciable pour les cellules tumorales : leur prolifération ralentit et nombre d’entre elles meurent. Toutefois, une fraction parvient à survivre. Ces survivantes sont fortement influencées par leur environnement physique. Sur des boîtes de plastique plates standard, elles finissent par disparaître, mais lorsqu’elles sont cultivées dans un gel de collagène souple — plus proche de la consistance des tissus réels — elles persistent et réapparaissent comme une nouvelle population, appelée cellules 3D-V5. Les analyses d’activité génique montrent que ces cellules réagissent à l’alarme permanente de dommages à l’ADN en activant l’autophagie, un programme d’auto-nettoyage qui recycle les éléments endommagés, en particulier les mitochondries déficientes. Cette réponse les aide à entrer dans un état de dormance à faible activité qui leur permet de supporter le stress plutôt que d’être éliminées.
Des cellules dormantes se reprogramment et se préparent à migrer
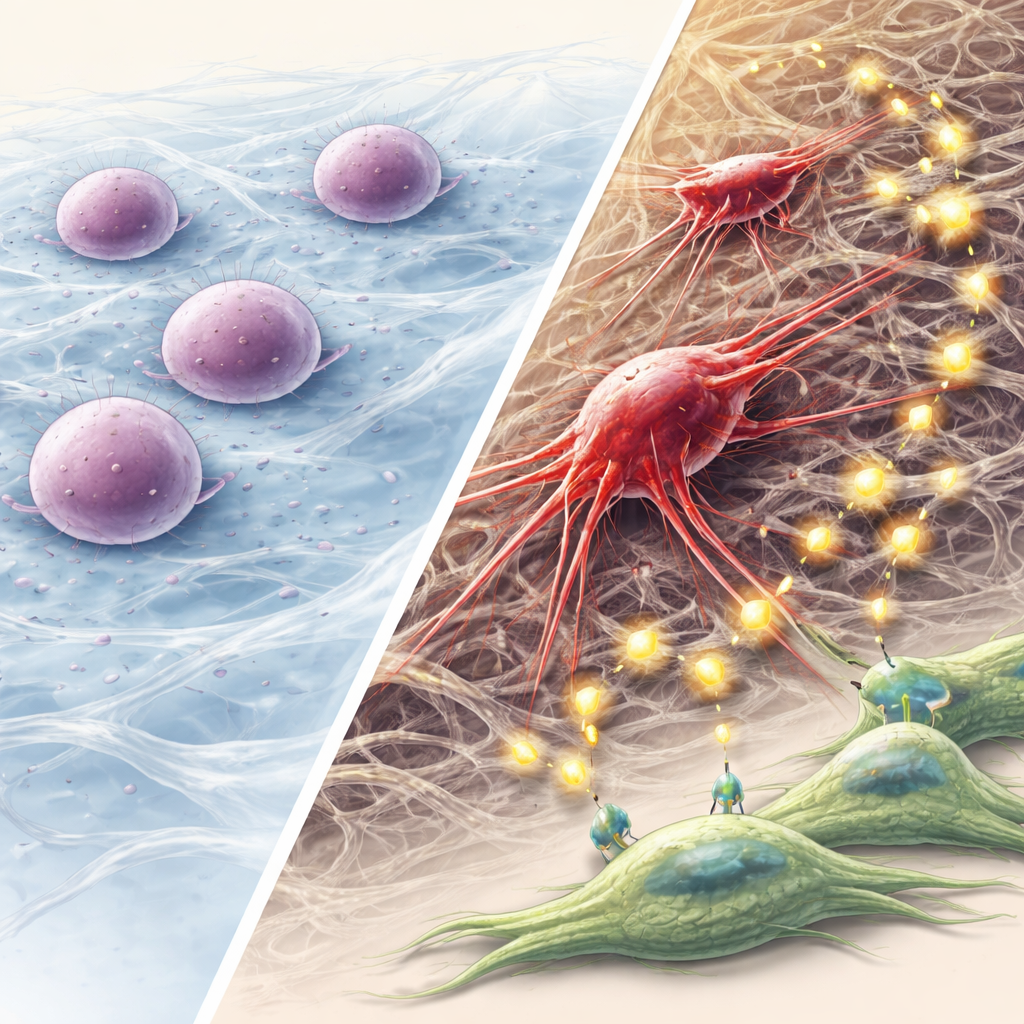
En état de dormance, ces cellules survivantes réécrivent discrètement leurs programmes internes. Elles modifient la composition de leurs kératines et adoptent une transition épithélio-mésenchymateuse « partielle » (pEMT) — une identité intermédiaire qui conserve certains traits épithéliaux tout en gagnant en souplesse et en motilité. Elles deviennent beaucoup plus aptes à former des sphères et à ensemencer de nouveaux agrégats cellulaires, un marqueur de la pluripotence tumorale. Avec le temps, leurs propriétés mécaniques se rétablissent : elles rigidifient à nouveau leurs noyaux, reconstruisent des filaments d’actine robustes et développent de longues protrusions qui sondent et saisissent la matrice environnante. Elles augmentent également l’expression d’enzymes appelées métalloprotéinases matricielles (MMP), qui dégradent la matrice extracellulaire et ouvrent des voies pour l’invasion.
Dialoguer avec les cellules voisines pour construire une niche favorable
Ces cellules cancéreuses reprogrammées n’agissent pas seules. L’équipe a observé que les cellules 3D-V5 libèrent un grand nombre de petits colis appelés vésicules extracellulaires dans leur environnement. Lorsque ces vésicules exposent des fibroblastes buccaux voisins — des cellules du tissu conjonctif — les fibroblastes modifient leur propre activité génique, devenant davantage des fibroblastes associés à la tumeur qui soutiennent la croissance tumorale. Beaucoup des signaux échangés tournent autour de l’axe FGF–FGFR, une famille de facteurs de croissance et de leurs récepteurs connue pour stimuler la prolifération, la plasticité et la résistance. En culture et dans des tumeurs de souris, le blocage de l’activité FGFR a réduit cet avantage de croissance. Chez l’animal, les tumeurs issues de cellules 3D-V5 étaient peu différenciées, plus invasives, riches en marqueurs de cellules souches et plus enclines à se propager au-delà du site d’injection.
Pourquoi cette voie mécanique vers un cancer agressif importe
Ce travail propose un modèle en étapes : une fusion de kératine perturbe l’échafaudage interne de la cellule, écrase le noyau et déclenche une alarme de dommages à l’ADN ; l’autophagie permet ensuite à quelques cellules d’entrer en dormance plutôt que de mourir ; avec le temps, ces survivantes réorganisent leur cytosquelette, acquièrent des traits de type souches et invasifs, et remodelent leur environnement via des vésicules et le signal FGF. Pour le grand public, le message clé est que les forces physiques et les protéines structurelles à l’intérieur des cellules peuvent être tout aussi déterminantes que les gènes et les molécules chimiques dans l’évolution du cancer. Cibler cette voie mécanique stress–autophagie–FGF, en particulier dans les cancers de la tête et du cou porteurs de fusions de kératine, pourrait offrir de nouvelles stratégies pour empêcher les cellules tumorales dormantes de se réveiller et de se propager.
Citation: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Mots-clés: pluripotence du cancer, cytosquelette cellulaire, dormance tumorale, cancer de la tête et du cou, mécanotransduction