Clear Sky Science · fr
Le rôle de la déméthylase des histones PHF2 en tant que suppresseur de tumeur dans le carcinome hépatocellulaire via la régulation de SRXN1
Pourquoi cette étude sur le cancer du foie est importante
Le cancer du foie est l’un des cancers les plus meurtriers dans le monde, et les traitements actuels n’allongent la vie que modestement pour de nombreux patients. Cette étude pose une question différente : au lieu de viser les gènes classiquement impliqués dans le cancer, peut-on exploiter la manière dont l’ADN est emballé et marqué chimiquement dans les cellules hépatiques pour découvrir des options thérapeutiques nouvelles et plus précises ? Les chercheurs se concentrent sur une protéine peu étudiée appelée PHF2 et révèlent comment elle pourrait contribuer à empêcher les cellules du foie de devenir cancéreuses.
À la recherche des faiblesses du système de contrôle du cancer
Le cancer n’est pas seulement causé par des gènes endommagés ; il est également alimenté par des contrôles « épigénétiques » défaillants — les marques chimiques et complexes protéiques qui déterminent quels gènes sont activés ou réprimés. Dans le carcinome hépatocellulaire, la forme la plus courante de cancer du foie, de nombreux régulateurs de ce type sont perturbés. L’équipe a testé systématiquement 497 régulateurs épigénétiques dans six lignées cellulaires du foie, en utilisant des outils d’ARN pour réduire temporairement chacun d’eux un par un, puis en mesurant la survie des cellules cancéreuses. Ce vaste criblage visait à révéler sur quels régulateurs les cancers s’appuient pour croître, et lesquels jouent normalement un rôle de frein à la formation tumorale.
Découvrir de nouveaux promoteurs et protecteurs du cancer
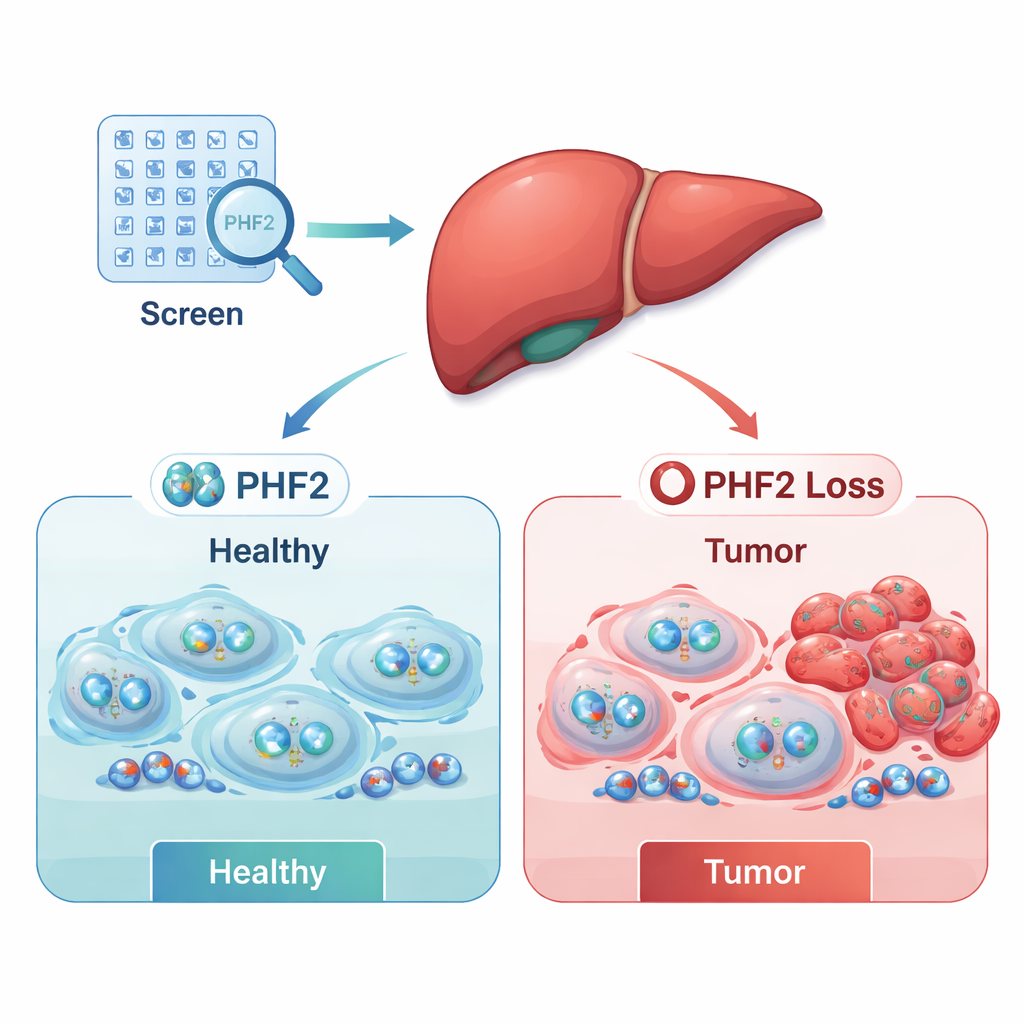
Le criblage a mis en évidence deux grands groupes : des « accélérateurs » potentiels du cancer (oncogènes) dont la perte nuit à la survie des cellules cancéreuses, et des « freins » potentiels (suppresseurs de tumeur) dont la perte favorise la croissance des cellules cancéreuses. En combinant leurs données de laboratoire avec de larges jeux de données publics de patients, les chercheurs ont réduit la liste à quelques candidats cliniquement pertinents. Deux régulateurs, SUPT7L et SMARCC1, avaient tendance à être plus actifs dans les tumeurs et étaient associés à une survie plus faible. En revanche, un régulateur — PHF2 — était souvent moins actif dans les tumeurs hépatiques, et les patients dont les tumeurs conservaient des niveaux plus élevés de PHF2 vivaient généralement plus longtemps. Ces schémas suggèrent que PHF2 pourrait agir comme un suppresseur de tumeur dans le cancer du foie humain.
Comment la perte de PHF2 modifie les cellules du cancer du foie
Pour examiner plus en profondeur le rôle de PHF2, l’équipe a conçu des cellules de cancer du foie produisant de façon stable moins de cette protéine et a suivi leur comportement au fil du temps. Les cellules avec une PHF2 réduite proliféraient plus rapidement et présentaient des niveaux plus élevés de Ki-67, un marqueur de division cellulaire active, indiquant que PHF2 aide normalement à freiner la prolifération. Ces effets étaient les plus marqués dans des lignées de cancer du foie déjà agressives, ce qui suggère que la simple perte de PHF2 ne suffit peut‑être pas à initier le cancer, mais peut accélérer la croissance des cellules malignes une fois que les tumeurs se sont formées.
Un lien surprenant avec les défenses contre le stress cellulaire
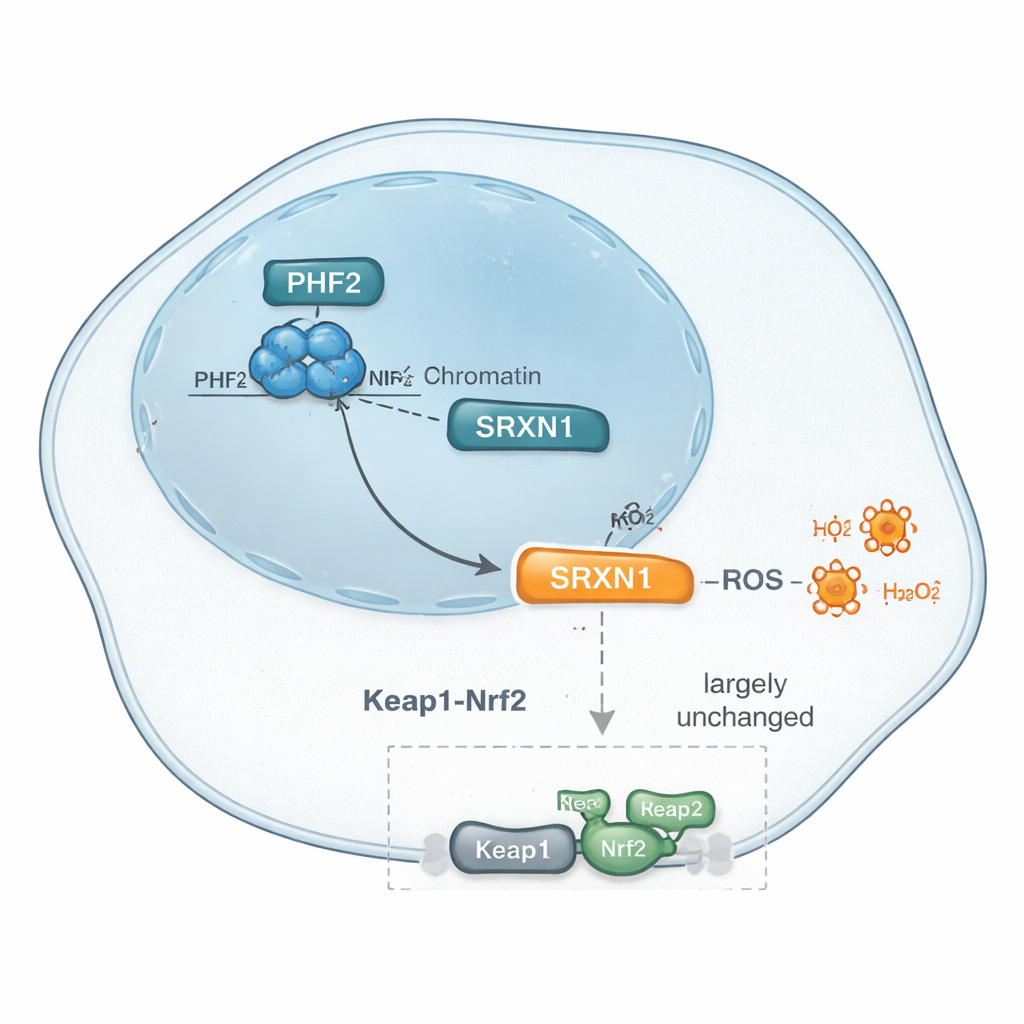
Puis, les chercheurs ont utilisé des méthodes modernes de profilage protéique pour inventorier des milliers de protéines dont les niveaux changeaient lorsque PHF2 était réduit. Parmi de nombreux changements subtils, un motif s’est distingué : les niveaux d’une protéine protectrice contre le stress appelée SRXN1 diminuaient systématiquement lors de la perte de PHF2. SRXN1 aide les cellules à gérer les espèces réactives de l’oxygène — des sous-produits chimiquement réactifs qui peuvent endommager l’ADN et les protéines mais qui peuvent aussi pousser les cellules cancéreuses à s’adapter. Les données suggèrent que PHF2 contribue au maintien des niveaux de SRXN1, et que l’altération de cet équilibre pourrait influencer la façon dont les cellules du foie cancéreuses répondent au stress interne et, ultimement, la vitesse à laquelle elles croissent.
Agir en dehors d’une voie de stress bien connue
SRXN1 est généralement contrôlé par un commutateur maître de la réponse au stress appelé Nrf2, qui active de nombreux gènes antioxydants lorsque les cellules subissent un stress oxydatif. Comme SRXN1 diminuait lorsque PHF2 était supprimée, l’équipe a demandé si PHF2 agissait simplement via cette voie Nrf2 bien caractérisée. Ils ont examiné des gènes et protéines clés liés à Nrf2, traité les cellules avec des médicaments qui activent Nrf2 en bloquant son inhibiteur Keap1, et utilisé des outils génétiques pour réduire directement Keap1. À travers ces tests, la réponse des cellules déficientes en PHF2 ressemblait beaucoup à celle des cellules normales, et des analyses plus larges de voies et de facteurs de transcription n’ont pas mis Nrf2 en avant comme acteur principal. Au lieu de cela, d’autres facteurs, dont ZNF384 et Nrf1 — tous deux déjà liés au cancer du foie — sont apparus comme candidats. Ensemble, les preuves suggèrent que le contrôle par PHF2 de SRXN1 et des réponses antioxydantes peut contourner la signalisation Nrf2 classique, laissant entrevoir une voie distincte de régulation du stress dans ces tumeurs.
Ce que cela pourrait signifier pour les traitements futurs
Pour un non‑spécialiste, l’idée essentielle est que cette étude identifie PHF2 comme un facteur protecteur prometteur dans le cancer du foie : lorsque PHF2 est présent et actif, les cellules tumorales croissent plus lentement ; lorsqu’il est diminué, elles gagnent un avantage de prolifération et modifient leur gestion du stress cellulaire. Comme PHF2 lui‑même peut être difficile à cibler directement avec des petites molécules classiques, les auteurs évoquent des stratégies émergentes telles que des thérapies à base d’ARN ou des médicaments qui renforcent l’activité de PHF2 via des partenaires de signalisation en amont. Ils soulignent aussi que les effets de PHF2 dépendent du contexte — son impact peut varier selon d’autres mutations comme le statut de p53 — de sorte que toute thérapie future nécessiterait probablement une sélection rigoureuse des patients. Dans l’ensemble, ce travail affine notre compréhension de la façon dont les régulateurs épigénétiques façonnent le comportement du cancer du foie et ouvre de nouvelles pistes pour concevoir des traitements qui restaurent ou imitent l’influence suppresseuse de tumeur de PHF2.
Citation: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Mots-clés: carcinome hépatocellulaire, régulation épigénétique, PHF2, SRXN1, thérapie du cancer du foie