Clear Sky Science · fr
La sécrétion d’OPN médiée par Rab37 enrichit les macrophages SPP1+ via un signal autocrine–paracrine pour favoriser la progression tumorale pulmonaire
Comment les cellules immunitaires peuvent secrètement aider les tumeurs pulmonaires à croître
Le cancer du poumon ne se développe pas isolément. Il prospère au sein d’un voisinage animé d’autres cellules immunitaires et de tissus conjonctifs, transformant parfois des prétendus défenseurs en alliés. Cette étude révèle comment une petite protéine de trafic à l’intérieur des cellules immunitaires, baptisée Rab37, aide certains macrophages à sécréter une molécule appelée ostéopontine (OPN), créant un environnement favorable à la tumeur qui rend le cancer du poumon plus agressif et plus difficile à traiter.
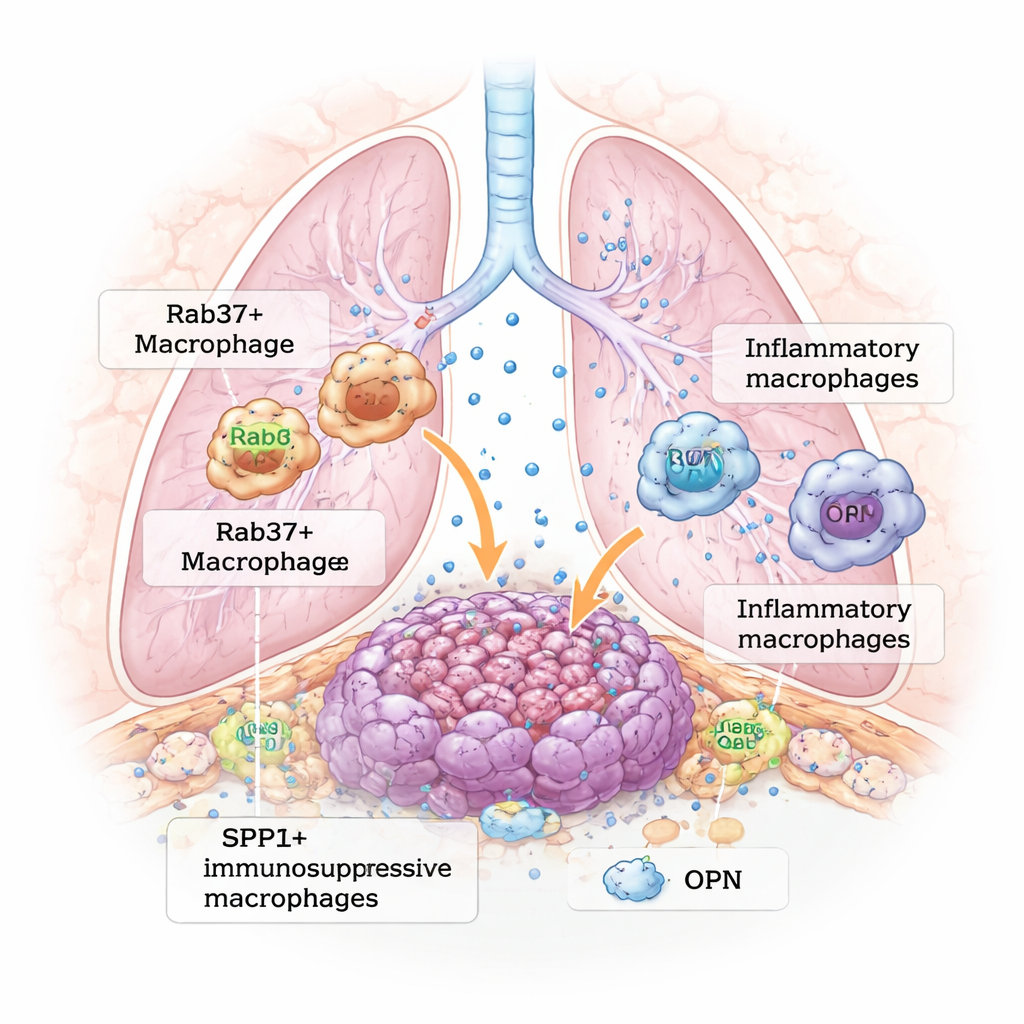
Un quartier très actif à l’intérieur d’une tumeur pulmonaire
Les recherches modernes sur le cancer montrent que les tumeurs ressemblent davantage à des écosystèmes complexes qu’à de simples amas de cellules délinquantes. Autour des tumeurs pulmonaires, cellules immunitaires, vaisseaux sanguins et cellules de soutien envoient sans cesse des messages chimiques les uns aux autres. Parmi elles, les macrophages — des cellules du système immunitaire qui éliminent normalement infections et débris — s’installent souvent dans les tumeurs sous la forme de « macrophages associés à la tumeur ». Au lieu d’attaquer le cancer, beaucoup de ces cellules prennent un rôle nourricier, calmant les attaques immunitaires et aidant la tumeur à croître et à se disséminer. La grande question abordée par cet article est : qu’est-ce qui pousse les macrophages vers cet état nuisible et pro‑tumoral ?
Deux types de macrophages : aides et entraves
Les chercheurs ont utilisé le séquençage ARN unicellulaire, une technologie qui lit l’activité de milliers de gènes dans des cellules individuelles, pour cartographier les cellules immunitaires à l’intérieur de tumeurs pulmonaires de souris. Ils ont comparé des souris normales et des souris dépourvues de Rab37. Dans les tumeurs des souris normales, ils ont trouvé de nombreux macrophages riches en expression du gène SPP1, qui code pour la protéine ostéopontine (OPN). Ces macrophages SPP1+ formaient un groupe immunosuppresseur et pro‑tumoral. En revanche, les tumeurs des souris knock-out pour Rab37 comptaient moins de macrophages SPP1+ et davantage de macrophages exprimant un autre gène, THBS1, associé à une réponse plus inflammatoire et potentiellement limitante pour la tumeur. Dans des échantillons humains de cancer du poumon, les patients dont les tumeurs contenaient de nombreux macrophages positifs pour CD163, Rab37 et OPN avaient plus de risques de rechute et une survie plus mauvaise, ce qui suggère que ce type précis de macrophage est cliniquement dangereux.
La protéine de transport qui booste la sécrétion d’OPN
Rab37 appartient à une famille de protéines qui contrôlent la façon dont les cellules emballent et libèrent des molécules. L’équipe a montré que Rab37 charge l’OPN dans de petites vésicules à l’intérieur des macrophages et en pilote la libération à l’extérieur. Lorsque les macrophages possédaient un Rab37 fonctionnel, ils sécrétaient beaucoup plus d’OPN, surtout exposés à des signaux provenant de cellules de cancer du poumon. Lorsque Rab37 était éliminé ou son activité bloquée, la libération d’OPN chutait fortement. L’étude a également mis au jour une boucle de rétroaction : l’OPN sécrétée active une protéine de signalisation appelée STAT3 dans les macrophages, qui augmente alors l’activité du gène SPP1 et pousse les macrophages davantage vers un état de type M2, promoteur de tumeur. Cette boucle verrouille les cellules dans une identité pro‑tumorale, les incitant à produire encore plus d’OPN.
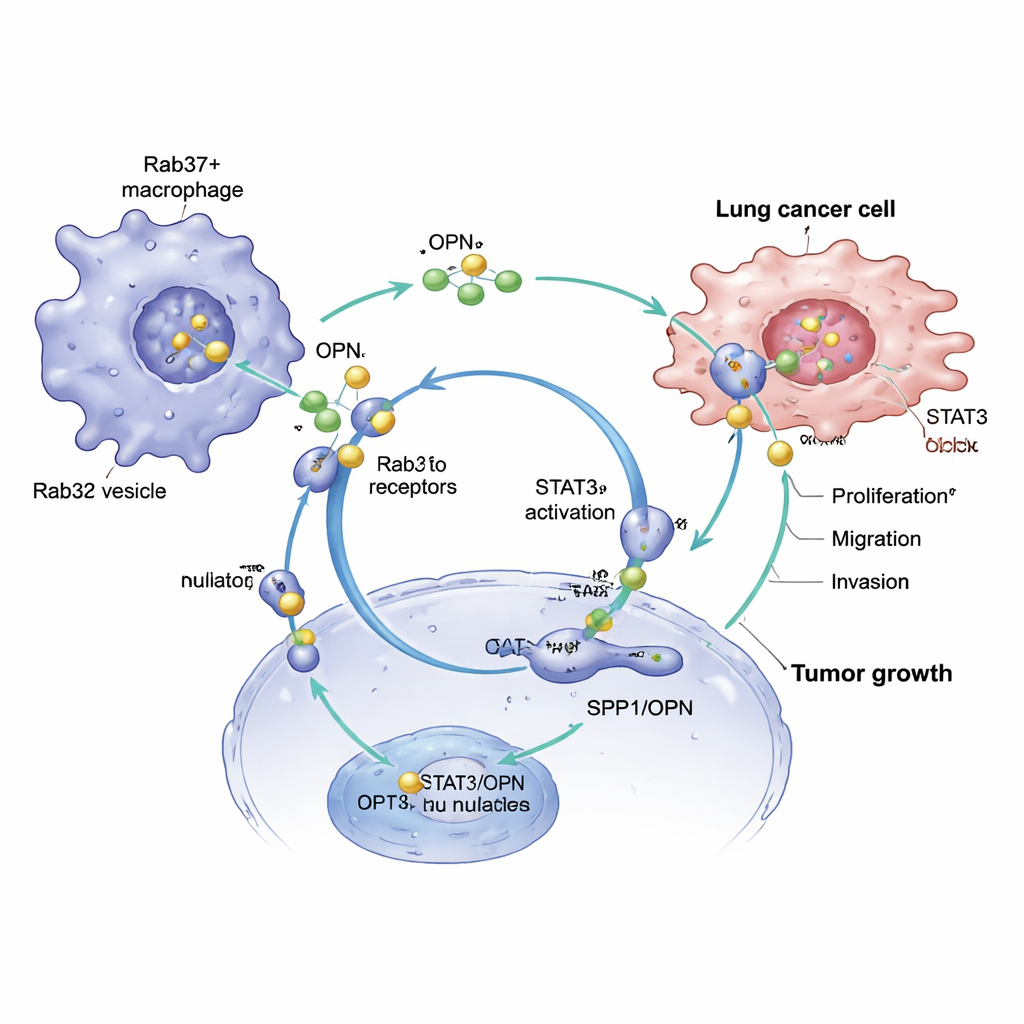
Des signaux immunitaires à l’accélération tumorale
L’OPN n’agit pas seulement sur les macrophages — elle communique aussi directement avec les cellules cancéreuses. Lorsque des cellules de cancer du poumon ont été baignées dans du liquide prélevé chez des macrophages positifs pour Rab37, elles ont proliféré plus vite et gagné en mobilité et en capacité invasive. Bloquer l’OPN dans ce milieu réduisait ces effets, tandis que réintroduire de l’OPN purifiée les restaurait. Le même circuit Rab37–OPN–STAT3 qui reprogramme les macrophages active aussi des voies de croissance et de survie à l’intérieur des cellules cancéreuses pulmonaires, favorisant prolifération, migration et invasion des tissus environnants. Ainsi, une seule molécule sécrétée contribue à la fois à remodeler le comportement immunitaire et à accélérer la progression tumorale.
Transformer une découverte en opportunité thérapeutique
Pour les non-spécialistes, le message principal est que certaines cellules immunitaires au sein des tumeurs pulmonaires deviennent des « agents doubles », et que Rab37 est un coordinateur clé de leur trahison. En aidant les macrophages à sécréter l’OPN et à maintenir une boucle de rétroaction pilotée par l’OPN, Rab37 favorise un environnement silencieux et tolérant où les tumeurs prospèrent et se propagent. Les patients dont les tumeurs sont chargées en macrophages Rab37+/OPN+ ont un pronostic plus mauvais, ce qui signifie que ce type cellulaire pourrait servir d’indicateur d’alerte et de cible thérapeutique. Des thérapies qui bloquent l’OPN, interfèrent avec STAT3 ou perturbent la fonction de trafic de Rab37 pourraient aider à reconvertir les macrophages vers un rôle anti‑tumoral, rendant le cancer du poumon plus vulnérable aux traitements existants, y compris l’immunothérapie.
Citation: Yang, YE., Lin, YA., Ling, LL. et al. Rab37-mediated OPN secretion enriches SPP1+ macrophages through autocrine–paracrine signaling to drive lung tumor progression. Oncogenesis 15, 4 (2026). https://doi.org/10.1038/s41389-026-00596-3
Mots-clés: cancer du poumon, microenvironnement tumoral, macrophages, ostéopontine, signalisation STAT3