Clear Sky Science · fr
La dégradation médiée par TRIM21 de HILPDA surmonte la résistance à l’immunothérapie anti‑PD‑1 dans le cancer du sein en limitant la palmitoylation de PD‑L1
Pourquoi certaines immunothérapies contre le cancer cessent de fonctionner
Les médicaments qui libèrent le système immunitaire, comme les thérapies anti‑PD‑1, ont transformé le traitement de plusieurs cancers, y compris des formes agressives du cancer du sein. Pourtant, de nombreuses tumeurs ne répondent jamais ou finissent par développer des mécanismes d’échappement. Cette étude explore l’un de ces circuits d’échappement dans le cancer du sein triple‑négatif et montre comment reprogrammer le métabolisme lipidique tumoral — et un médicament repositionné appelé fénretinide — pourrait rouvrir la voie pour le système immunitaire lorsque l’immunothérapie standard échoue. 
Un auxiliaire caché qui protège les tumeurs
Les chercheurs se sont concentrés sur une protéine peu connue nommée HILPDA, auparavant associée à la gestion des lipides par les cellules en situation de stress. En comparant des tumeurs mammaires de souris restées sensibles à l’anti‑PD‑1 avec des tumeurs devenues résistantes, ils ont constaté des niveaux beaucoup plus élevés de HILPDA dans les cancers résistants. Des analyses de larges bases de données de patients et d’échantillons tumoraux provenant de femmes atteintes d’un cancer du sein ont confirmé que HILPDA est plus abondant dans les tumeurs que dans le tissu mammaire normal, en particulier dans la maladie triple‑négative, et que les patientes dont les tumeurs expriment davantage de HILPDA tendent à avoir un pronostic plus défavorable. Les tumeurs de personnes n’ayant pas bénéficié des traitements bloquant PD‑1 présentaient également plus de HILPDA, reliant ainsi cette protéine directement à l’échec thérapeutique.
Comment les tumeurs retournent le paysage immunitaire contre nous
Pour comprendre ce que fait réellement HILPDA dans les tumeurs, l’équipe a modifié des cellules de cancer du sein pour qu’elles surproduisent ou manquent de la protéine, puis les a cultivées avec des cellules immunitaires humaines ou chez la souris. Lorsque HILPDA était élevé, les tumeurs recrutaient davantage de lymphocytes T régulateurs, de cellules suppressives myéloïdes d’origine tumorale et de macrophages de type M2 — des types cellulaires qui atténuent la réponse immunitaire et aident les cancers à se dissimuler. Parallèlement, le nombre et la vigueur des lymphocytes T CD8 cytotoxiques et des cellules NK diminuaient, ainsi que leur capacité à libérer des molécules toxiques et des signaux inflammatoires. L’inhibition de HILPDA inversait ce tableau : les tumeurs hébergeaient moins de cellules suppressives, plus de cellules tueuses actives, une croissance plus lente et moins de métastases. De façon cruciale, lorsque des animaux porteuses de tumeurs à faible HILPDA recevaient une thérapie anti‑PD‑1, leurs tumeurs régressaient davantage et les souris vivaient plus longtemps, démontrant que HILPDA contrôle l’efficacité de l’immunothérapie.
Synthèse lipidique, armure moléculaire et échappement immunitaire
En approfondissant, les scientifiques ont découvert comment HILPDA reconfigure le métabolisme tumoral pour renforcer les défenses immunitaires. À l’intérieur des cellules cancéreuses, HILPDA se lie à une protéine chaperonne nommée HSP90 pour stabiliser un facteur de transcription, KLF5, qui stimule la production de lipides. Ce trio augmente la synthèse d’acides gras, en particulier le palmitate, et remplit les cellules tumorales de gouttelettes lipidiques. L’un de ces lipides est ensuite attaché à PD‑L1, la protéine de point de contrôle située à la surface tumorale qui envoie un signal « ne pas attaquer » aux cellules immunitaires. L’équipe a montré que l’ajout de palmitate à un site spécifique de PD‑L1 agit comme une colle moléculaire : il aide PD‑L1 à rester stable dans la membrane cellulaire et empêche sa dégradation. La mutation de ce site d’attachement unique prive PD‑L1 de sa stabilité et affaiblit sa capacité à protéger les cellules cancéreuses, même en présence d’un excès de HILPDA. Autrement dit, la production lipidique pilotée par HILPDA alimente une modification chimique de PD‑L1 qui transforme le bouclier immunitaire tumoral d’une protection fragile en une armure renforcée.
Le frein intégré qui peut être activé
Tout accélérateur a besoin d’un frein, et ici le frein est une autre protéine appelée TRIM21. Les auteurs ont découvert que TRIM21 reconnaît HILPDA et la marque par des « étiquettes » moléculaires qui l’acheminent vers les mécanismes de dégradation cellulaire. Dans les tumeurs mammaires de patientes, les niveaux de TRIM21 étaient généralement faibles lorsque HILPDA était élevé, et un faible TRIM21 était associé à un mauvais pronostic, suggérant que ce système de freinage naturel est souvent affaibli dans le cancer. L’équipe a ensuite recherché des médicaments capables de renforcer TRIM21 et a identifié le fénretinide, un rétinoïde déjà testé chez l’humain. Dans des modèles cellulaires et animaux du cancer du sein triple‑négatif, le fénretinide a stimulé l’activité de TRIM21, accéléré la dégradation de HILPDA, réduit la synthèse lipidique et la modification protectrice de PD‑L1, et ralenti la croissance et la dissémination tumorales. Plus frappant encore, l’association du fénretinide avec une thérapie anti‑PD‑1 a rendu les tumeurs plus vulnérables à l’attaque immunitaire, augmentant les lymphocytes T cytotoxiques et les cellules NK tout en réduisant les cellules suppressives dans le microenvironnement tumoral. 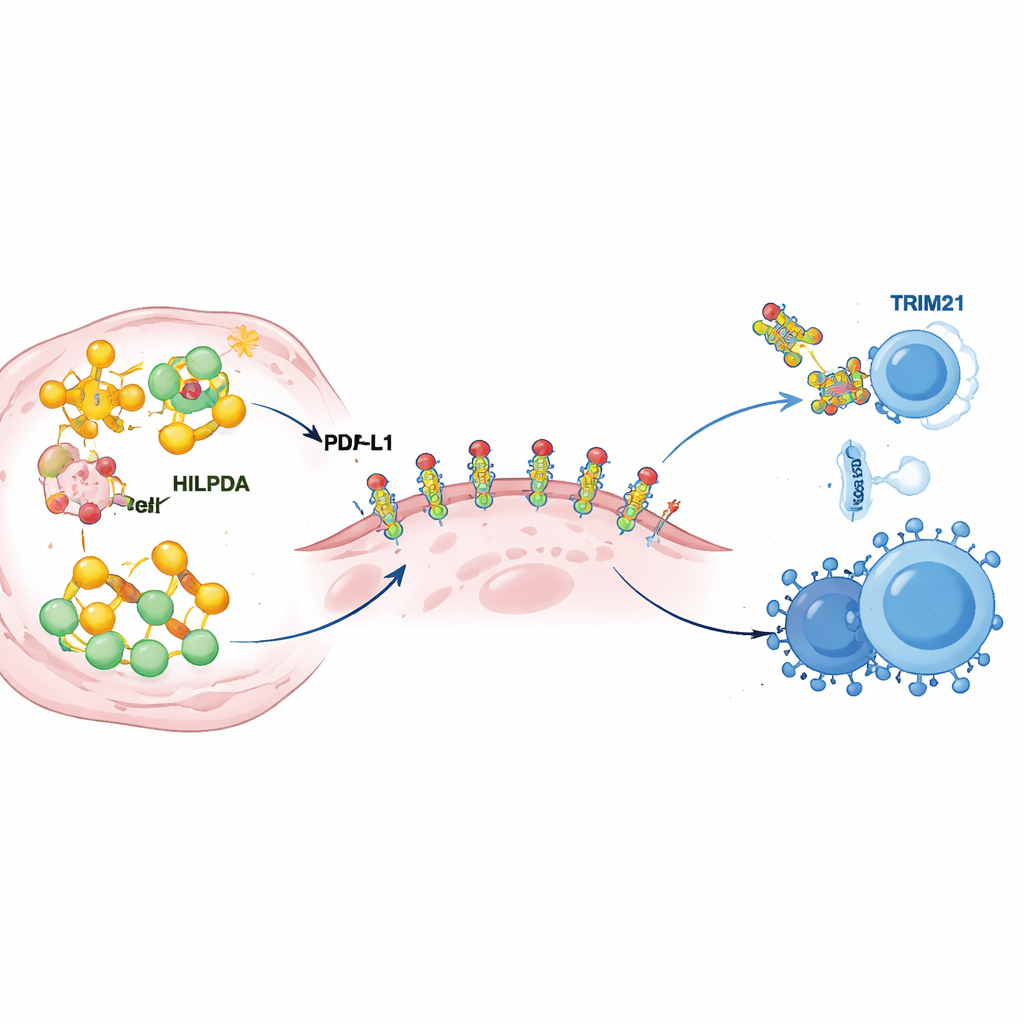
Ce que cela signifie pour les soins du cancer à venir
Ce travail dévoile une chaîne d’événements dans laquelle des cellules mammaires cancéreuses stressées augmentent HILPDA, intensifient la production de lipides et renforcent chimiquement PD‑L1 à leur surface, leur permettant de continuer à supprimer les cellules immunitaires malgré les traitements bloquant PD‑1. TRIM21 agit comme un garde‑fou interne capable de démanteler HILPDA, mais il est souvent trop faible dans les tumeurs. En montrant que le fénretinide peut réactiver ce garde‑fou, l’étude propose une approche pratique pour combiner un médicament métabolique avec l’immunothérapie existante afin de surmonter la résistance. Si ces résultats sont confirmés en essais cliniques, cibler l’axe TRIM21–HILPDA–PD‑L1 pourrait offrir aux patientes atteintes d’un cancer du sein triple‑négatif difficile à traiter une seconde chance de bénéficier des traitements à base d’immunité.
Citation: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Mots-clés: cancer du sein triple‑négatif, résistance à l’immunothérapie, palmitoylation de PD‑L1, métabolisme lipidique tumoral, fénretinide