Clear Sky Science · fr
La céréblon (CRBN) inhibe les métastases du cancer de la prostate en régulant négativement la 6-phosphogluconate déshydrogénase (6PGD)
Pourquoi cette recherche est importante
Lorsque le cancer de la prostate se propage de la prostate vers d’autres organes, il devient beaucoup plus difficile à traiter et est souvent mortel. Cette étude révèle comment une protéine de « contrôle qualité » intracellulaire peu connue, la céréblon (CRBN), contribue à empêcher la dissémination du cancer de la prostate en démantelant une enzyme métabolique qui alimente les comportements agressifs. Comprendre ce système de frein intégré suggère de nouvelles approches pour ralentir ou stopper les métastases, en particulier dans les formes difficiles à traiter de la maladie.
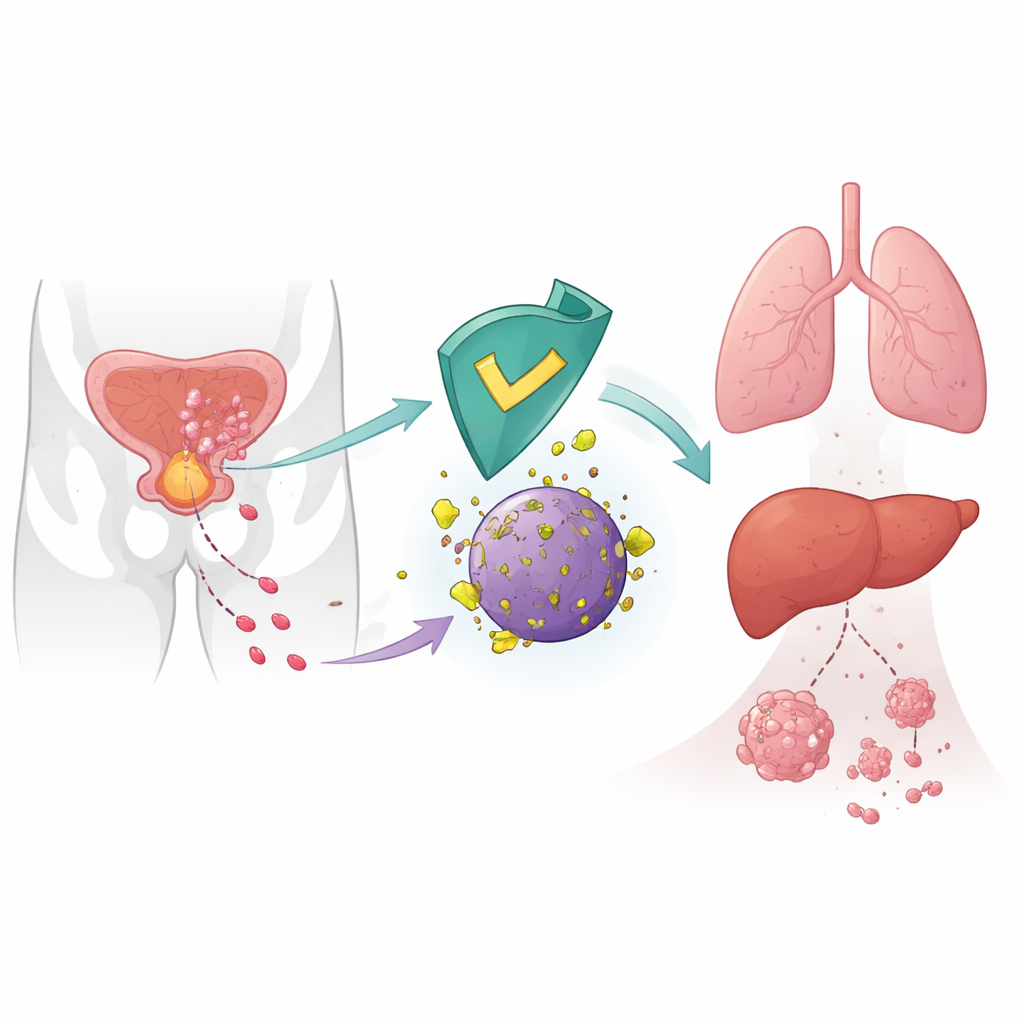
Un frein interne à la propagation du cancer
Les cellules cancéreuses ne se propagent pas au hasard ; elles reconfigurent leur machinerie interne pour se déplacer, envahir et coloniser des organes distants. Les auteurs se sont concentrés sur CRBN, une protéine surtout connue comme cible de médicaments tels que la thalidomide utilisés dans les cancers hématologiques. Dans les cellules saines, CRBN fait partie d’une unité moléculaire d’élimination qui marque certaines protéines pour destruction. Des travaux antérieurs laissaient entendre que de faibles niveaux de CRBN dans les tumeurs étaient associés à de mauvais pronostics, mais son rôle direct dans les métastases restait flou. Ici, les chercheurs montrent que CRBN agit comme un suppresseur naturel de la dissémination du cancer de la prostate en ciblant une enzyme métabolique appelée 6-phosphogluconate déshydrogénase (6PGD) pour sa dégradation.
Un moteur métabolique détourné par le cancer
La 6PGD appartient à une voie métabolique connue sous le nom de voie oxydative des pentoses phosphate, qui aide les cellules à générer du NADPH, une molécule fournissant à la fois des éléments de construction et une capacité antioxydante. De nombreuses tumeurs suractivent cette voie pour croître plus vite et tolérer le stress. L’équipe a constaté que les prélèvements de cancer de la prostate chez des patients présentent en général moins de CRBN et davantage de 6PGD que les tissus prostatiques normaux, et que ce déséquilibre est particulièrement prononcé dans les formes agressives. Dans des lignées cellulaires de cancer de la prostate, l’inhibition de CRBN ou sa dégradation par un composé conçu à cet effet entraînait une augmentation des niveaux protéiques et de l’activité enzymatique de la 6PGD, augmentant le NADPH. Restaurer CRBN produisait l’effet inverse, réduisant 6PGD et le NADPH sans modifier le message génétique de la 6PGD, ce qui indique un contrôle au niveau protéique.
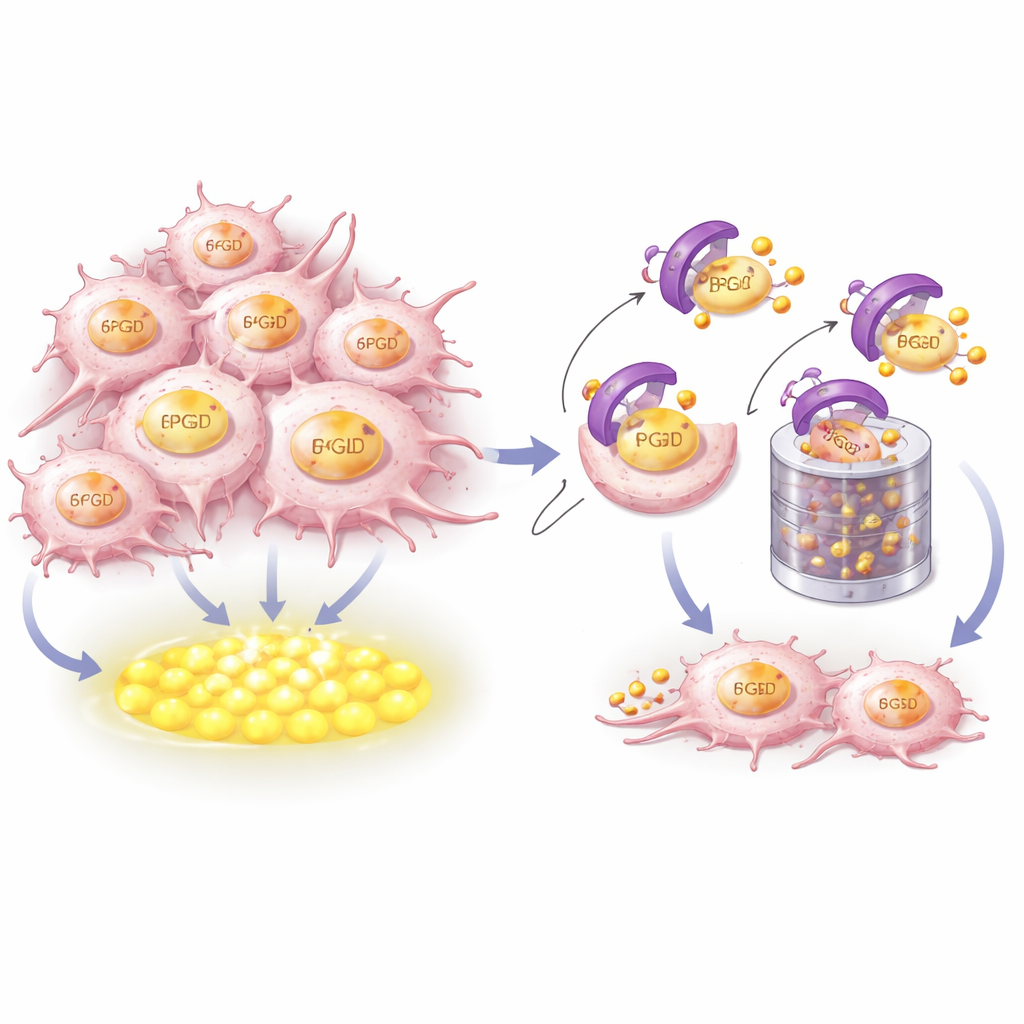
Comment CRBN reconnaît et détruit la source d’énergie
Pour comprendre comment CRBN contrôle la 6PGD, les chercheurs ont combiné modélisation structurale et expériences biochimiques. Ils ont montré que CRBN saisit physiquement un court segment hélicoïdal très conservé près de l’extrémité C-terminale de la 6PGD. Des acides aminés clés des deux protéines forment une interface d’accolement étroite. Lorsque ces points de contact sont modifiés, CRBN ne peut plus se lier à la 6PGD, lui attacher les petites étiquettes ubiquitine qui la marquent pour élimination, ni l’acheminer vers le destructeur cellulaire qu’est le protéasome. Il est notable que cette surface de reconnaissance est distincte de la poche où des médicaments immunomodulateurs se lient à CRBN, ce qui signifie que le contrôle de la 6PGD par CRBN fait partie de son rôle domestique natif et non d’un effet induit par un médicament.
Du métabolisme altéré aux cellules migrantes
Les conséquences de cette interaction moléculaire se traduisent au niveau du comportement cellulaire. Dans les cellules de cancer de la prostate dépourvues de CRBN, l’augmentation de la 6PGD et du NADPH s’accompagnait d’une mobilité et d’une invasion accrues à travers des barrières artificielles, signes caractéristiques d’un potentiel métastatique. Lorsque CRBN était surproduite, les cellules devenaient moins mobiles et moins invasives, même si leur vitesse de croissance ne changeait pas. Le profilage de l’activité génique a montré que CRBN augmentait les niveaux de CDH1, associé à des cellules épithéliales fortement compactes, et diminuait les niveaux de MMP1, lié à la dégradation tissulaire et à la migration. De manière importante, ces changements exigeaient une liaison directe CRBN–6PGD et pouvaient être inversés en bloquant l’activité enzymatique de la 6PGD, reliant ainsi les modifications métaboliques aux changements du comportement métastatique.
Preuves provenant de modèles animaux et d’autres cancers
L’équipe a testé ces idées chez la souris en injectant des cellules de cancer de la prostate dans la circulation sanguine ou la rate. Les cellules conçues pour produire un surplus de CRBN formaient beaucoup moins de nodules métastatiques dans le foie et les poumons que les cellules témoins, confirmant un rôle anti-métastatique in vivo. Des souris déficientes en CRBN présentaient des niveaux protéiques de 6PGD plus élevés dans plusieurs organes. Des schémas similaires ont été observés dans des lignées de glioblastome, de cancer du poumon et du rein : supprimer CRBN augmentait 6PGD et renforçait la mobilité et l’invasion cellulaires, tandis que l’inhibition génétique ou médicamenteuse de la 6PGD freinait ce comportement agressif. Ces observations suggèrent que le frein CRBN–6PGD sur les métastases n’est pas unique au cancer de la prostate.
Ce que cela pourrait signifier pour de futurs traitements
Globalement, l’étude propose que CRBN sert de gardien métabolique qui limite l’approvisionnement en énergie nécessaire pour que les cellules cancéreuses se détachent, migrent et ensemencent de nouvelles tumeurs. Lorsque CRBN est perdu ou faible, la 6PGD s’accumule, la production de NADPH augmente et les cellules sont plus susceptibles de subir des transformations favorisant les métastases. Pour les patients, cela ouvre deux pistes : mesurer les niveaux de CRBN et de 6PGD pourrait aider à identifier les tumeurs à haut risque métastatique, et des thérapies visant à renforcer la fonction de CRBN — ou à atténuer sélectivement la 6PGD dans les tumeurs pauvres en CRBN — pourraient offrir de nouvelles façons de ralentir ou prévenir la propagation du cancer de la prostate et d’autres cancers.
Citation: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Mots-clés: métastases du cancer de la prostate, métabolisme du cancer, céréblon, enzyme 6PGD, voie du NADPH