Clear Sky Science · fr
L1TD1 favorise la progression de l’adénocarcinome mucineux colorectal en renforçant la stabilité de l’ARNm d’ABCC3
Pourquoi ce cancer riche en mucus est important
Le cancer colorectal est une cause majeure de mortalité liée au cancer dans le monde. Parmi ses sous-types, l’adénocarcinome mucineux se distingue parce que ses tumeurs sont remplies d’un mucus épais qui représente plus de la moitié de la masse tumorale. Cette barrière visqueuse peut aider les cellules cancéreuses à se cacher de la chimiothérapie et des défenses de l’organisme. Cette étude pose une question fondamentale mais cruciale : qu’est-ce qui contrôle toute cette production de mucus, et peut-on l’inhiber pour ralentir le cancer et améliorer l’efficacité des traitements ?
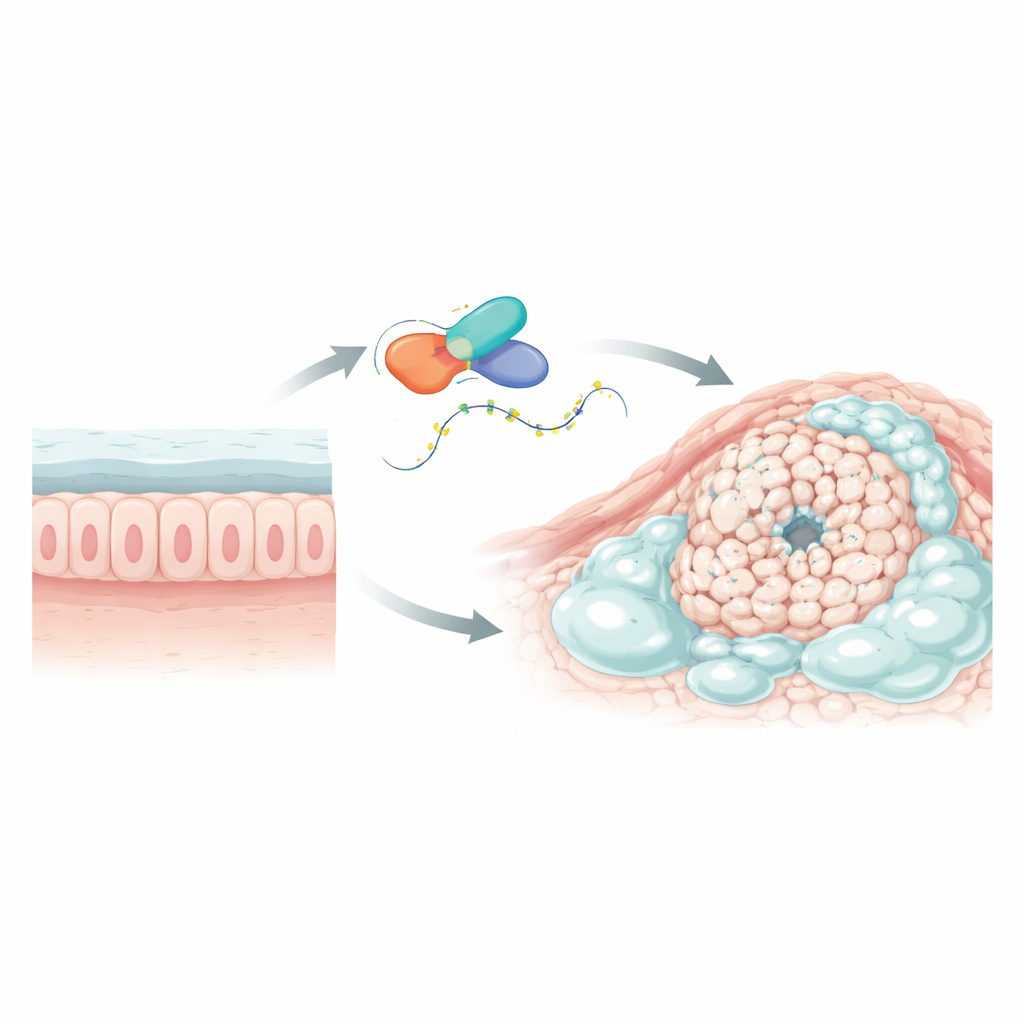
Identification d’un gène-clé problématique
Les chercheurs ont d’abord exploré de larges bases de données sur le cancer et des données de séquençage unicellulaire pour repérer des gènes dont l’expression diffère dans les tumeurs colorectal mucineuses par rapport aux cancers colorectaux ordinaires et aux tissus sains adjacents. Un gène, nommé L1TD1, est apparu de façon marquée. Il était fortement augmenté dans les tumeurs mucineuses mais pas dans les tumeurs classiques, et son expression était plus élevée dans le tissu tumoral que dans le côlon normal environnant. L1TD1 code pour une protéine qui se lie à l’ARN, la molécule qui transporte les messages génétiques de l’ADN vers la machinerie de synthèse protéique de la cellule. Comme les protéines liant l’ARN peuvent ajuster la durée de vie des messages et leur traduction, L1TD1 était un bon candidat pour agir comme régulateur maître dans ces cancers chargés de mucus.
Comment L1TD1 favorise la croissance et la dissémination cancéreuse
Pour tester la fonction de L1TD1, l’équipe a utilisé des lignées cellulaires de cancer du côlon et des modèles murins. Lorsque L1TD1 était surexprimé dans les cellules cancéreuses, celles-ci proliféraient plus vite, migraient plus facilement et envahissaient des barrières de type tissulaire de manière plus agressive. Réduire L1TD1 avait l’effet inverse, ralentissant la croissance et diminuant l’invasion. Chez des souris injectées avec des cellules à fort taux de L1TD1, les tumeurs étaient plus volumineuses et se propageaient plus souvent au foie et à la cavité abdominale. Les tumeurs exprimant davantage de L1TD1 avaient aussi tendance à être plus grosses, moins bien différenciées et à un stade plus avancé chez les patients, reliant ce gène à un comportement tumoral plus agressif en clinique.
Activation de la production de mucus et résistance aux médicaments
Le mucus lui-même s’est avéré central dans l’impact de L1TD1. Les cellules exprimant plus de L1TD1 produisaient des quantités accrues de protéines essentielles à la formation de mucus, en particulier MUC2 et MUC5AC, et présentaient des caractéristiques de cellules caliciformes, les cellules sécrétrices de mucus normales de l’intestin. Des cultures tridimensionnelles et des colorations tissulaires provenant de patients et de souris ont confirmé que des niveaux plus élevés de L1TD1 allaient de pair avec un mucus plus épais et plus abondant. Il est important de noter que ce mucus n’était pas un simple spectateur : lorsque les chercheurs ont réduit sélectivement MUC2, la prolifération accrue, l’invasion et la résistance à la chimiothérapie induites par L1TD1 ont en grande partie disparu. Les cellules riches en L1TD1 étaient plus difficiles à éliminer avec l’oxaliplatine, un médicament couramment utilisé, et les tumeurs portant ces cellules ont régressé moins sous traitement chez la souris, soulignant le rôle protecteur du mucus que L1TD1 contribue à former.
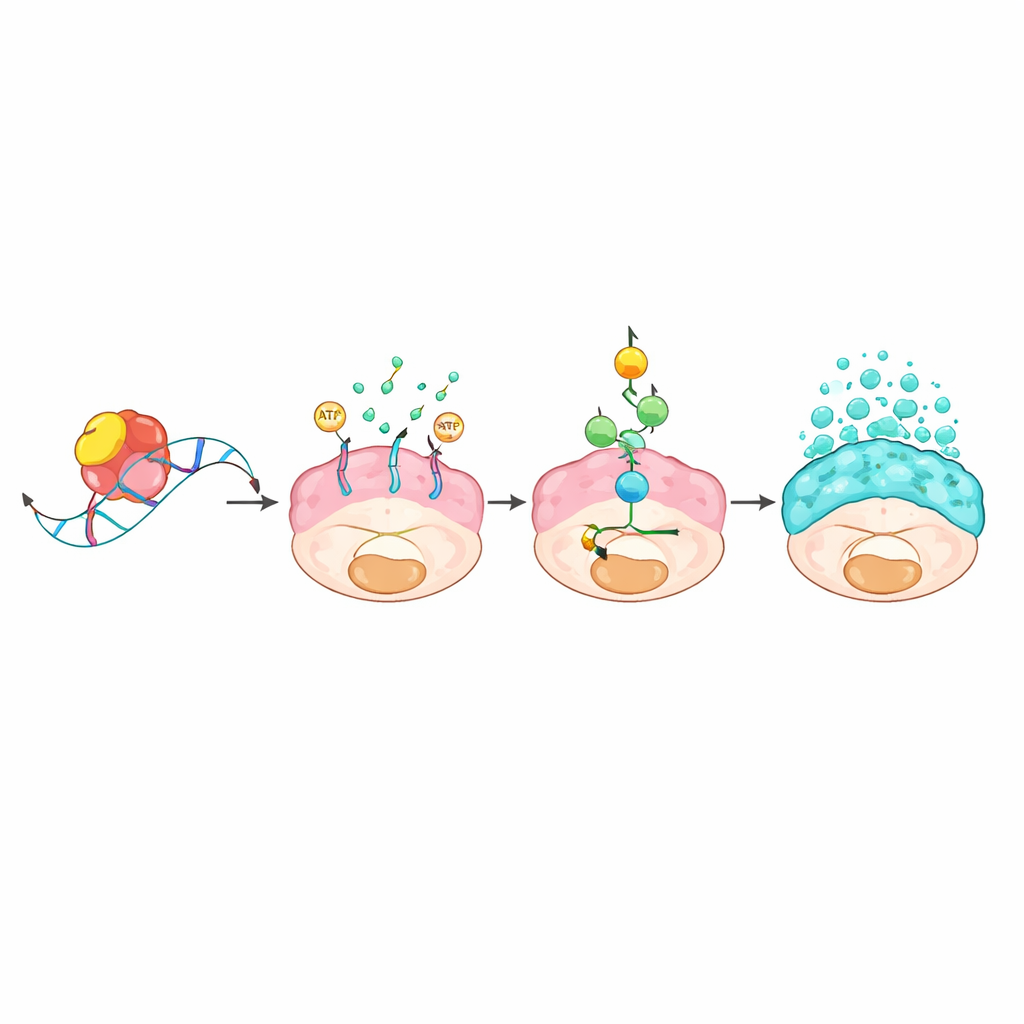
Une chaîne moléculaire reliant le contrôle de l’ARN aux inondations de mucus
L’équipe a ensuite cherché comment une protéine liant l’ARN pouvait provoquer de tels changements. En isolant les molécules d’ARN physiquement liées à L1TD1 et en comparant l’activité génique avec ou sans L1TD1, ils ont identifié un gène codeur d’un transporteur nommé ABCC3 comme cible principale. L1TD1 se lie à un court motif « GUGU » dans la région terminale de l’ARNm d’ABCC3, le stabilisant de sorte que la cellule produise davantage de la protéine ABCC3, connue sous le nom de MRP3. Ce transporteur, situé dans la membrane cellulaire, consomme de l’énergie pour expulser des substances hors de la cellule. La déperdition d’énergie qui en résulte active un système d’alerte métabolique centré sur le capteur AMPK, qui à son tour active une voie classique de croissance et de réponse au stress connue sous le nom de MAPK. Une fois activée, cette cascade augmente la production et la libération des protéines de mucus et renforce la capacité des cellules cancéreuses à croître, migrer et résister aux médicaments. Bloquer ABCC3 génétiquement ou avec un composé expérimental, ou inhiber la voie MAPK, a atténué la production de mucus et affaibli les tumeurs.
Ce que cela signifie pour les patients
Ensemble, ces résultats révèlent un système de contrôle en plusieurs étapes pour le cancer colorectal mucineux : L1TD1 stabilise l’ARNm d’ABCC3, ABCC3 draine l’énergie cellulaire, la voie AMPK–MAPK s’active, et la tumeur réagit en surproduisant du mucus et en devenant plus agressive et résistante aux traitements. Pour les patients, cela suggère plusieurs axes prometteurs. Les niveaux de L1TD1 et d’ABCC3 pourraient aider à repérer les tumeurs susceptibles d’avoir un comportement agressif ou de résister à la chimiothérapie standard. Plus important encore, des médicaments perturbant l’interaction L1TD1–ABCC3, bloquant l’activité de pompe du MRP3, ou ciblant la voie de signalisation en aval pourraient amincir la barrière de mucus, ralentir la croissance tumorale et rendre les traitements existants plus efficaces contre cette forme difficile de cancer colorectal.
Citation: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Mots-clés: cancer colorectal mucineux, L1TD1, ABCC3 MRP3, production de mucine, résistance aux chimiothérapies