Clear Sky Science · fr
L’hélicase d’ARN multifonctionnelle DDX39A stimule la progression du glioblastome en modulant l’épissage alternatif de WISP1 qui induit une polarisation immunosuppressive des macrophages
Pourquoi cette étude sur le cancer du cerveau compte
Le glioblastome est l’un des cancers cérébraux les plus mortels, connu pour récidiver après traitement et résister aux médicaments. Cette étude révèle comment un seul « interrupteur » moléculaire dans les cellules tumorales non seulement favorise la croissance du cancer, mais persuade aussi les cellules immunitaires voisines d’arrêter de combattre et de commencer à protéger la tumeur. En retraçant cette chaîne d’événements, les chercheurs identifient également un antipsychotique existant qui pourrait être réutilisé pour perturber ce réseau néfaste.
Un assistant clé à l’intérieur des cellules tumorales cérébrales
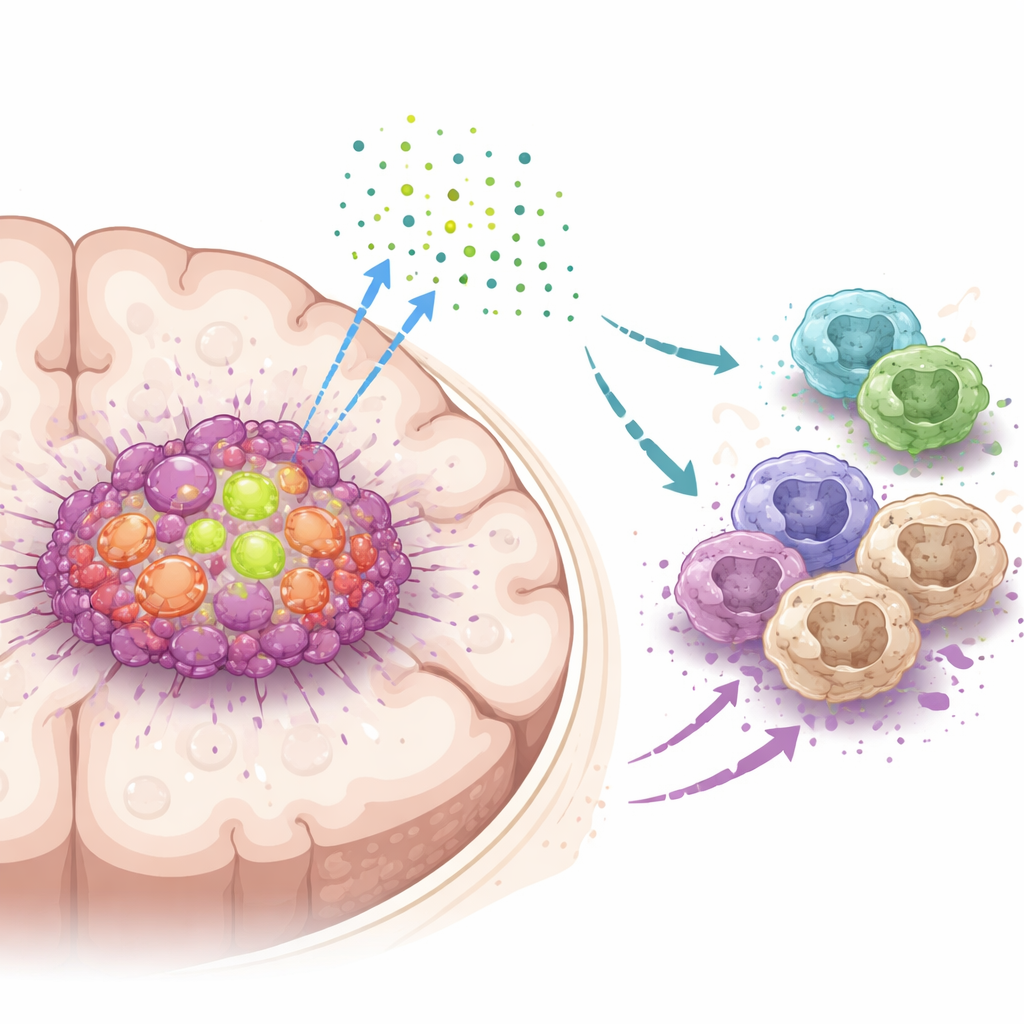
L’équipe s’est concentrée sur une protéine appelée DDX39A, une machine moléculaire qui aide les cellules à traiter l’ARN, la copie active de l’information génétique. En analysant de larges jeux de données de patients et des échantillons de tumeurs, ils ont constaté que DDX39A est beaucoup plus active dans le glioblastome que dans le tissu cérébral normal, et que son niveau augmente avec le grade tumoral. Des analyses en cellule unique ont montré que DDX39A est particulièrement abondante dans les cellules tumorales à division rapide et dans certains globules immunitaires appelés macrophages présents dans la masse tumorale. Les patients dont les tumeurs présentaient des niveaux plus élevés de DDX39A avaient tendance à avoir de moins bons pronostics, ce qui suggère que cette protéine est étroitement liée à la maladie agressive.
Comment cet assistant alimente la croissance et la dissémination
Pour tester ce que DDX39A fait réellement, les chercheurs ont utilisé des outils génétiques pour en réduire l’expression dans des cellules souches tumorales du glioblastome cultivées en laboratoire et dans des modèles murins de tumeur cérébrale. Lorsque DDX39A était diminuée, les cellules tumorales se multipliaient plus lentement, envahissaient moins efficacement les tissus environnants et étaient plus susceptibles de subir une mort cellulaire programmée. Les cellules souches tumorales ont également perdu une grande partie de leur capacité à former de nouvelles sphères tumorales, signe d’une altération de leur capacité d’auto-renouvellement. Chez la souris, les tumeurs avec DDX39A abaissée étaient plus petites et les animaux vivaient plus longtemps, confirmant que cette protéine stimule activement la progression tumorale, plutôt que d’en être un simple marqueur.
Un signal secret qui désarme les défenseurs immunitaires
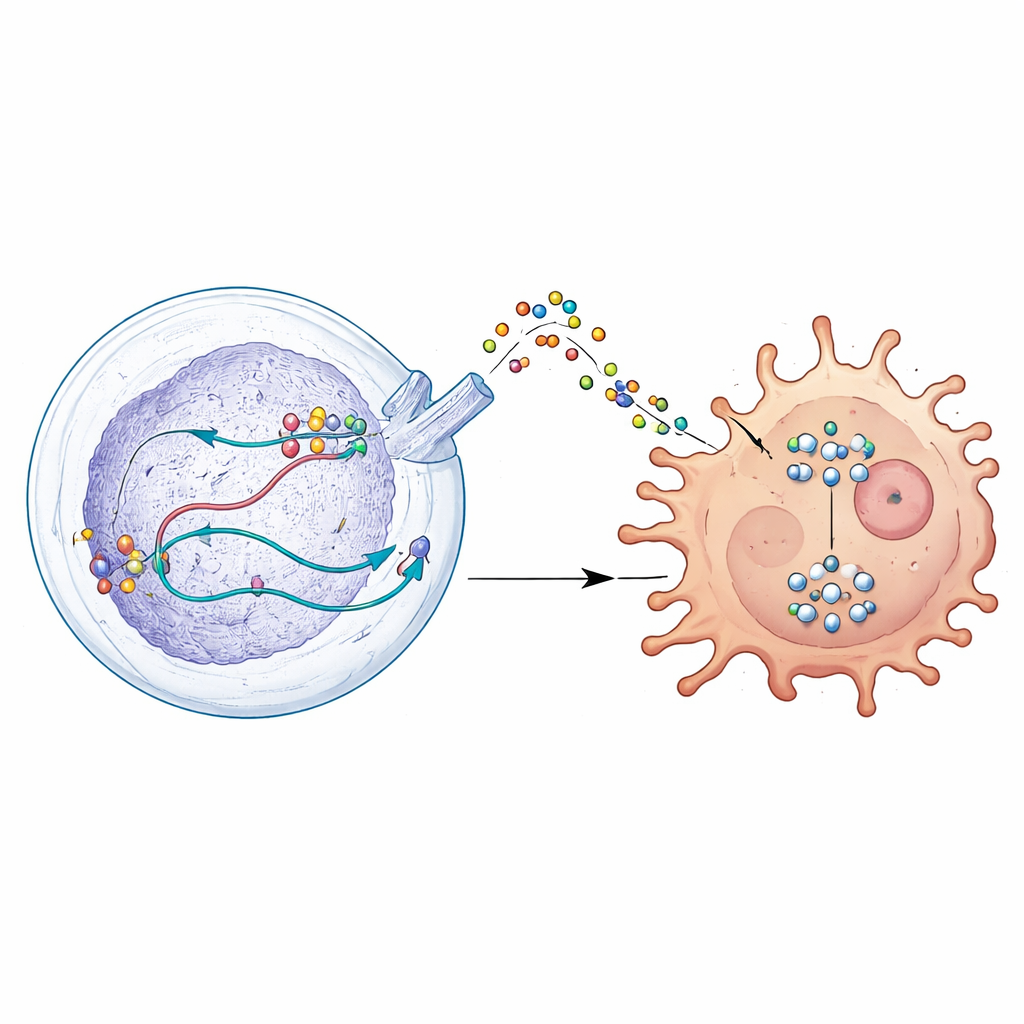
En creusant plus loin, les scientifiques ont découvert que DDX39A modifie la façon dont un gène appelé WISP1 est traité. Plutôt que d’allumer ou d’éteindre WISP1, DDX39A contribue à façonner son ARN d’une manière qui stabilise le message et augmente la production de la protéine WISP1. Les cellules tumorales libèrent alors WISP1 dans leur environnement, où il se comporte comme un signal trompeur et inquiétant. Les macrophages à proximité, qui peuvent soit attaquer les tumeurs soit les soutenir, répondent à ce signal en basculant vers un état immunosuppressif et pro-tumeur. Ce basculement est conduit par l’activation d’une voie de contrôle de la croissance intracellulaire connue sous le nom d’AKT. Lorsque DDX39A ou WISP1 était réduit, cette voie se calmait, les cellules tumorales devenaient moins agressives et les macrophages retrouvaient un profil plus favorable à la lutte contre la tumeur.
Transformer un médicament psychiatrique en arme anticancer
Armés de cette cartographie du circuit, les chercheurs ont exploré des bases de données pharmaceutiques à la recherche de molécules susceptibles d’interférer avec l’activité de DDX39A. Ils ont identifié la fluphénazine, un antipsychotique utilisé depuis longtemps et connu pour atteindre le cerveau. La modélisation informatique et des tests de liaison ont montré que la fluphénazine peut se fixer directement sur DDX39A. Dans les cellules tumorales, le médicament affaiblissait l’interaction de DDX39A avec l’ARN de WISP1, diminuait les niveaux de WISP1 et réduisait la signalisation AKT. Les cellules traitées proliféraient moins, envahissaient moins, formaient moins de sphères tumorales et étaient plus enclines à mourir. Dans des modèles murins, la fluphénazine ralentissait la croissance des tumeurs cérébrales, réduisait le nombre de macrophages soutenant la tumeur et prolongeait la survie, le tout à des doses proches de celles déjà utilisées chez l’homme pour d’autres indications.
Ce que cela signifie pour les traitements futurs
En termes simples, cette étude montre que les cellules de glioblastome exploitent DDX39A pour affiner un message (WISP1) qui renforce à la fois leur endurance et reprogramme les cellules immunitaires voisines en gardes du corps plutôt qu’en soldats. Bloquer cet assistant, soit génétiquement soit avec un médicament comme la fluphénazine, affaiblit le cancer sur deux fronts : les cellules tumorales elles-mêmes et le bouclier protecteur des macrophages immunosuppressifs. Bien que beaucoup d’essais supplémentaires soient nécessaires avant que cette stratégie puisse atteindre les patients, le travail ouvre une voie prometteuse pour réaffecter un médicament familier afin de cibler une faiblesse nouvellement révélée dans l’un des cancers cérébraux les plus tenaces.
Citation: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Mots-clés: glioblastome, épissage de l’ARN, microenvironnement tumoral, polarisation des macrophages, réaffectation de médicaments