Clear Sky Science · fr
PMM2 interagit avec TRIM28 pour recruter E2F4 et promouvoir la glycolyse tumorale médiée par KIFC3 et la progression du cancer colorectal
Pourquoi cette histoire de cancer est importante
Le cancer colorectal figure parmi les cancers les plus mortels au monde, en partie parce que de nombreuses tumeurs apprennent à détourner les systèmes énergétiques de l’organisme pour alimenter une croissance incontrôlée. Cette étude révèle comment une enzyme peu connue, PMM2, aide les tumeurs colorectales à brûler le sucre de façon plus agressive et à se propager, et pourquoi cela en fait une cible prometteuse pour de futurs médicaments et tests diagnostiques.
Un moteur tumoral affamé de sucre
Les cellules cancéreuses réorganisent souvent leur utilisation du glucose, favorisant une forme de combustion du sucre rapide mais peu efficiente connue sous le nom de glycolyse. Les chercheurs ont commencé par comparer des milliers de gènes dans des échantillons de tumeurs colorectales et dans les tissus sains voisins. PMM2, une enzyme habituellement impliquée dans l’ajout de chaînes de sucre aux protéines, s’est démarquée comme l’un des gènes les plus fortement surexprimés dans le cancer. Les cellules tumorales surexprimant PMM2 proliféraient plus rapidement, formaient davantage de colonies et se propageaient plus facilement en culture, tandis que les cellules dont PMM2 avait été désactivé ralentissaient leur croissance, migraient moins et étaient plus susceptibles de mourir.
Comment les cellules tumorales suralimentent l’utilisation du sucre
Lorsque l’équipe a réduit les niveaux de PMM2 dans des cellules de cancer colorectal, ces cellules absorbaient moins de glucose, produisaient moins d’ATP (leur principale monnaie énergétique) et relâchaient moins de lactate, le déchet de la glycolyse. Des mesures métaboliques sensibles ont confirmé que l’acidification globale du milieu environnant diminuait, tandis que la consommation d’oxygène augmentait, indiquant un déplacement hors de la glycolyse turbo-versée vers une respiration plus normale. Les protéines clés de la glycolyse, PKM2 et LDHA, déclinaient également. De façon surprenante, même une version catalytiquement « morte » de PMM2 pouvait encore favoriser ce comportement affamé de sucre, montrant que le rôle de PMM2 dans le cancer ne repose pas sur sa chimie habituelle, mais sur ses interactions avec d’autres protéines à l’intérieur de la cellule.
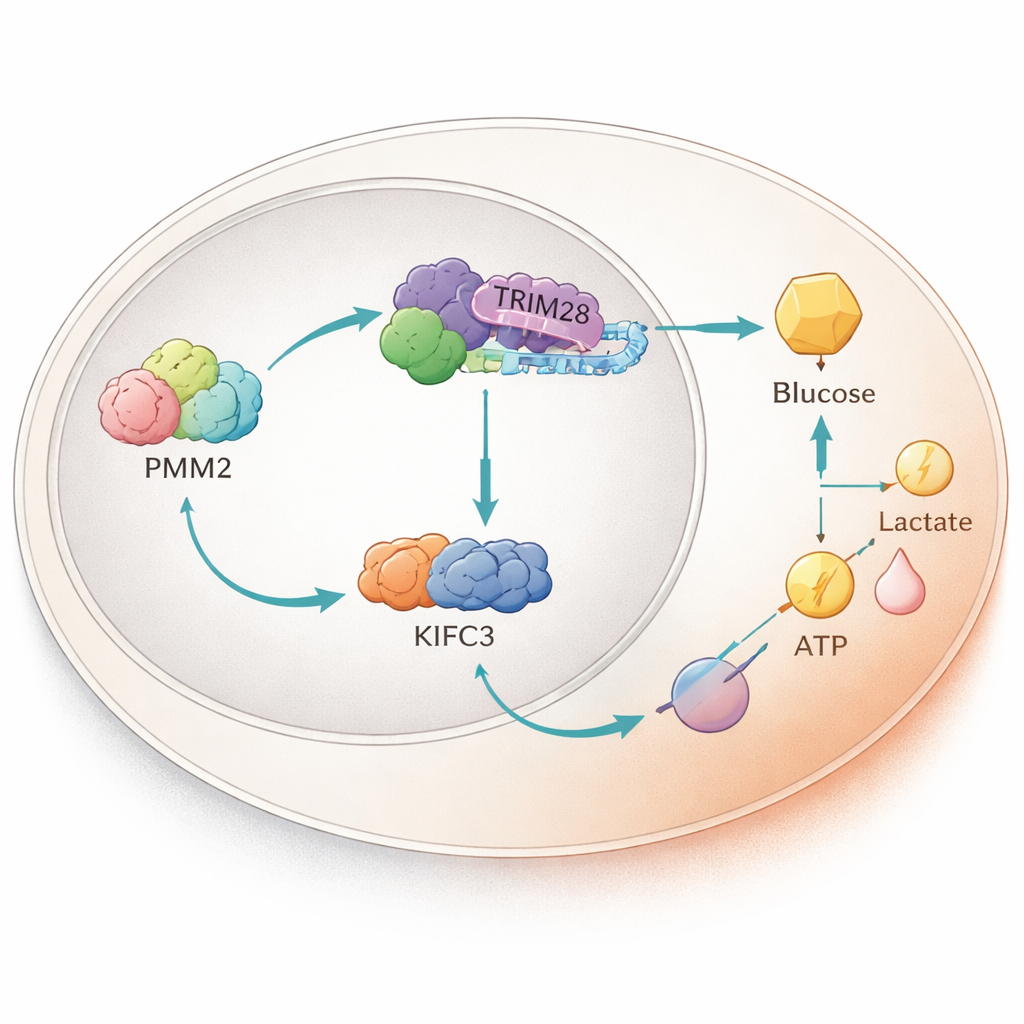
Une transmission protéique à l’intérieur du noyau
En approfondissant, les scientifiques ont découvert que PMM2 se lie physiquement à une autre protéine appelée TRIM28, qui peut se déplacer dans le noyau cellulaire et influencer l’activité des gènes. PMM2 favorise l’accumulation de TRIM28 dans le noyau, où TRIM28 s’associe à un facteur de transcription, E2F4. Ensemble, ce trio augmente la production d’une protéine motrice nommée KIFC3 en se fixant sur une région spécifique de son ADN régulateur. Des expériences supprimant la région de PMM2 nécessaire à la liaison avec TRIM28 ont éliminé la capacité de PMM2 à stimuler la glycolyse et la croissance cellulaire, soulignant que ce partenariat protéique — et non la fonction enzymatique classique de PMM2 — confère l’avantage tumoral.
Activation d’un interrupteur métabolique clé
KIFC3, mieux connu pour son rôle dans le transport de cargos le long de l’ossature interne de la cellule, s’est révélé être un commutateur métabolique crucial. Lorsque les chercheurs ont réduit les niveaux de KIFC3, les cellules de cancer colorectal consommaient moins de glucose, produisaient moins d’ATP et de lactate, et présentaient une activité glycolytique plus faible, tandis que leur consommation d’oxygène augmentait. De manière importante, la suppression de KIFC3 annula partiellement le gain de glycolyse et l’avantage de croissance normalement induits par PMM2. Chez des souris greffées avec des cellules humaines de cancer colorectal, les tumeurs surexprimant PMM2 étaient plus volumineuses, mais cet effet était atténué lorsque KIFC3 était réduit. Les échantillons tumoraux de ces animaux montraient des niveaux plus élevés de PMM2, de KIFC3 et de marqueurs de la glycolyse, reliant l’ensemble de cette chaîne d’événements dans un tissu vivant.
Des modèles de laboratoire aux échantillons de patients
Pour rapprocher le travail de la clinique, l’équipe a créé de petits organoïdes tumoraux tridimensionnels à partir de cancers colorectaux de patients. Les organoïdes présentant des niveaux plus élevés de PMM2 et de KIFC3 croissaient plus vite et produisaient plus d’ATP et de lactate que ceux ayant des niveaux plus faibles. Forcer l’expression de PMM2 dans les organoïdes augmentait KIFC3 et la glycolyse, tandis que la réduction de PMM2 avait l’effet inverse. Des analyses de séries tumorales de patients ont en outre montré que des niveaux élevés de PMM2 étaient associés à une maladie plus avancée, à une dissémination aux ganglions lymphatiques et à une survie globale plus courte, faisant de PMM2 un biomarqueur candidat solide.
Ce que cela signifie pour les soins futurs
En termes simples, cette étude montre que de nombreuses tumeurs colorectales semblent intégrer PMM2 dans une chaîne de relais protéique nucléaire — via TRIM28 et E2F4 — pour augmenter KIFC3 et, par conséquent, leur machinerie de combustion du sucre. Cette montée métabolique aide les cancers à croître et à se propager. Parce que cette voie dépend d’interactions protéiques plutôt que de l’activité enzymatique habituelle de PMM2, elle ouvre de nouvelles pistes thérapeutiques : des petites molécules, des peptides ou des médicaments dégradateurs qui perturbent la liaison de PMM2 à TRIM28, bloquent l’accès d’E2F4 à l’ADN ou atténuent l’activité de KIFC3 pourraient, en théorie, priver les tumeurs de leur carburant préféré. Bien que de tels traitements ne soient pas encore disponibles, la chaîne PMM2–TRIM28–E2F4–KIFC3 se distingue désormais comme une feuille de route prometteuse pour des stratégies plus ciblées et centrées sur le métabolisme contre le cancer colorectal.
Citation: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
Mots-clés: cancer colorectal, métabolisme tumoral, glycolyse, signalisation oncogénique, biomarqueur