Clear Sky Science · fr
ULK1 favorise la progression métastatique dans des modèles expérimentaux du cancer épithélial de l’ovaire
Pourquoi cette recherche est importante
Le cancer épithélial de l’ovaire est souvent détecté seulement après s’être silencieusement propagé dans l’abdomen, ce qui en fait l’un des cancers les plus meurtriers chez les femmes. Une étape clé de cette dissémination est la formation de petits amas de cellules tumorales, appelés sphéroïdes, qui flottent dans le liquide abdominal, survivent à la chimiothérapie et ensemencent de nouvelles tumeurs. Cette étude pose une question ciblée aux implications majeures : un « interrupteur de survie » cellulaire nommé ULK1 aide-t-il ces amas à perdurer et à se propager, et son inhibition pourrait-elle ouvrir de nouvelles voies de traitement du cancer ovarien avancé ?
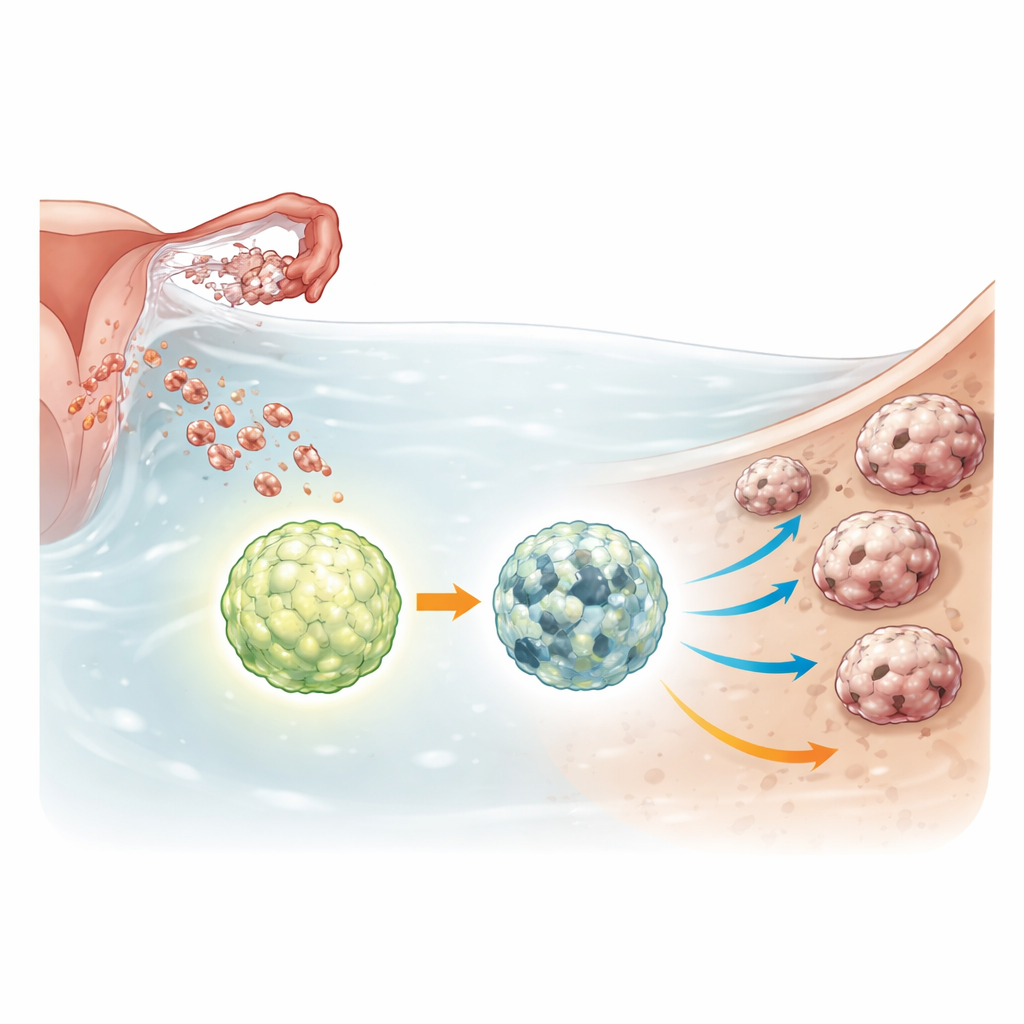
Un interrupteur de survie au sein des amas de cellules cancéreuses
Les sphéroïdes du cancer ovarien supportent des conditions difficiles : faible apport en nutriments, absence d’attachement et exposition à la chimiothérapie. Pour faire face, ils augmentent un processus de recyclage appelé autophagie, qui dégrade et réutilise des composants internes pour maintenir les cellules en vie sous stress. ULK1 est le commutateur principal qui active ce système de recyclage. Les chercheurs ont utilisé des outils d’édition génétique pour supprimer complètement ULK1 dans plusieurs lignées de cellules cancéreuses ovariennes et dans une lignée non cancéreuse de trompe utérine représentant des stades précancéreux. Ils ont ensuite comparé le comportement des cellules normales et déficientes en ULK1 lorsqu’elles sont cultivées en sphéroïdes flottants ou en mini-tumeurs tridimensionnelles appelées organoïdes.
Que se passe-t-il quand l’interrupteur est coupé
Lorsque ULK1 a été supprimé dans des cellules de cancer ovarien, leur capacité à réaliser l’autophagie au sein des sphéroïdes a été fortement réduite, comme l’ont montré des variations de protéines clés du recyclage. Ces sphéroïdes dépourvus d’ULK1 contenaient moins de cellules vivantes et présentaient davantage de signes d’apoptose programmée, indiquant que les amas tumoraux ne supportaient plus aussi bien les conditions stressantes. Fait intéressant, la suppression d’ULK1 dans les cellules précurseurs non cancéreuses n’a pas autant compromis leur système de recyclage, ce qui suggère que les cellules cancéreuses dépendent davantage d’ULK1 que leurs homologues saines. Cette dépendance spécifique au cancer fait d’ULK1 une cible thérapeutique prometteuse.
Ralentir la dissémination et affaiblir les avant-postes tumoraux
Au-delà de la survie en suspension, les sphéroïdes doivent s’attacher et envahir la paroi lisse de la cavité abdominale pour former de nouvelles tumeurs. Grâce à des modèles de laboratoire reproduisant cette étape précoce de la métastase, l’équipe a montré que les sphéroïdes déficients en ULK1 étaient nettement moins efficaces pour repousser et envahir une couche de cellules mésothéliales, qui tapissent normalement les organes abdominaux. Lorsqu’elles étaient cultivées en organoïdes incorporés dans une matrice gélatineuse, les cellules cancéreuses sans ULK1 formaient aussi des structures tumorales plus petites et moins robustes. Dans des modèles murins où des cellules humaines de cancer ovarien étaient injectées dans la cavité abdominale, la perte d’ULK1 a entraîné moins de dépôts tumoraux et moins d’accumulation de liquide, deux signes d’une maladie avancée, bien que la survie globale des animaux ne se soit pas améliorée.
Affaiblissement des signaux clés et renforcement des effets des médicaments ciblés
Pour comprendre comment ULK1 soutient le cancer au-delà du recyclage, les chercheurs ont cartographié les modifications protéiques dans des sphéroïdes dépourvus d’ULK1. Ils ont constaté que d’importantes voies de croissance et de survie intracellulaires — en particulier les voies MEK–MAPK et PI3K–AKT–mTOR — étaient perturbées. Ces voies aident normalement les cellules cancéreuses à résister à la mort et à continuer à se diviser. Lorsque l’équipe a traité des sphéroïdes déficients en ULK1 avec des médicaments bloquant MEK ou mTOR, les amas tumoraux sont devenus beaucoup plus vulnérables, avec une viabilité et une capacité de réattachement fortement réduites. En revanche, la suppression d’ULK1 n’a pas amélioré l’efficacité des chimiothérapies classiques comme le carboplatine, le paclitaxel, ou de l’inhibiteur de PARP olaparib, et dans certaines conditions a semblé en réduire l’efficacité.
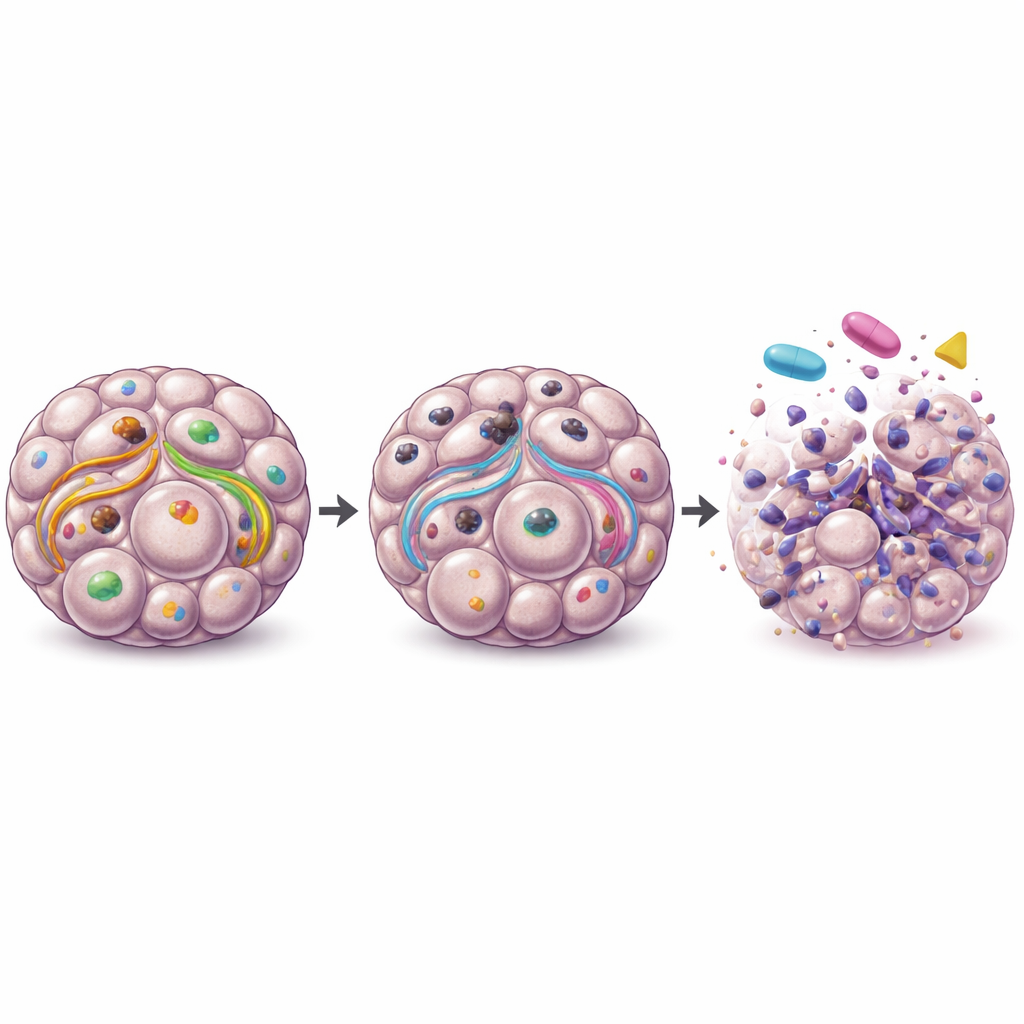
Indices tirés de tumeurs de patientes et de modèles miniatures dérivés de patientes
En examinant de larges jeux de données publics sur des tumeurs ovariennes, les auteurs ont observé qu’une activité élevée du gène ULK1 était associée à une moins bonne survie à long terme et était particulièrement élevée dans les échantillons métastatiques comparés aux tumeurs primaires et aux tissus normaux. Pour se rapprocher de la clinique, ils ont testé une pilule clinique inhibitrice d’ULK1, DCC-3116, sur des organoïdes dérivés de patientes et cultivés à partir d’échantillons tumoraux métastatiques. Dans une sous-partie de ces modèles, bloquer ULK1 seul, ou utiliser des inhibiteurs de MEK ou de mTOR seuls, réduisait la survie des organoïdes, bien que la combinaison des agents n’ajoute pas systématiquement un bénéfice supplémentaire. D’autres organoïdes de patientes étaient résistants à tous les traitements, soulignant la grande diversité des cancers ovariens et la nécessité de biomarqueurs pour identifier qui pourrait bénéficier.
Ce que cela signifie pour les soins futurs
Pris ensemble, ces résultats dessinent ULK1 comme un acteur central de la dissémination du cancer ovarien : il alimente le recyclage interne qui maintient les sphéroïdes en vie, soutient leur capacité à envahir de nouveaux sites et contribue au maintien de puissants signaux de croissance. Inhiber ULK1 affaiblit ces processus, réduit la taille des tumeurs expérimentales et rend les amas cellulaires tumoraux plus sensibles à certains médicaments ciblés, sans améliorer l’action des chimiothérapies standards. Pour les patientes, ce travail suggère qu’ULK1 pourrait entrer dans une stratégie de médecine de précision — notamment pour celles dont la tumeur métastatique présente une forte activité d’ULK1 — où des inhibiteurs ciblés d’ULK1 seraient associés à des bloqueurs de MEK ou de mTOR pour limiter la croissance et la dissémination tumorales, à condition que des tests fiables permettent d’identifier les tumeurs les plus susceptibles de répondre.
Citation: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Mots-clés: cancer de l’ovaire, métastase, autophagie, ULK1, thérapie ciblée