Clear Sky Science · fr
Association des rétinoïdes, des récepteurs de l’acide rétinoïque et de l’épigénétique dans le cancer du sein
Pourquoi la vitamine A compte dans le cancer du sein
La plupart des gens connaissent la vitamine A comme un nutriment important pour la vision, mais sa forme active dans l’organisme, l’acide rétinoïque, aide aussi les cellules à décider de se diviser, de se spécialiser ou de s’autodétruire lorsqu’elles sont endommagées. Cet article de synthèse examine comment l’acide rétinoïque et ses « stations d’ancrage » cellulaires sont altérés dans le cancer du sein, pourquoi des résultats prometteurs en laboratoire ne se sont pas encore traduits par des médicaments efficaces chez les patients, et comment de nouvelles connaissances sur le « logiciel » des cellules cancéreuses — leur code épigénétique — pourraient relancer cette stratégie thérapeutique.
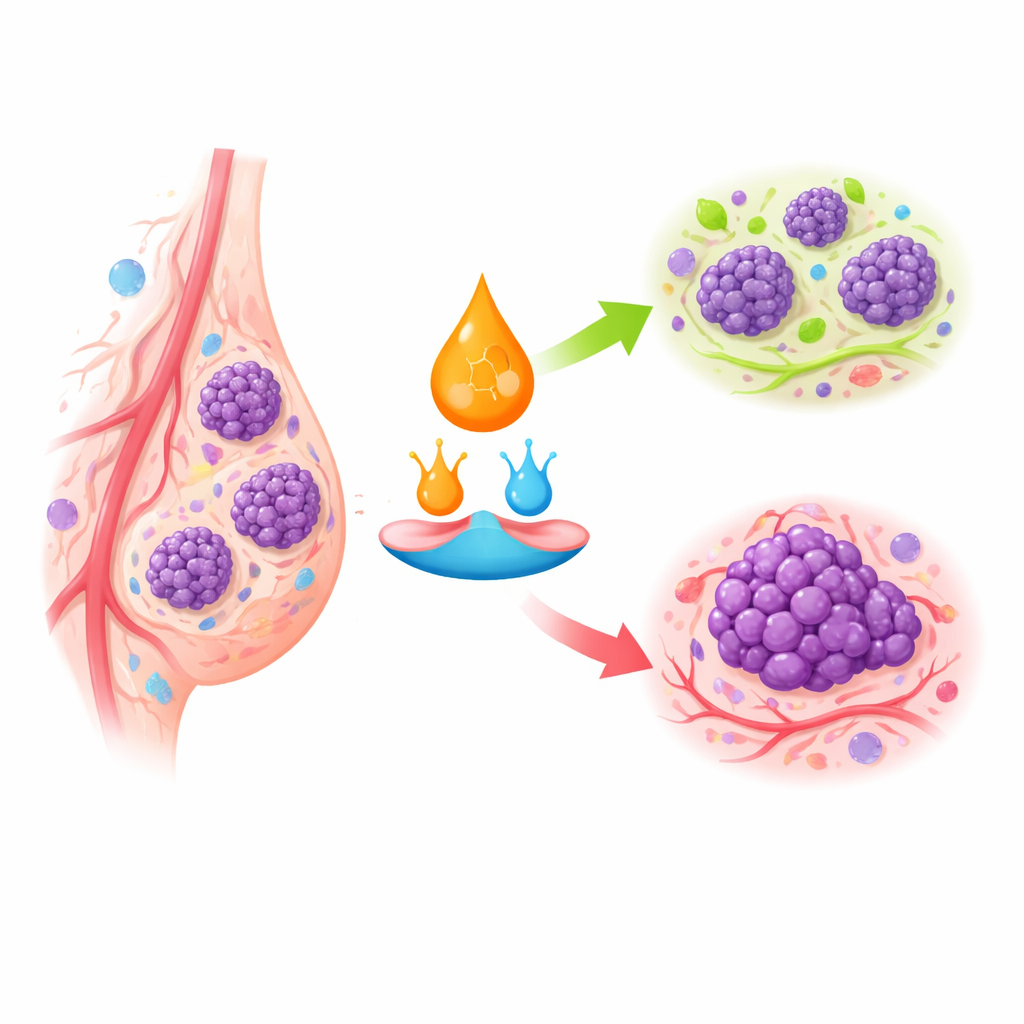
Feux de signalisation cellulaires pour la croissance et l’autodestruction
L’acide rétinoïque agit en se liant à des récepteurs spécifiques à l’intérieur des cellules, qui commandent alors l’activation ou la répression de larges ensembles de gènes. Dans le tissu mammaire sain, ce système encourage les cellules à arrêter de se diviser, à mûrir en formes stables ou à mourir si elles deviennent anormales. Dans le cancer du sein, en particulier dans les sous‑types les plus agressifs, des récepteurs clés sont absents ou silencieux, et le transport interne de l’acide rétinoïque est réorienté. Au lieu d’être acheminé vers des récepteurs qui freinent la croissance, il peut être dirigé vers des voies qui favorisent la survie et la prolifération. Cela aide à expliquer pourquoi certaines tumeurs mammaires répondent faiblement aux rétinoïdes alors que ces mêmes médicaments sont très efficaces dans certains cancers du sang.
Interrupteurs cachés dans le logiciel de la cellule cancéreuse
Les auteurs se concentrent sur l’épigénétique — des marques chimiques sur l’ADN et ses protéines d’emballage qui fonctionnent comme des réglages logiciels pour le génome. Dans de nombreux cancers du sein, ces marques verrouillent d’importants récepteurs de l’acide rétinoïque, en particulier un récepteur nommé RARβ2, en position « off » sans modifier la séquence d’ADN sous‑jacente. Des groupes méthyle supplémentaires sur l’ADN et le resserrement de la « bobine » protéique ferment ce récepteur, tandis que d’autres enzymes remodelent le paysage de la chromatine pour favoriser la croissance et la migration. Les ARN non codants, qui ne produisent pas de protéines mais influencent l’activité génique, dévient encore davantage la signalisation loin de la mort cellulaire et de la différenciation. Ensemble, ces changements donnent aux cellules cancéreuses la flexibilité nécessaire pour résister aux traitements et s’adapter au stress.
Reconfigurer les voies de signalisation
De manière importante, ces verrous épigénétiques sont réversibles. Dans des modèles de laboratoire, des médicaments qui éliminent la méthylation de l’ADN ou assouplissent la chromatine peuvent restaurer RARβ2 et d’autres composants de la voie de l’acide rétinoïque. Lorsqu’ils sont combinés à l’acide rétinoïque lui‑même et à la chimiothérapie standard, ces agents de « préamorçage » réduisent les tumeurs plus efficacement et diminuent le réservoir de cellules proches des cellules souches, considérées comme à l’origine des rechutes. La manière dont l’acide rétinoïque est transporté à l’intérieur de la cellule importe également : une protéine de transport le guide vers des récepteurs qui suppriment la croissance, tandis qu’une autre le délivre à des voies pro‑croissance. Ajuster l’équilibre entre ces transporteurs peut transformer l’action de l’acide rétinoïque, passant d’un effet d’engrais à un effet de frein.
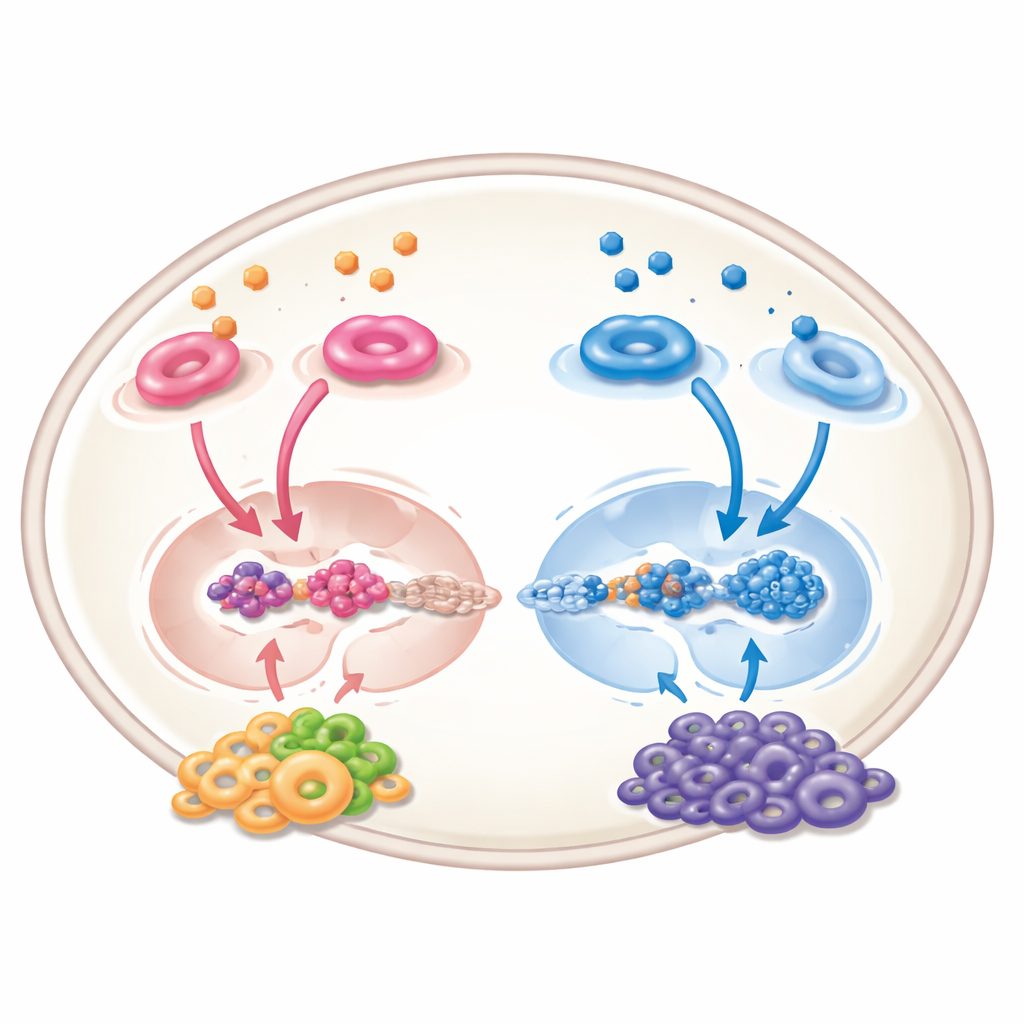
Au‑delà de la tumeur : l’effet de voisinage
L’acide rétinoïque n’agit pas uniquement sur les cellules cancéreuses ; il remodèle aussi le « voisinage » tumoral composé des vaisseaux sanguins, des cellules immunitaires et des cellules de soutien. Dans des systèmes expérimentaux, il peut réduire la néovascularisation, orienter les cellules immunitaires vers un état plus actif et antitumoral, et limiter les cellules suppressives qui atténuent normalement les défenses de l’organisme. Pourtant, le tableau n’est pas entièrement positif : dans certains éléments du stroma autour de la tumeur, l’activation de la signalisation de l’acide rétinoïque peut en réalité favoriser la croissance tumorale en renforçant des canaux de communication chimique qui attirent et soutiennent les cellules malignes. Ces effets opposés signifient que toute thérapie future devra être finement réglée pour cibler les bons types cellulaires de la bonne manière.
Concevoir des essais plus intelligents pour l’avenir
Les premiers essais cliniques des rétinoïdes dans le cancer du sein ont largement échoué, mais ils ont été menés avant la compréhension actuelle des sous‑types, des biomarqueurs et de la pharmacologie complexe. Les auteurs soutiennent que les nouveaux essais devraient sélectionner des patientes dont les tumeurs présentent les signes moléculaires de sensibilité aux rétinoïdes, tels qu’une expression conservée des récepteurs ou des profils spécifiques de méthylation de l’ADN, et associer les rétinoïdes à des médicaments qui débloquent les blocages épigénétiques, ciblent les voies de croissance ou renforcent l’attaque immunitaire. Des formulations améliorées maintenant des concentrations médicamenteuses stables dans l’organisme, ainsi qu’une surveillance étroite de la tumeur et des tissus environnants, seront cruciales. Si ces obstacles peuvent être surmontés, les traitements à base d’acide rétinoïque pourraient trouver leur place comme outils de précision contre des formes sélectionnées de cancer du sein.
Citation: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
Mots-clés: acide rétinoïque, cancer du sein, épigénétique, thérapie de différenciation, microenvironnement tumoral