Clear Sky Science · fr
Modéliser les échanges entre tissu adipeux et cancer : une perspective tridimensionnelle
Pourquoi la graisse et le cancer sont plus proches que vous ne le pensez
La plupart d’entre nous considèrent la graisse corporelle comme un simple rembourrage ou une réserve d’énergie, mais les recherches la révèlent aujourd’hui comme un organe actif et communicant qui peut influencer notre santé de manière surprenante. Cet article de synthèse examine comment le tissu adipeux et les cellules cancéreuses communiquent, et comment de nouveaux modèles de laboratoire tridimensionnels (3D) aident les scientifiques à reproduire ce dialogue de façon plus réaliste que jamais. Comprendre cette conversation cachée pourrait améliorer la prévention du cancer, les tests de médicaments et les traitements, en particulier dans un monde où le surpoids est de plus en plus fréquent. 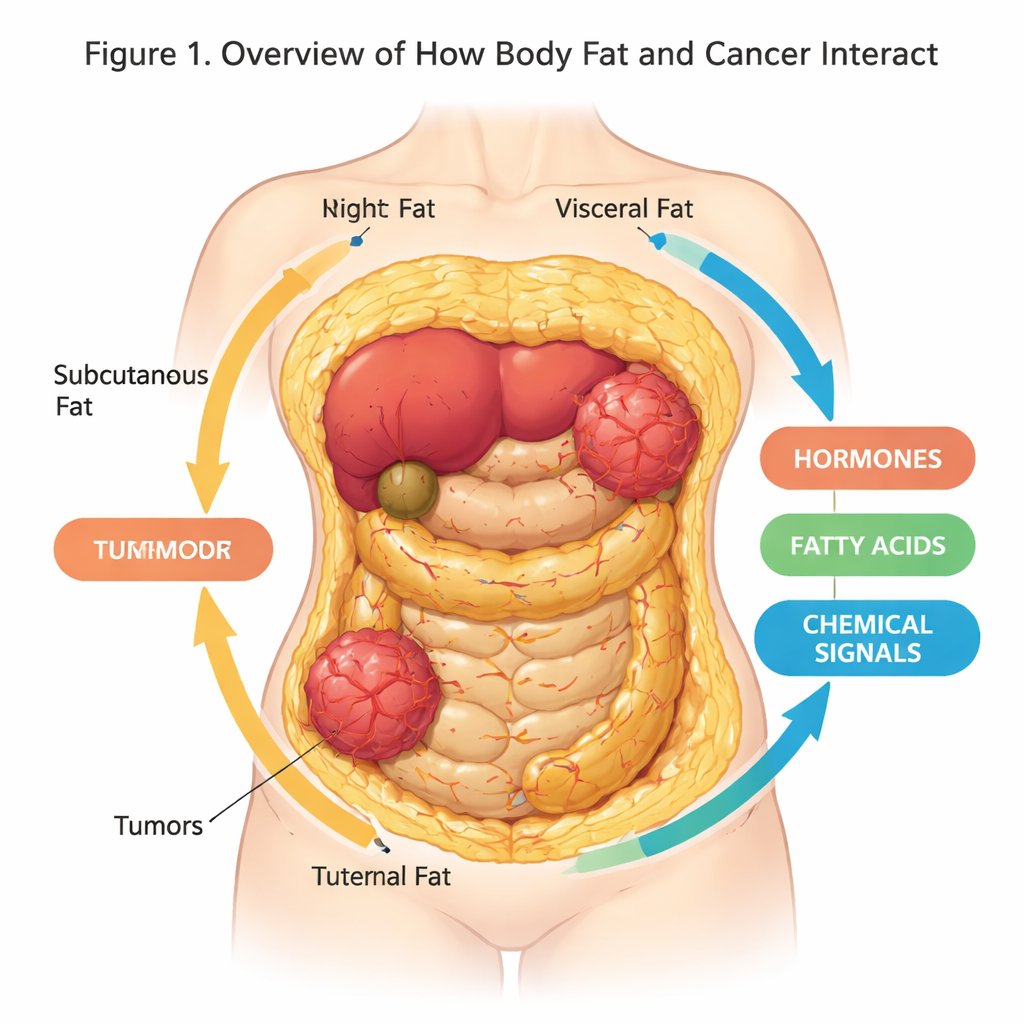
La graisse comme organe vivant et communicant
Le tissu adipeux—notre graisse corporelle—n’est pas seulement un site de stockage passif. C’est un organe complexe composé d’adipocytes, de cellules immunitaires, de vaisseaux sanguins et de cellules de soutien, tous intégrés dans une trame structurelle appelée matrice extracellulaire. Différents types de graisse se trouvent à divers endroits : la graisse sous‑cutanée sous la peau, la graisse viscérale autour des organes internes, et des adipocytes blancs, bruns et beiges qui diffèrent selon leur manière de stocker l’énergie ou de la brûler sous forme de chaleur. Ces cellules libèrent en permanence un cocktail d’hormones, d’acides gras et de protéines de signalisation qui influencent le métabolisme, l’inflammation et, comme on le sait maintenant, le risque et le comportement du cancer.
Obésité, inflammation et risque de cancer
Lorsque nous prenons trop de poids, les adipocytes blancs augmentent en taille et en nombre et le tissu devient stressé et enflammé. Cette graisse « malsaine » libère davantage de molécules inflammatoires et d’acides gras dans la circulation sanguine, tout en traitant moins efficacement le sucre et les lipides. De larges études épidémiologiques ont associé l’obésité à un risque accru et à des issues plus défavorables pour de nombreux cancers, notamment du sein, du côlon, du pancréas et de l’utérus. La revue explique comment un tissu adipeux dysfonctionnel peut « nourrir » les tumeurs avec un apport énergétique supplémentaire, raidir le tissu environnant et recruter d’autres types cellulaires qui, ensemble, créent un milieu plus favorable au cancer.
Une conversation bidirectionnelle entre graisse et tumeurs
Le cancer est désormais considéré comme une maladie d’un écosystème entier, et pas seulement de cellules défaillantes. Les cellules tumorales exploitent la graisse voisine pour leur soutien, reprogrammant les adipocytes, les cellules immunitaires et les fibroblastes afin de favoriser leur croissance et leur dissémination. En retour, les adipocytes répondent en décomposant leurs lipides stockés et en libérant des acides gras et des hormones que les cellules cancéreuses peuvent utiliser directement. Ce dialogue peut s’opérer à distance via des signaux circulants, ou localement lorsque les tumeurs poussent à côté de la graisse, comme au niveau du sein ou de l’abdomen. Les cellules tumorales peuvent même pousser les adipocytes à perdre leur identité initiale pour devenir davantage des cellules semblables à des fibroblastes cicatriciels ou à des cellules immunitaires, remodelant le tissu et favorisant l’invasion. 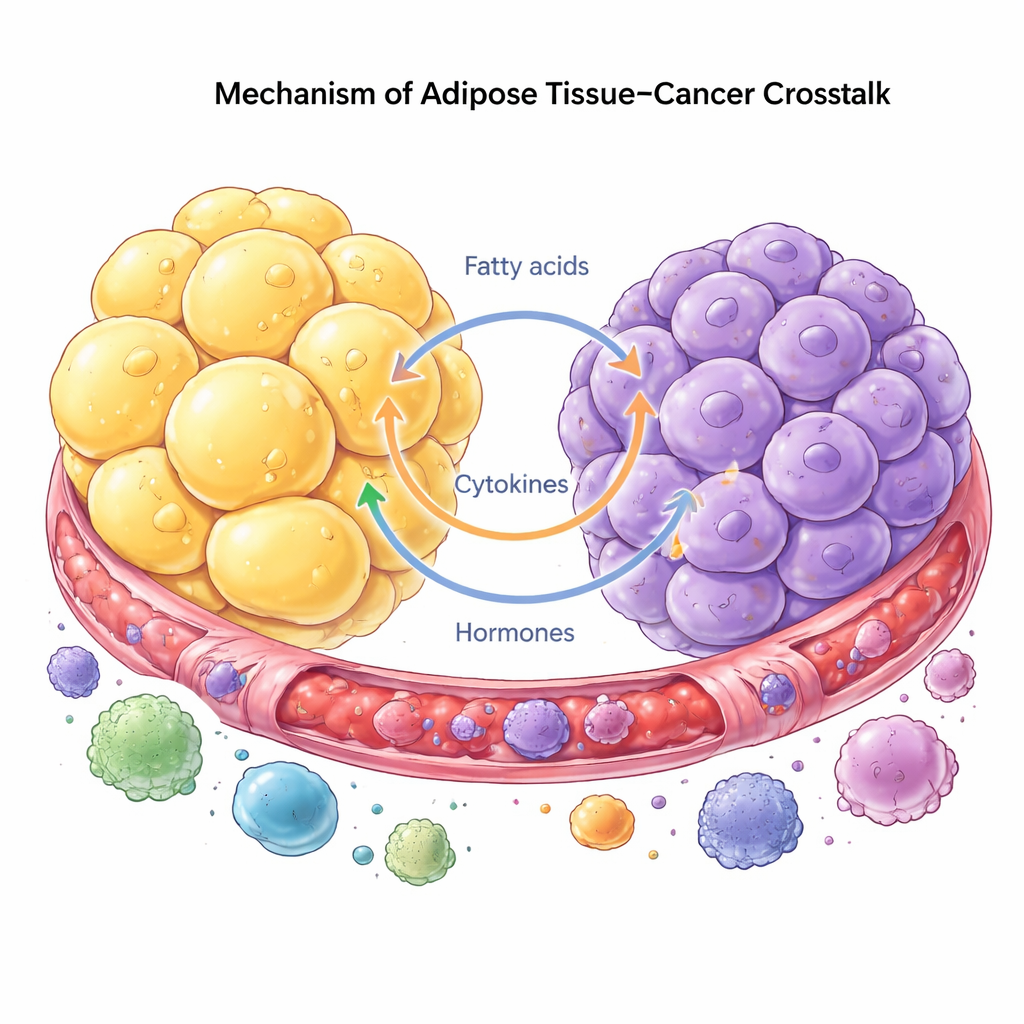
Construire des mini‑tissus en 3D
Les cultures cellulaires traditionnelles en 2D et les modèles animaux échouent souvent à capturer ces interactions complexes. Les auteurs décrivent une nouvelle génération de systèmes 3D qui ressemblent davantage aux tissus réels. Les sphéroïdes sont de simples amas cellulaires qui s’auto‑assemblent en petites sphères ; les échafaudages sont des matériaux conçus qui fournissent un support 3D pour la croissance cellulaire ; les organoïdes sont des versions miniatures et auto‑organisées de tissus ; et les assembloïdes combinent plusieurs organoïdes ou sphéroïdes en « mini‑organes » composites. Les chercheurs utilisent désormais ces approches 3D pour cocultiver adipocytes et cellules cancéreuses, étudier comment des conditions proches de l’obésité modifient leur comportement, et tester comment les médicaments pourraient perturber le dialogue néfaste entre eux.
Promesses et lacunes actuelles
Chaque modèle présente des compromis. Les sphéroïdes sont peu coûteux et adaptés au haut débit mais relativement simples. Les échafaudages permettent un contrôle précis des propriétés physiques telles que la rigidité, qui peut influencer la dissémination tumorale, mais ils sont plus exigeants techniquement. Les organoïdes et les assembloïdes offrent le plus haut degré de réalisme, avec de multiples types cellulaires interagissant, mais ils sont coûteux, difficiles à standardiser et manquent souvent de réseaux vasculaires complets ou de composants immunitaires. La revue insiste sur le fait que les systèmes actuels sont encore loin de reproduire parfaitement le tissu adipeux et tumoral humains, en particulier pour ce qui est de restituer la matrice extracellulaire complète, des adipocytes matures et la participation des cellules immunitaires.
Vers où se dirige cette recherche
Les auteurs concluent que l’amélioration des modèles 3D des interactions graisse–cancer est essentielle pour des essais médicamenteux plus précis et pour comprendre comment l’obésité favorise le cancer. À mesure que ces « mini‑tissus » deviennent plus réalistes — combinant une graisse fidèle, des cellules tumorales, des vaisseaux sanguins et des cellules immunitaires — ils pourraient aider les chercheurs à prédire quels traitements fonctionneront chez des patients spécifiques, concevoir de meilleures stratégies pour bloquer l’utilisation de la graisse corporelle comme carburant par le cancer, et finalement orienter des thérapies qui ciblent non seulement les tumeurs, mais aussi les environnements malsains qui les aident à prospérer.
Citation: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
Mots-clés: tissu adipeux, obésité, microenvironnement tumoral, culture cellulaire 3D, métabolisme tumoral