Clear Sky Science · fr
O-GlcNAcylation de POM121 facilite la métastase osseuse dans le cancer bronchique non à petites cellules via une importation nucléaire accrue de c-MYC et le reprogrammation de la MEC
Pourquoi cette recherche est importante
Lorsque le cancer du poumon se propage aux os, il provoque des douleurs intenses, des fractures et une survie fortement raccourcie ; pourtant les médecins disposent encore de peu d’outils pour arrêter cette étape mortelle. Cette étude explore les mécanismes internes des cellules cancéreuses pulmonaires pour comprendre comment certaines d’entre elles acquièrent un avantage particulier leur permettant de migrer depuis le poumon vers l’os et d’y prospérer. En retraçant ce processus jusqu’à de minuscules modifications sur une seule protéine de garde à la frontière du noyau, les auteurs identifient une nouvelle chaîne d’événements qui pourrait être ciblée pour mieux prédire, prévenir ou traiter les métastases osseuses chez les patients atteints de cancer bronchique non à petites cellules.
Une étiquette sucrée qui modifie le comportement du cancer
Les chercheurs se sont intéressés aux modifications post‑traductionnelles, de petites altérations chimiques que subissent les protéines après leur synthèse. L’une d’entre elles, l’O‑GlcNAcylation, consiste en l’addition d’un petit sucre à des sites spécifiques des protéines. En utilisant des lignées cellulaires de cancer du poumon et des modèles murins, l’équipe a comparé des cellules tumorales ordinaires à des sous‑populations sélectionnées de manière répétée pour leur capacité à coloniser l’os. Ils ont constaté que ces cellules « chercheuses d’os » présentaient des niveaux globaux d’O‑GlcNAcylation bien plus élevés, dus à une activité accrue de l’enzyme OGT, qui place l’étiquette sucrée. Parmi des centaines de protéines modifiées, une a particulièrement attiré l’attention : POM121, un composant central du pore nucléaire, la structure qui contrôle les échanges entre le noyau et le cytoplasme.
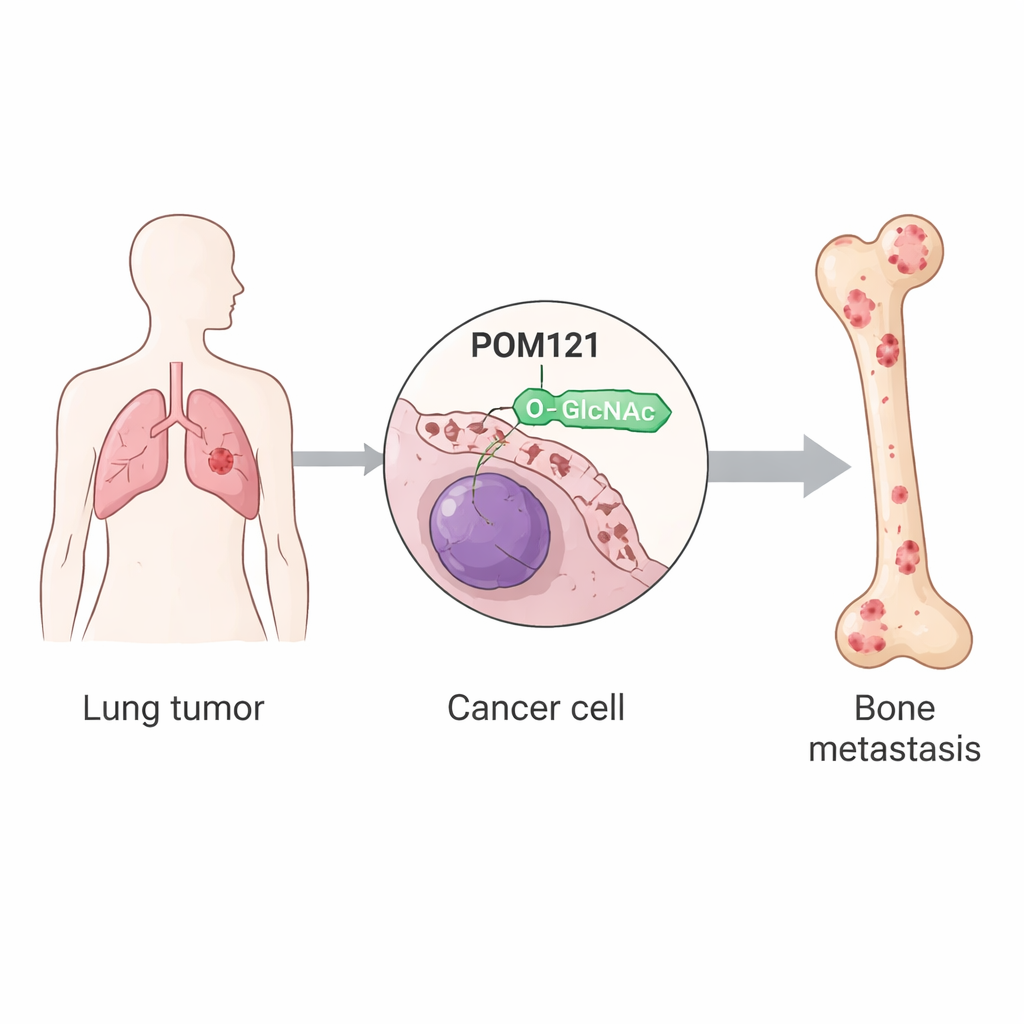
Le gardien nucléaire POM121 est stabilisé
POM121 est intégré dans la membrane entourant le noyau et fait partie du canal par lequel doivent passer de nombreuses protéines de signalisation. Dans les cellules de cancer du poumon métastatiques aux os, POM121 portait une forte charge d’O‑GlcNAc en un seul site d’acide aminé appelé sérine 199. Lorsque ce site était muté de façon à ne plus pouvoir être modifié, la protéine devenait instable et était rapidement dégradée par les mécanismes d’élimination cellulaires. L’étude montre que l’étiquette sucrée protège POM121 contre le marquage pour destruction par une enzyme nommée TRIM21, qui attache normalement des étiquettes d’ubiquitine signalant l’élimination. En présence d’O‑GlcNAc, TRIM21 se lie moins bien, l’ubiquitination diminue et POM121 s’accumule au pore nucléaire sans changer de localisation.
Ouverture de la porte à un puissant moteur de cancer
Quelle différence apporte un POM121 plus stable ? La clé réside dans une protéine connue pour favoriser le cancer, le facteur de transcription c‑MYC. c‑MYC doit pénétrer dans le noyau pour activer des gènes, mais son passage dépend de composants du pore nucléaire comme POM121. Les auteurs ont montré que lorsque POM121 était abondant et O‑GlcNAcylé, davantage de c‑MYC se retrouvait à l’intérieur du noyau ; lorsque les niveaux de POM121 étaient réduits ou que son étiquette sucrée était supprimée, l’import nucléaire de c‑MYC chutait fortement. Chez la souris, les cellules de cancer du poumon portant le mutant non modifiable de POM121 formaient beaucoup moins de métastases osseuses et de plus petite taille, tandis que la restauration de c‑MYC dans des cellules déficientes en POM121 sauvait une grande partie de leur capacité à coloniser l’os. Cela place POM121 en amont de c‑MYC dans une voie métastatique critique.
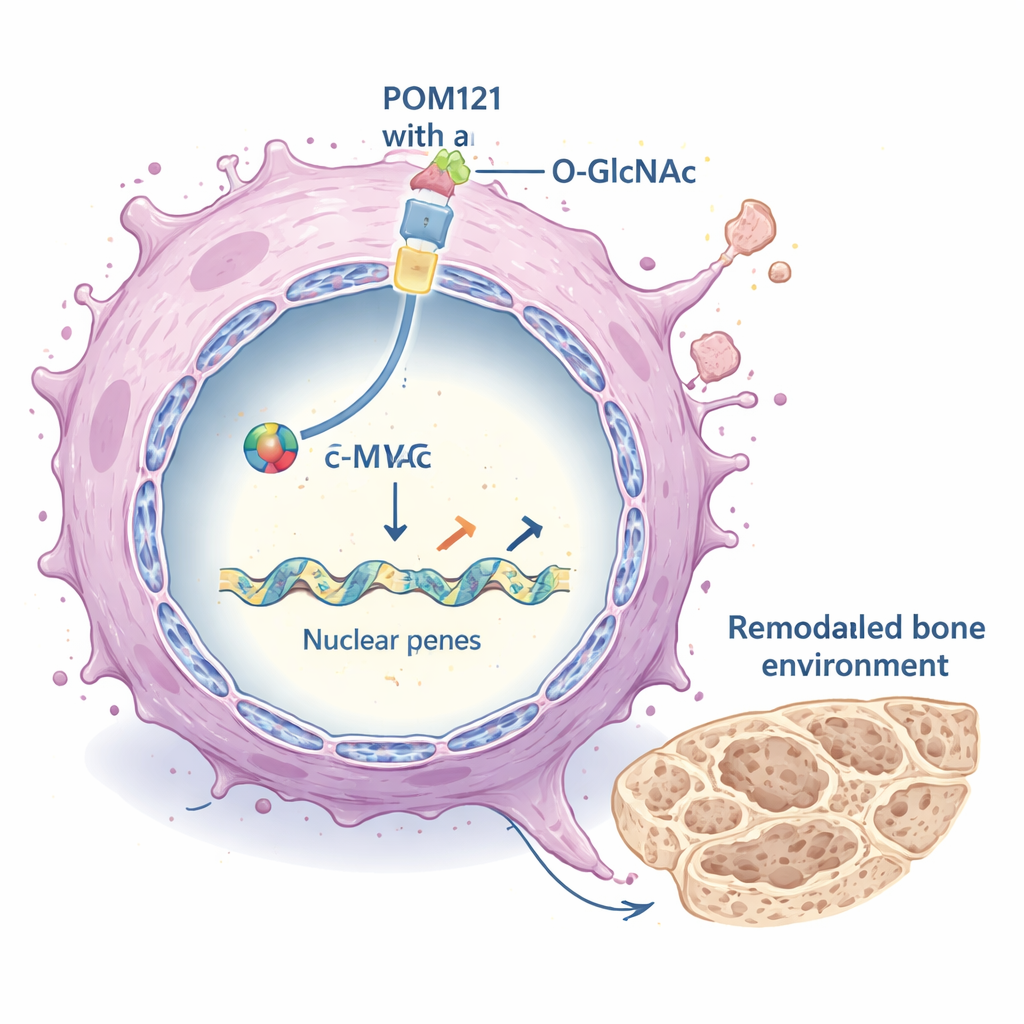
Reconfiguration de l’environnement tumoral
Une fois dans le noyau, c‑MYC agit comme un commutateur maître pour de nombreux gènes. Il a été trouvé qu’il active fortement un ensemble de gènes qui façonnent la matrice extracellulaire (MEC) – l’armature de protéines entourant les cellules. Ces gènes de la MEC, qui comprennent divers collagènes et des enzymes remodelant la structure tissulaire, étaient réprimés lorsque POM121 ou c‑MYC étaient bloqués, et activés lorsque l’O‑GlcNAcylation et POM121 étaient élevées. La MEC altérée renforçait à son tour d’importantes voies de croissance à l’intérieur des cellules cancéreuses, notamment la cascade de signalisation PI3K–AKT–mTOR, qui soutient survie, croissance et dissémination. Des schémas similaires sont apparus dans plusieurs modèles de cancer du poumon différents, suggérant que ce mécanisme n’est pas limité à une seule lignée cellulaire.
De la découverte en laboratoire à l’impact pour les patients
En analysant des données de patients, les chercheurs ont constaté que des niveaux élevés d’OGT, de POM121 et de c‑MYC, ainsi que des gènes de la MEC qu’ils régulent, étaient associés à de moins bons pronostics et à des tumeurs pulmonaires déjà disséminées aux os. Pris ensemble, les travaux décrivent un axe OGT–POM121–c‑MYC–MEC : une O‑GlcNAcylation accrue stabilise le gardien nucléaire POM121, qui transporte plus de c‑MYC vers le noyau, ce qui reprogramme ensuite l’armature tissulaire et les signaux de croissance en faveur des métastases osseuses. Pour les patients, cela suggère de nouveaux types de biomarqueurs pour identifier ceux à risque de diffusion osseuse, et de nouvelles approches thérapeutiques – depuis le blocage d’OGT ou de la fonction de POM121 jusqu’à l’atténuation de c‑MYC ou du remodelage de la MEC – qui pourraient un jour aider à empêcher le cancer du poumon d’atteindre le squelette.
Citation: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Mots-clés: métastase osseuse cancer du poumon, POM121, O-GlcNAcylation, c-MYC, matrice extracellulaire