Clear Sky Science · fr
La sortiline présente une activité de type suppresseur de tumeur en limitant la fonction de transduction de l’EGFR
Pourquoi cela a de l’importance pour le traitement du cancer
Le cancer du poumon est la première cause de décès par cancer dans le monde, et de nombreux médicaments modernes ciblent une molécule appelée EGFR qui stimule la croissance tumorale. Ces traitements fonctionnent souvent bien au départ, mais les tumeurs deviennent fréquemment résistantes. Cette étude révèle un « frein » naturel à l’intérieur des cellules de cancer du poumon — un rôle inattendu pour une protéine nommée sortiline — qui peut atténuer les signaux pro‑tumoraux de l’EGFR. Comprendre cette relation pourrait aider à expliquer pourquoi certains patients répondent mieux aux thérapies ciblant l’EGFR et suggérer de nouvelles voies pour prolonger l’efficacité de ces traitements. 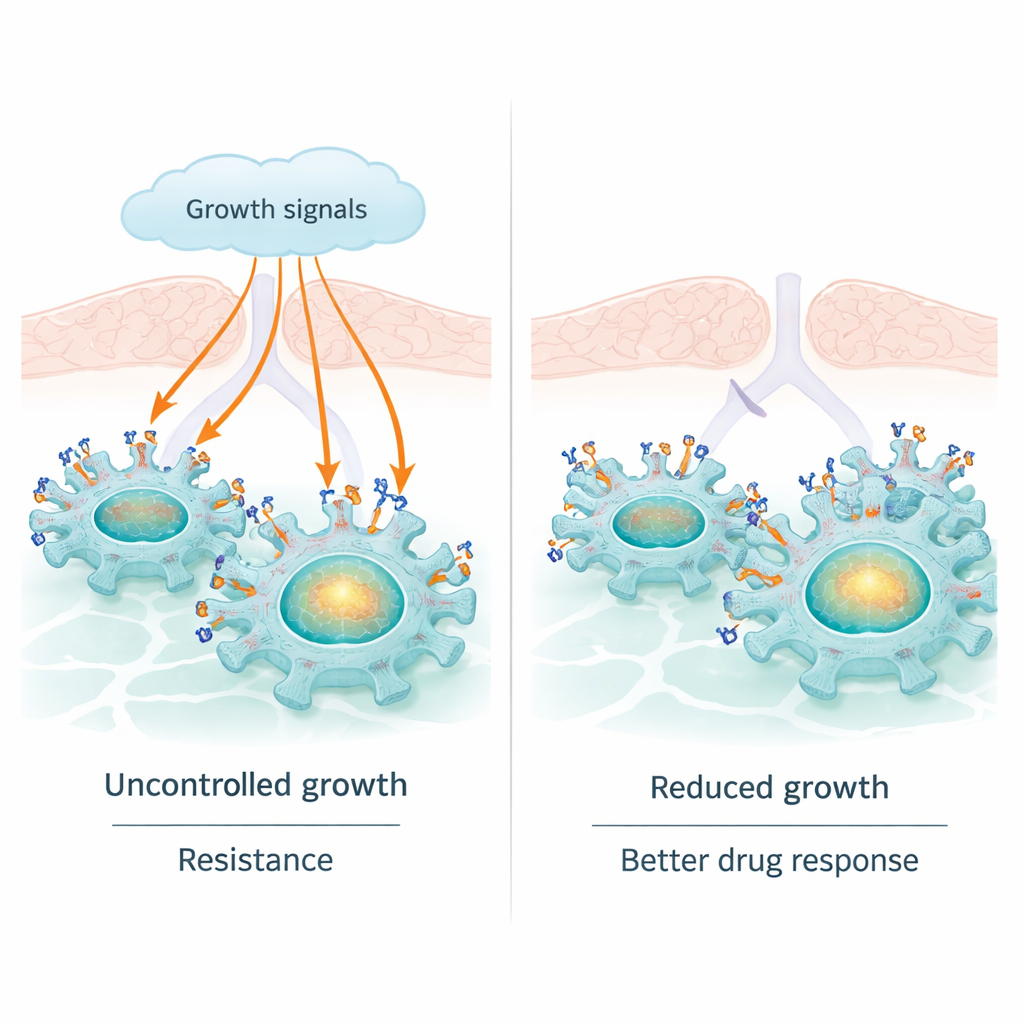
Un commutateur de croissance déréglé
L’EGFR est un récepteur situé à la surface de nombreuses cellules, où il détecte des signaux de croissance provenant de l’environnement. Dans une grande fraction des adénocarcinomes pulmonaires, l’EGFR est altéré de sorte qu’il reste constamment activé. Cela alimente une croissance et une division permanentes, et explique pourquoi les pilules bloquant l’EGFR, appelées inhibiteurs de tyrosine‑kinase, peuvent réduire les tumeurs. Mais l’EGFR a un autre versant, moins connu : il peut migrer dans le noyau cellulaire et agir directement sur l’ADN, activant des gènes tels que cMYC et CCND1 qui renforcent encore la croissance, la survie et la résistance aux traitements. Ce rôle nucléaire de l’EGFR peut aider les tumeurs à échapper même lorsque son activité à la surface est chimiquement bloquée.
La sortiline entre dans le noyau
La sortiline était jusque‑là surtout reconnue comme une protéine de triage qui facilite l’internalisation de l’EGFR depuis la membrane et son envoi vers la dégradation, affaiblissant ainsi ses signaux de croissance. Dans ce travail, les auteurs montrent que la sortiline suit également l’EGFR dans le noyau lorsque les cellules de cancer pulmonaire sont stimulées. Grâce à une microscopie à haute résolution et à une fractionnement biochimique, ils ont observé des complexes EGFR–sortiline se formant à l’intérieur des noyaux peu après l’activation. Fait important, lorsque l’EGFR ne pouvait pas pénétrer dans le noyau, la sortiline restait elle aussi à l’extérieur, ce qui indique que l’EGFR sert de « ticket » à la sortiline pour entrer dans ce compartiment. Une fois là, des complexes EGFR–sortiline ont été retrouvés liés à des segments d’ADN proches des régions de démarrage de gènes clés du contrôle de la croissance, dont cMYC et CCND1.
Un frein intégré sur les gènes du cancer
Pour comprendre la fonction de ces complexes, les chercheurs ont cartographié leurs sites de liaison à l’échelle du génome et mesuré les changements d’activité génique. Ils ont constaté que l’EGFR seul tend à favoriser l’activation des gènes liés à la croissance, tandis que la présence de la sortiline aux mêmes régions d’ADN atténue cet effet. Lorsque les niveaux de sortiline étaient artificiellement réduits, la liaison de l’EGFR aux gènes cibles augmentait, et des gènes oncogéniques comme cMYC et CCND1 devenaient plus actifs. À l’inverse, augmenter les niveaux de sortiline produisait l’effet opposé : l’ancrage de l’EGFR sur l’ADN se relâchait, le recrutement de la machinerie de transcription diminuait, et l’expression de ces gènes oncogéniques baissait. Chez la souris, des tumeurs pulmonaires génétiquement modifiées pour surproduire la sortiline croissaient plus lentement et présentaient des niveaux réduits de cMYC et CCND1. 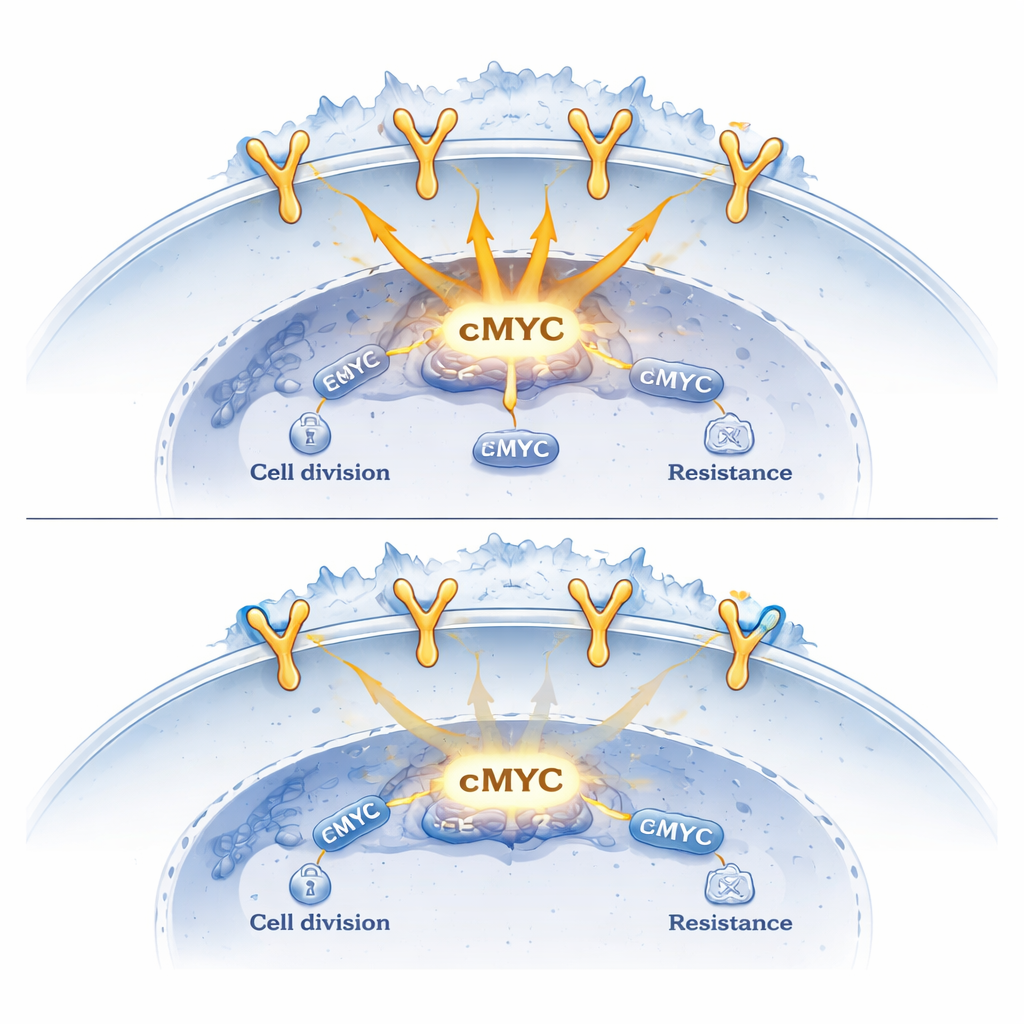
Interaction avec les médicaments ciblant l’EGFR
L’étude a également examiné comment ce mécanisme interagit avec l’osimertinib, un médicament largement utilisé ciblant l’EGFR et conçu pour bloquer les mutations problématiques de l’EGFR. De manière surprenante, même lorsque l’osimertinib inhibait l’activité enzymatique de l’EGFR, le récepteur continuait à migrer vers le noyau. Là, il restait lié à l’ADN, en particulier près du gène cMYC. La sortiline, en revanche, s’accumulait également dans le noyau dans ces conditions. Lorsque la sortiline était abondante, les niveaux de cMYC chutaient plus fortement en réponse à l’osimertinib, et la viabilité des cellules cancéreuses diminuait. L’analyse de tumeurs de patients et de larges jeux de données publiques sur le cancer a montré que les niveaux de sortiline sont souvent plus faibles dans les adénocarcinomes pulmonaires que dans le tissu pulmonaire normal, et qu’une expression plus élevée de sortiline est de façon constante associée à une expression plus faible de cMYC.
Ce que cela implique pour les patients
Pris ensemble, ces résultats décrivent la sortiline comme un partenaire de type suppresseur tumoral qui accompagne l’EGFR dans le noyau puis le restreint. En limitant la capacité de l’EGFR à activer des gènes puissants de croissance tels que cMYC, la sortiline peut ralentir la progression tumorale et renforcer l’effet des médicaments bloquant l’EGFR. Parce que de nombreuses tumeurs pulmonaires présentent une sortiline réduite, elles peuvent manquer de ce frein interne, ce qui contribue à expliquer pourquoi certains cancers sont particulièrement agressifs ou acquièrent rapidement une résistance aux traitements. La mesure des niveaux de sortiline dans les tumeurs pourrait aider à prédire la réponse d’un patient aux thérapies ciblant l’EGFR, et des stratégies visant à augmenter l’activité de la sortiline pourraient offrir une nouvelle voie pour mieux contrôler à long terme les cancers drivés par l’EGFR.
Citation: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
Mots-clés: cancer du poumon, EGFR, sortiline, cMYC, résistance aux thérapies ciblées