Clear Sky Science · fr
RO4938581, un modulateur allostérique négatif du GABAA-α5 a corrigé les phénotypes comportementaux et EEG d’un modèle murin du syndrome Dup15q
Pourquoi cette recherche cérébrale est importante
Le syndrome Dup15q est une affection génétique rare qui provoque souvent de l’autisme, des convulsions et de graves difficultés d’apprentissage. Les familles disposent de peu de mesures au-delà des soins de soutien, et il n’existe pas de traitement s’attaquant à la biologie sous-jacente. Cette étude a utilisé des souris portant le même segment d’ADN supplémentaire que les personnes atteintes de Dup15q pour explorer ce qui dysfonctionne dans le cerveau — et pour tester si un médicament expérimental très ciblé peut atténuer ce problème. Ce travail met en lumière un type précis de récepteur cérébral comme une cible prometteuse et testable pour de futurs médicaments de précision.
Trop de frein dans le cerveau
Nos cerveaux reposent sur un équilibre délicat entre des signaux « go » qui excitent les neurones et des signaux « stop » qui les calment. Dans le syndrome Dup15q, un segment du chromosome 15 est dupliqué. Cette région contient trois gènes qui codent des composants d’un récepteur clé de « stop » dans le cerveau, appelé récepteur GABAA, et en particulier une version contenant une sous-unité nommée alpha-5. Les chercheurs ont conçu des souris avec le même type de duplication et ont constaté que ces animaux produisaient environ 50 % de récepteurs contenant alpha-5 en plus dans des régions cérébrales importantes pour la mémoire, l’émotion et le mouvement, y compris l’hippocampe et le cortex. Plusieurs méthodes — de l’expression génique à l’imagerie des récepteurs — convergent vers la même conclusion : ce système de frein particulier est surdéveloppé dans le modèle Dup15q.
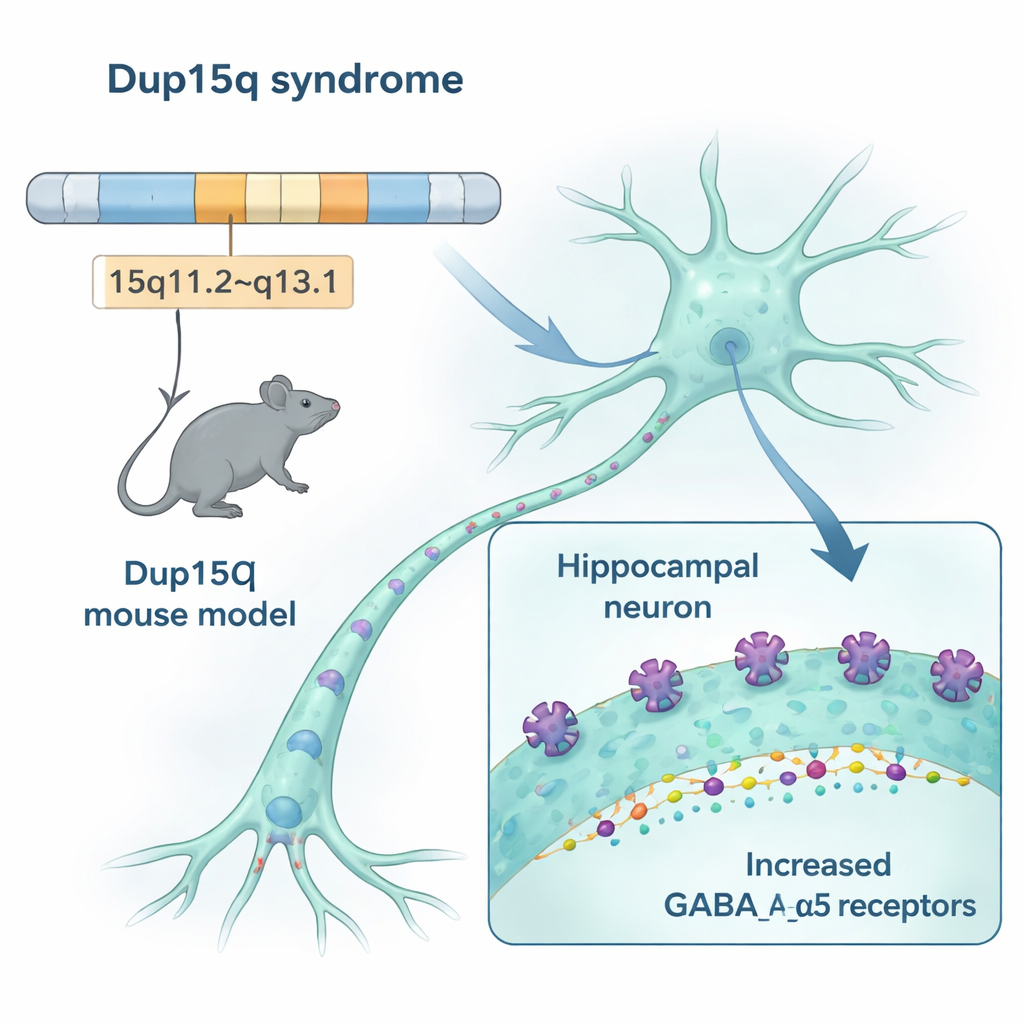
Comment des récepteurs en excès modifient les signaux cérébraux
Avoir davantage de récepteurs de frein n’a d’importance que si cela modifie effectivement le fonctionnement des circuits. Dans de fines coupes d’hippocampe, l’équipe a mesuré les petits courants électriques que les neurones inhibiteurs envoient aux autres cellules. Chez les souris Dup15q, ces courants inhibiteurs survenaient plus fréquemment, suggérant que les neurones subissaient un freinage soutenu plus important, même si l’amplitude de chaque signal individuel restait inchangée. Un autre test du comportement des réseaux, appelé inhibition par paire d’impulsions, a également montré que les réseaux de ces souris étaient plus fortement atténués que ceux de leurs congénères sains. Ensemble, les données indiquent que les récepteurs en excès rendent les circuits inhibiteurs plus dominants, déplaçant l’équilibre et réduisant la souplesse du traitement de l’information.
Comportement et ondes cérébrales chez les souris affectées
Les scientifiques ont ensuite cherché à savoir si ce câblage modifié se traduisait par des comportements rappelant les symptômes humains. Dans une série de tests, les souris Dup15q ont montré des indices de différences sociales et de communication et, de façon plus nette, des difficultés de flexibilité cognitive. Dans une tâche du labyrinthe aquatique, les souris normales et Dup15q ont appris où se trouvait une plate-forme cachée. Mais lorsque la plate-forme a été déplacée, les animaux Dup15q ont été lents à abandonner l’ancien emplacement et à s’adapter au nouveau — un parallèle en laboratoire des routines rigides souvent observées dans l’autisme. L’équipe a aussi enregistré des signaux d’électroencéphalographie (EEG), soit les rythmes sommés de nombreux neurones. Comme chez les personnes atteintes de Dup15q, les souris présentaient une activité inhabituelle renforcée dans la bande bêta, un rythme rapide souvent augmenté par des médicaments qui renforcent les récepteurs GABAA, renforçant l’idée que leur système inhibiteur était hyperactif.
Un médicament ciblé qui relâche le frein
Pour voir s’ils pouvaient normaliser ce sur-freinage, les chercheurs se sont tournés vers RO4938581, un composé expérimental qui affaiblit sélectivement les récepteurs GABAA de type alpha-5 sans affecter les autres formes. Dans des coupes hippocampiques, le médicament a réduit la quantité de transfert de charge inhibitrice dans les neurones Dup15q, compensant l’excès de freinage. Administré chaque jour par voie orale pendant plusieurs semaines, le même composé a amélioré les performances des animaux dans la phase de renversement du labyrinthe aquatique, leur permettant de s’adapter au déplacement de la plate-forme plus comme les souris saines. Il a aussi rapproché leurs interactions sociales de la normale. Lors d’enregistrements EEG, une dose aiguë a partiellement réduit la puissance bêta exagérée chez les souris Dup15q, orientant leurs rythmes cérébraux vers un schéma typique.
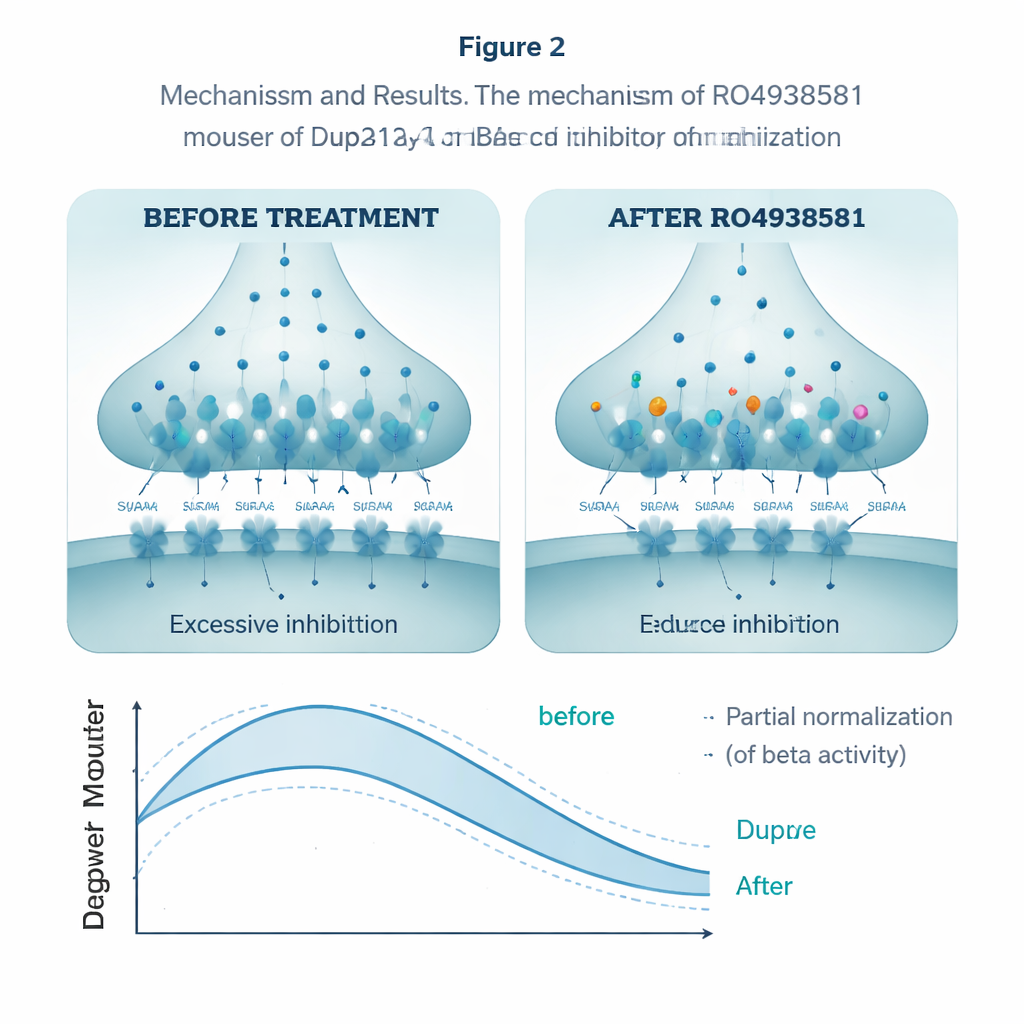
Ce que cela pourrait signifier pour les traitements futurs
Pour les familles vivant avec le syndrome Dup15q, ces résultats ne représentent pas une cure immédiate, mais ils offrent une piste concrète. Le travail identifie un sous-type particulier de récepteur — les récepteurs GABAA contenant l’unité alpha-5 — comme à la fois surproduit et fonctionnellement important dans un modèle animal pertinent. Diminuer modestement l’activité de ce récepteur avec un modulateur négatif comme RO4938581 n’a pas tout résolu, mais a amélioré l’apprentissage flexible, le comportement social et un marqueur EEG clé. Cette combinaison de changements au niveau cérébral, comportemental et du biomarqueur renforce l’argument en faveur d’essais de médicaments ciblant l’alpha-5, plus sûrs et adaptés à l’humain, comme traitements de précision pour Dup15q et potentiellement pour des troubles du neurodéveloppement apparentés.
Citation: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
Mots-clés: syndrome Dup15q, récepteur GABAA alpha-5, trouble du neurodéveloppement, puissance EEG bêta, modèle murin