Clear Sky Science · fr
Microfluidique inertielle en cascade pour l’enrichissement à haut débit et à multi-échelles des cellules tumorales et des amas intacts en vue d’un meilleur diagnostic de la malignité
Pourquoi il est important de trier les cellules cancéreuses dans les liquides
Lorsque le cancer se propage, les cellules tumorales s’échappent souvent dans les liquides qui baignent nos organes. Chez les patients atteints d’un cancer du poumon, cela peut inclure le liquide qui s’accumule autour des poumons, appelé épanchement pleural. Cachées dans ce liquide se trouvent des cellules tumorales rares isolées et des agrégats serrés de cellules. Ces amas sont considérés comme particulièrement dangereux car ils sont fortement associés à une maladie agressive et à de mauvais pronostics. Pourtant, les méthodes de laboratoire actuelles peinent à extraire, de façon douce et efficace, à la fois les cellules isolées et les amas à partir de volumes importants de liquide patient. Cette étude présente une nouvelle technologie sur puce capable de trier rapidement et délicatement ces cellules à partir d’épanchements pleuraux, ouvrant la voie à des diagnostics du cancer plus fiables et à une meilleure compréhension de la dissémination tumorale.
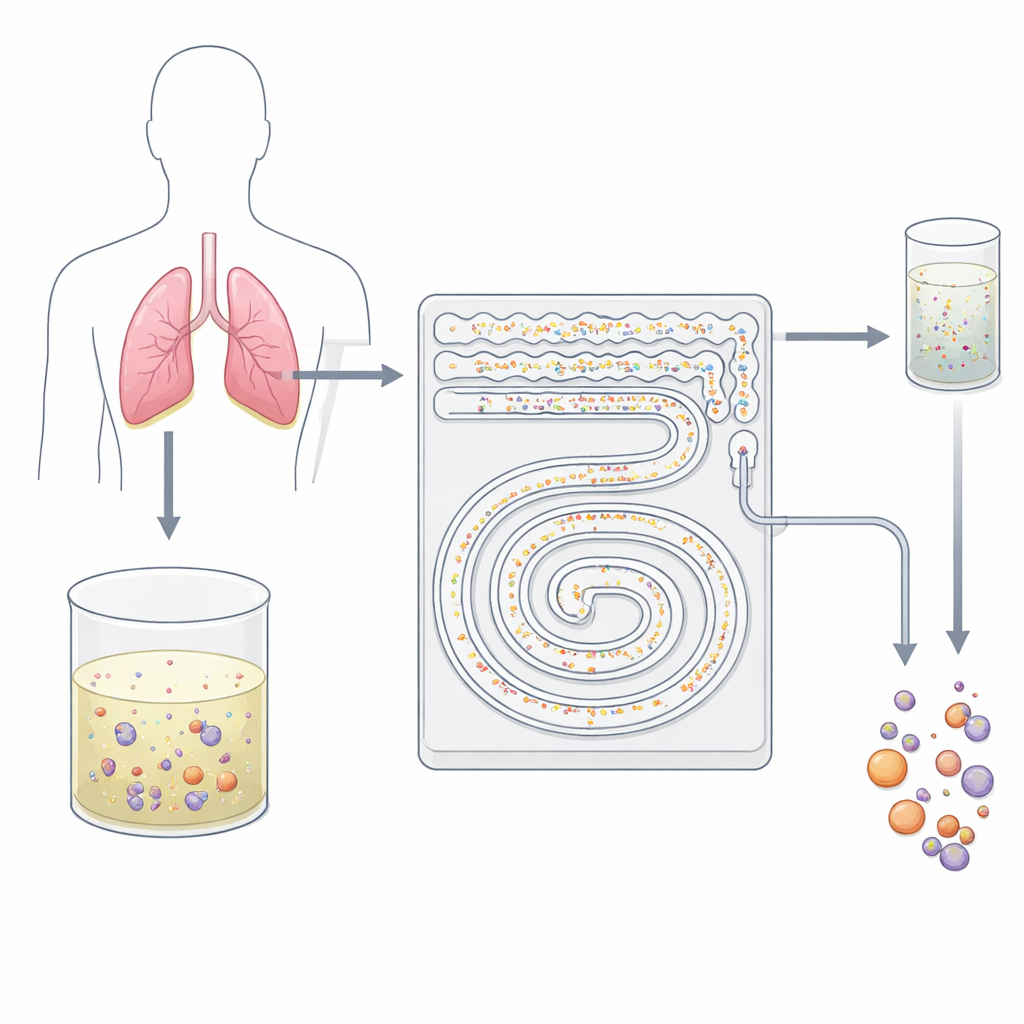
Une « passoire » cellulaire douce sur une puce
Les chercheurs ont conçu un dispositif plastique de la taille de la paume, creusé de microcanaux qui font office de filtre intelligent en deux étapes. Plutôt que d’utiliser des anticorps adhésifs ou des tamis agressifs, la puce exploite le comportement des cellules dans un flux liquide rapide. Lorsque le liquide circule dans des microcanaux courbés, des forces invisibles poussent les particules de tailles différentes vers des lignes d’écoulement distinctes. L’équipe tire parti de cet effet, appelé de manière générale microfluidique inertielle, pour séparer les petites cellules sanguines de fond des cellules tumorales plus grandes et de leurs amas sans contact ni marquage. Comme tout se déroule dans un écoulement continu et fermé, le dispositif peut traiter des dizaines de millilitres de liquide en quelques minutes — ce que la cytologie conventionnelle sur lames ne permet pas facilement.
Première étape : dégager la foule
Dans la première phase du dispositif, l’épanchement pleural — après élimination de l’excès de liquide et remise en suspension des cellules — est poussé à travers un réseau de canaux serpentins parallèles. Là, l’écoulement tourbillonnant et courbé pousse les petits leucocytes vers les parois du canal, tandis que les cellules tumorales plus grandes et les amas restent près du centre du flux. Les petites cellules sont guidées vers des sorties déchets, ce qui réduit considérablement le bruit de fond. Cette étape à haut débit peut fonctionner à environ 8 millilitres par minute, ce qui signifie qu’un échantillon clinique typique de 50 millilitres peut être traité en environ six minutes et demie sans obstruction. Ce qui sort de cette première étape est un mélange beaucoup plus propre, enrichi en cellules potentiellement malignes et prêt pour une séparation plus fine.
Deuxième étape : séparer les cellules individuelles des amas
L’échantillon partiellement enrichi entre ensuite dans un canal en spirale incliné qui présente un motif répétitif de sections étroites et larges. À ce stade, plusieurs forces d’écoulement s’équilibrent différemment selon la taille des objets, les orientant vers des voies distinctes proches de la paroi intérieure ou extérieure de la spirale. Les cellules tumorales individuelles, qui sont plus petites, se rangent à une position latérale, tandis que les amas plus volumineux migrent vers une position différente, plus proche de la paroi intérieure. En plaçant des sorties aux bons endroits, la puce divise physiquement ces flux : une sortie collecte principalement les cellules tumorales isolées, une autre recueille les amas intacts, et d’autres sorties évacuent les petites cellules restantes. Il est important de noter que les amas restent en un seul morceau, évitant les dommages et la fragmentation souvent observés avec des méthodes de filtration traditionnelles.
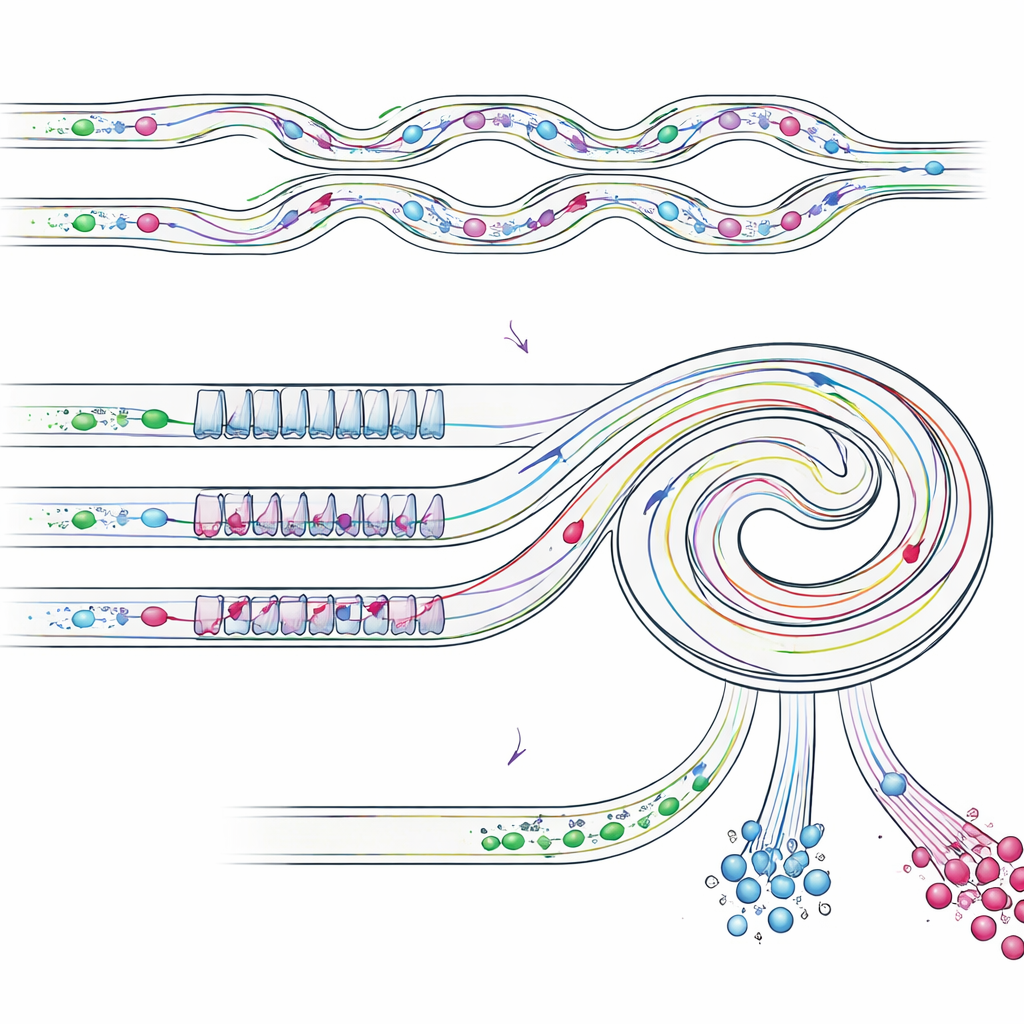
Évaluer le dispositif
Pour vérifier les performances de leur conception, l’équipe a d’abord utilisé des billes en plastique de tailles connues pour imiter des cellules sanguines, des cellules tumorales individuelles et des amas. Ils ont montré que la puce en cascade récupérait plus de 87 % des billes « mono-cellulaires » et environ 92 % des billes « amas », tout en éliminant la plupart des billes « cellules sanguines » plus petites. Ils sont ensuite passés à de véritables cellules de cancer du poumon (cellules A549) mélangées à des leucocytes. Dans ces tests, le dispositif a récupéré environ 82 % des cellules cancéreuses au total, avec environ 76 % de pureté dans la fraction enrichie et près de 80 % de pureté pour les amas cellulaires. Enfin, ils ont traité des échantillons d’épanchement pleural réels provenant de trois patients atteints d’un cancer du poumon. Partant d’un liquide dans lequel les cellules tumorales et les amas représentaient moins de 1 % de toutes les cellules, la puce a produit des fractions où les cellules malignes isolées atteignaient environ 68 % de toutes les cellules, et où les amas constituaient environ 35 % des cellules dans un flux de sortie dédié.
Ce que cela pourrait signifier pour les patients
En n’utilisant que l’écoulement du fluide et la géométrie des canaux, ce dispositif peut rapidement et en douceur extraire à la fois les cellules tumorales isolées et les amas intacts à partir de grands volumes de liquide patient sans étiquettes chimiques ni instruments complexes. Les cellules enrichies restent compatibles avec des tests standard tels que la coloration par immunofluorescence et la microscopie, s’intégrant aisément dans les flux de travail hospitaliers existants. Bien que l’étude actuelle ait impliqué un petit nombre de patients et nécessite des essais plus importants pour démontrer son impact sur le diagnostic et le pronostic, le travail illustre un concept puissant : un « concentrateur de cellules » rapide et sans marquage qui révèle à la fois le nombre et l’état agrégé des cellules tumorales dans les épanchements pleuraux. À long terme, de tels outils pourraient affiner l’évaluation de la malignité, guider les choix thérapeutiques personnalisés et offrir une fenêtre plus claire sur la façon dont les cancers métastasent.
Citation: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Mots-clés: biopsie liquide, tri cellulaire microfluidique, amas de cellules tumorales, épanchement pleural, diagnostic du cancer