Clear Sky Science · fr
Conception d’un système automatisé de microinjection par lots de cellules basé sur des pinces magnétiques pour embryons de poisson zèbre
Pourquoi les œufs de petit poisson sont importants
Avant que de nouveaux médicaments ou des thérapies géniques n’atteignent les humains, les chercheurs les testent souvent sur de petits animaux à croissance rapide. Les embryons de poisson zèbre sont prisés parce qu’ils sont transparents et se développent rapidement, ce qui permet d’observer la formation des organes en temps réel. Mais pour modifier leurs gènes ou administrer des médicaments, il faut injecter chaque œuf délicat avec une aiguille microscopique, une tâche généralement lente, fatigante et fortement dépendante de l’habileté humaine. Cet article présente un nouveau système robotisé capable d’injecter automatiquement des lots d’embryons de poisson zèbre de façon plus rapide, plus douce et plus fiable qu’un opérateur humain, ouvrant la voie à des expériences plus larges et plus cohérentes.
Une nouvelle façon de manipuler des cellules fragiles
La microinjection traditionnelle exige qu’un opérateur formé guide une aiguille en verre sous un microscope, localise chaque embryon, l’oriente correctement et le perce sans endommager les structures vitales. C’est particulièrement difficile car les embryons sont des sphères molles avec des régions importantes qu’il faut éviter pour assurer leur survie. Les systèmes robotiques existants ont aidé à automatiser le transport et la perforation, mais ils ne contrôlent généralement pas la rotation de chaque embryon en trois dimensions. Il en résulte que l’aiguille peut pénétrer selon un angle risqué, diminuant les taux de survie et limitant le nombre d’embryons traitables de façon fiable. L’équipe à l’origine de cette étude s’est donnée pour objectif de construire une plateforme entièrement intégrée capable de transporter, faire tourner, injecter et relâcher les embryons en une séquence fluide, sans changements constants d’objectifs ni ajustements manuels.
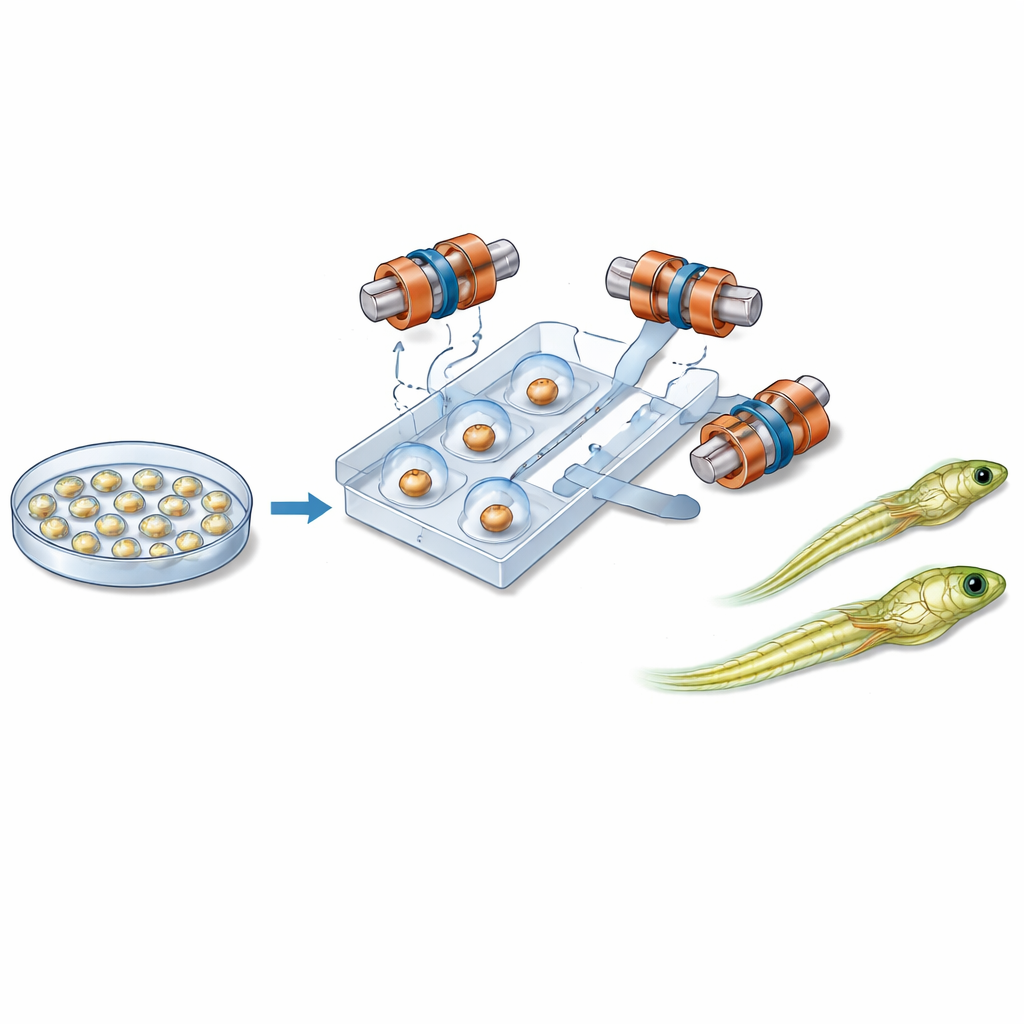
Aimants, microcanaux et commande douce
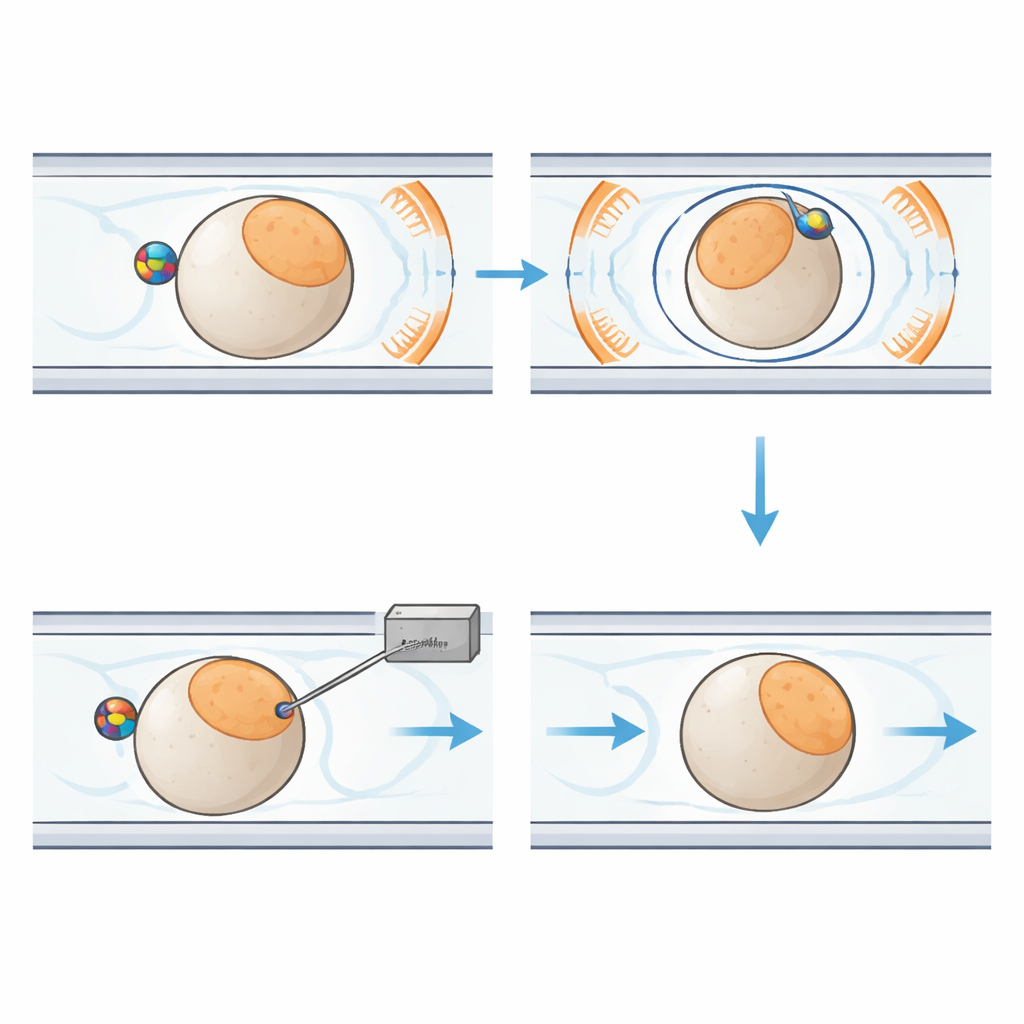
Au cœur du nouveau système se trouve une puce en plastique de la taille de la paume, contenant des canaux étroits qui guident chaque embryon le long d’un trajet fixe. Près de chaque embryon se trouve une petite bille magnétique. Autour de la puce, six bobines soigneusement disposées génèrent un champ magnétique uniforme en trois dimensions. En changeant la direction de ce champ au fil du temps, le système fait tourner la bille. Grâce au frottement entre la bille et la surface de l’embryon, toute la cellule tourne avec elle, comme deux engrenages engagés. Cela permet au robot d’incliner l’embryon hors du plan d’imagerie ou de le faire pivoter dans le plan jusqu’à ce que la région sensible soit positionnée en sécurité, à l’écart de l’aiguille entrante. Des flux liquides et une pression d’air douce déplacent et maintiennent les embryons en place, tandis qu’un module séparé commande l’aiguille d’injection et le minuscule débit de matériel génétique.
Voir clairement dans un champ de vision minuscule
Pour rendre cette chorégraphie précise possible, les chercheurs ont également conçu un système avancé de vision par ordinateur, appelé réseau de perception pour la manipulation microscopique. Il analyse en temps réel les images d’une caméra microscopique pour repérer chaque embryon, détecter la fine pointe de l’aiguille et distinguer les deux « pôles » opposés de l’œuf où se trouvent des structures développementales clés. Le réseau utilise des techniques modernes d’apprentissage profond — telles que des chemins d’extraction de caractéristiques doubles, des modules d’attention qui mettent en valeur les détails importants et une fusion multi-échelle des informations d’image — pour gérer le milieu encombré et faiblement éclairé à l’intérieur d’une puce microfluidique. Dans des tests sur des milliers d’images, il a détecté correctement les objets et segmenté les régions d’embryons avec environ 98–99 % de précision, fournissant le retour fiable nécessaire pour piloter à la fois la rotation magnétique et le positionnement de l’aiguille.
Preuve de fonctionnement sur des poissons zèbre vivants
L’équipe a comparé son système automatisé à des opérateurs humains expérimentés en utilisant 100 embryons de poisson zèbre chacun. Le robot a réalisé ses injections en environ 33,8 secondes par embryon, soit plus du double de la vitesse du travail manuel, et a percé avec succès chaque cellule. Il a également orienté chaque embryon avec une erreur angulaire moyenne de seulement 2,1 degrés, soit à peu près la moitié de l’erreur des opérateurs humains. Surtout, 88 % des embryons injectés par le robot ont survécu jusqu’à l’éclosion en larves, contre 66 % après injection manuelle. Au microscope à fluorescence, les larves issues du système automatisé brillaient en vert, montrant que le matériel génétique introduit avait été incorporé et exprimé comme prévu. En faisant tourner les embryons magnétiquement plutôt qu’en les comprimant avec des outils mécaniques, le système a minimisé la déformation et les dommages tout en maintenant un débit élevé.
Ce que cela signifie pour les études futures
En termes simples, ce travail montre qu’une combinaison soigneusement conçue de microcanaux, de contrôle magnétique et d’analyse d’images intelligente peut injecter des embryons de poisson fragiles plus rapidement et avec une meilleure survie qu’un opérateur qualifié utilisant des outils traditionnels. Parce que le poisson zèbre est une plateforme clé pour étudier le développement, la maladie et les effets des médicaments, un injecteur fiable à haut débit pourrait accélérer les grands criblages génétiques et les études biologiques à long terme qui étaient auparavant limités par le travail manuel. Avec des modifications de conception adaptées à la puce et aux paramètres de contrôle, la même stratégie pourrait être adaptée à d’autres types cellulaires et petits organismes, contribuant à transformer la chirurgie cellulaire délicate, jusqu’ici art réservé à quelques spécialistes, en un processus automatisé et standardisé.
Citation: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
Mots-clés: embryons de poisson zèbre, microinjection, pinces magnétiques, microfluidique, manipulation robotique des cellules