Clear Sky Science · fr
Plate-forme de biosurveillance sans marquage à sensibilité extrême basée sur une nano-optique de phase topologiquement disruptive
Pourquoi voir l’invisible importe
Nombreuses sont les maladies, notamment le cancer et les troubles neurodégénératifs, qui libèrent des molécules indicatrices dans le sang bien avant l’apparition des symptômes. Les tests diagnostiques actuels manquent souvent ces signes précoces parce que les molécules sont trop petites ou trop peu nombreuses pour être détectées de façon fiable. Cet article décrit un nouveau type de capteur optique capable de repérer des quantités infimes de ces biomolécules sans recourir à des marqueurs fluorescents ni à des étiquettes chimiques. En concevant la matière à l’échelle de quelques atomes, les auteurs exploitent des décalages subtils de la lumière pour convertir de très petits événements biochimiques en signaux importants et faciles à mesurer.
Transformer la lumière en détecteur ultra-sensible
Les biocapteurs plasmoniques classiques fonctionnent en éclairant un film métallique mince et en surveillant comment la lumière réfléchie change lorsque des molécules se déposent à la surface. Ces dispositifs sont déjà sensibles, mais peinent avec des molécules très petites ou des concentrations extrêmement faibles. Plutôt que de suivre l’intensité ou la couleur, la nouvelle plate-forme se concentre sur la phase de la lumière — le timing précis de son onde. Dans des conditions particulières, la lumière réfléchie tend presque à disparaître et sa phase varie extrêmement rapidement. Ces points, connus sous le nom d’états optiques « sombres » ou de singularités de phase, rendent le système extraordinairement réactif à de légers changements à proximité de la surface métallique.
Construire un piège optique à l’échelle nanométrique
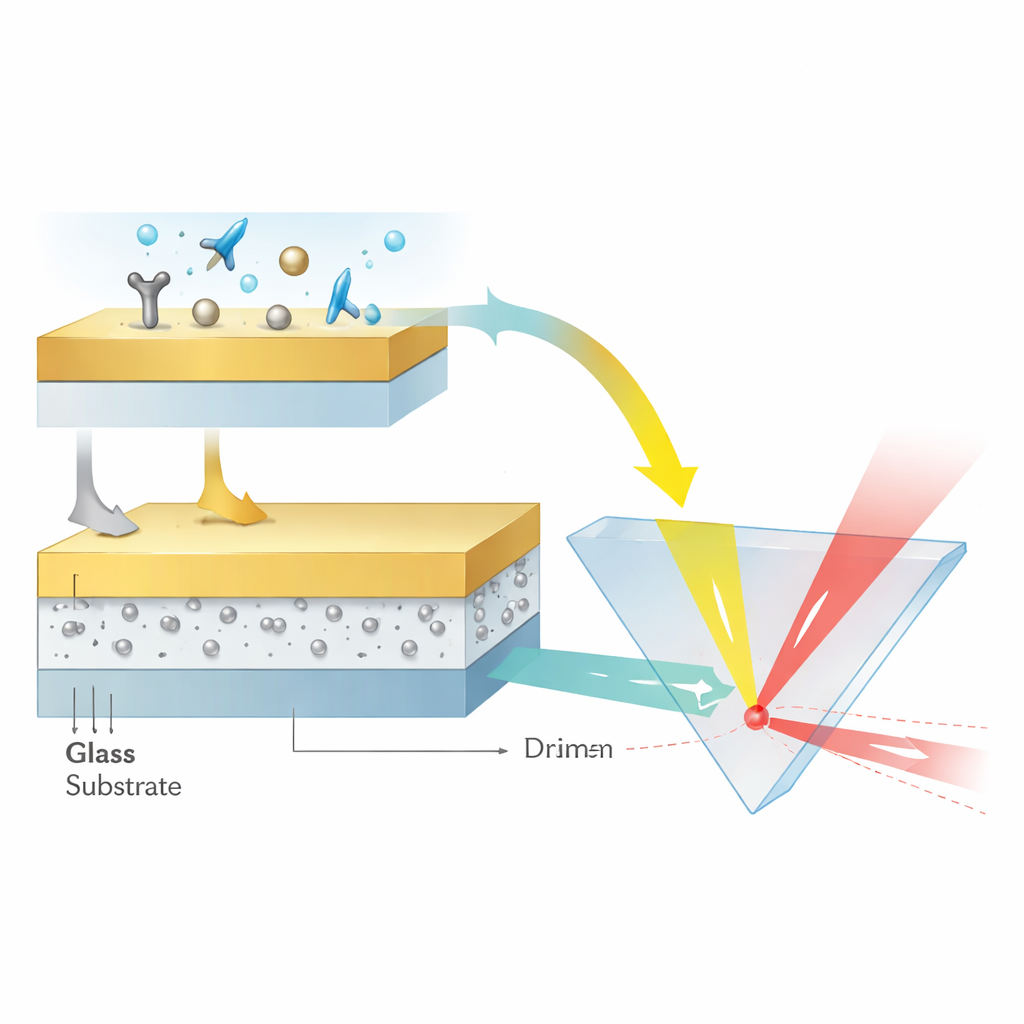
Pour créer ces singularités, l’équipe a conçu une structure stratifiée de seulement quelques dizaines de nanomètres d’épaisseur. Une base en verre soutient une couche d’oxyde d’aluminium de 12 nanomètres contenant de très petites nanoparticules d’argent de moins de 3 nanomètres de diamètre, le tout recouvert par un film d’or lisse de 48 nanomètres. Les particules d’argent sont générées et incorporées avec soin afin de rester cristallines, quasi sphériques et espacées de manière uniforme à des distances sub-nanométriques. Cet arrangement permet aux modes plasmon localized des particules de coupler fortement entre eux et avec les ondes plasmoniques se propageant dans la couche d’or. Le résultat est une sorte de cavité optique nanométrique où l’énergie lumineuse est fortement confinée et où la phase devient extrêmement sensible au milieu environnant.
Faire glisser la lumière latéralement
Plutôt que de mesurer des angles ou des couleurs, les auteurs lisent la réponse de leur capteur en suivant le décalage latéral le long de la surface du faisceau de lumière réfléchi — un phénomène appelé décalage de Goos–Hänchen. Lorsqu’un faisceau laser est réfléchi dans les bonnes conditions, son pic d’énergie peut émerger légèrement décalé de l’endroit prédit par la géométrie simple. Près d’une singularité de phase, ce déplacement croit de façon spectaculaire. En ajustant la concentration de nanoparticules d’argent à environ 16 pour cent, l’équipe a poussé la réflectivité près de zéro et accentué le saut de phase jusqu’à ce que de minuscules changements d’indice de réfraction, causés par la liaison de molécules à la surface d’or, produisent des déplacements latéraux du faisceau de l’ordre de centaines de micromètres. Dans des tests d’étalonnage utilisant des solutions diluées de glycérine, l’appareil a atteint une sensibilité équivalente à 3,27 × 10^8 nanomètres de décalage de faisceau par unité de changement d’indice de réfraction et a résolu des variations aussi faibles qu’environ quatre parties par dix millions.
Détecter des molécules minuscules à des concentrations quasi nulles
Pour démontrer l’intérêt pratique en biosurveillance, les chercheurs ont d’abord ciblé la biotine, une molécule de la taille d’une vitamine possédant un très faible poids moléculaire. Les capteurs plasmoniques de surface standard ne peuvent pas voir la biotine de façon fiable même à l’échelle micromolaire. Ici, en décorant la surface d’or avec de la streptavidine, qui lie fortement la biotine, la nouvelle plate-forme a suivi clairement l’association en temps réel à des concentrations aussi faibles que 1 femtomolaire — soit approximativement une molécule parmi 10^15 molécules de solvant. Le signal augmentait régulièrement à chaque multiplication par dix de la concentration, confirmant que le décalage du faisceau évolue de façon prévisible avec la couverture de ces analytes minimes.
Chasser les marqueurs du cancer à l’échelle attoseconde
L’équipe s’est ensuite tournée vers une cible d’intérêt clinique : le facteur de nécrose tumorale alpha (TNF-α), une cytokine associée à l’inflammation et au cancer, présente dans le sérum des patients à environ 10^−13 molaire. Ils ont fonctionnalisé la surface d’or avec de courts brins d’ADN (aptamères) qui captent spécifiquement le TNF-α et bloqué les zones restantes pour réduire les liaisons non spécifiques. Dans ces conditions, le capteur a enregistré des signaux clairs et stables pour le TNF-α à des concentrations aussi faibles que 0,1 attomolaire (10^−19 molaire) et a produit un décalage de près de 47 micromètres à 10^−13 molaire, soit bien dans la plage pertinente médicalement. Des tests témoins avec une autre cytokine, l’interleukine-6, ont donné presque aucun signal durable, confirmant que la réponse était à la fois très sensible et sélective.
Ce que cela signifie pour les futurs tests médicaux
En termes simples, ce travail montre que des nanoparticules d’argent soigneusement organisées sous une fine couche d’or peuvent convertir un changement presque imperceptible à la surface en un grand mouvement latéral de la lumière, facile à mesurer. En opérant aux singularités de phase, la plate-forme évite le besoin de marqueurs fluorescents et pousse la sensibilité dans les régimes zépto- à attomolaires pour des cibles biologiques réelles. Si cela se traduit en dispositifs robustes et conviviaux, de tels capteurs pourraient permettre des analyses sanguines détectant des marqueurs de maladie bien plus tôt que les méthodes actuelles, ouvrant de nouvelles fenêtres pour un diagnostic précoce et une surveillance en temps réel de la santé.
Citation: Du, F., Gireau, M., Youssef, J. et al. Extreme sensitivity label-free biosensing platform based on topologically disruptive phase nano-optics. Microsyst Nanoeng 12, 106 (2026). https://doi.org/10.1038/s41378-026-01222-3
Mots-clés: biosurveillance sans marquage, capteur plasmonique, nanoparticules, détection précoce des maladies, biomarqueurs du cancer