Clear Sky Science · fr
Feuillets hybrides WS2 dopés au Cu et PEGylés pour une thérapie multimodale ciblée du cancer
Pourquoi des traitements du cancer plus intelligents comptent
De nombreuses personnes atteintes d’un cancer du sein subissent encore des traitements agressifs qui peuvent endommager les tissus sains sans éliminer complètement la tumeur. Cette étude décrit un nouveau type de feuillet ultra‑petit, trop petit pour être vu à l’œil nu, conçu pour circuler dans l’organisme, cibler les tumeurs mammaires et les attaquer de façon coordonnée par plusieurs mécanismes. En combinant chaleur, chimie et un médicament anticancéreux classique dans un seul dispositif ciblé, les chercheurs cherchent à rendre le traitement à la fois plus puissant et moins nocif pour le reste du corps. 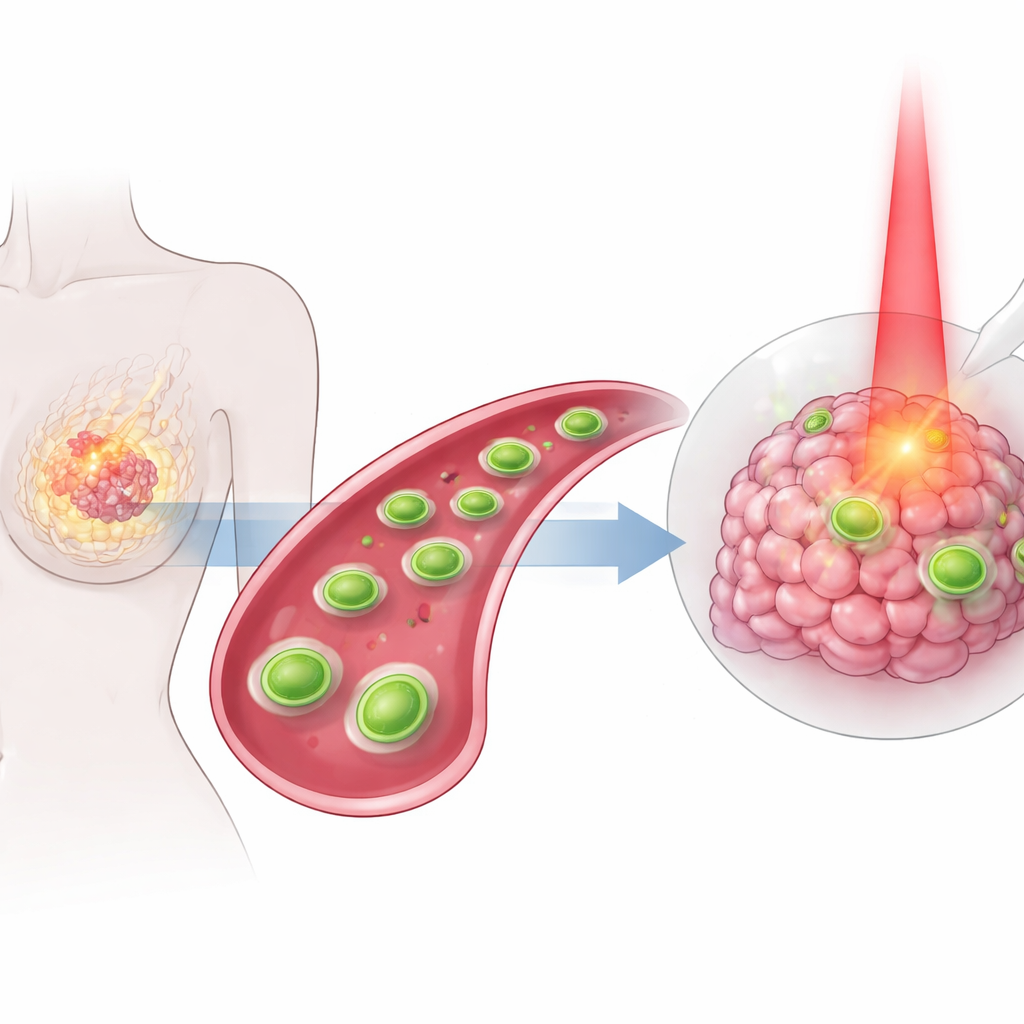
De minuscules feuillets conçus pour transporter et délivrer un traitement
Le cœur de l’approche est un matériau ultra‑fin composé de tungstène et de soufre, façonné en feuillets de taille nanométrique. Ces feuillets absorbent naturellement la lumière proche infrarouge et la transforment en chaleur. L’équipe a d’abord synthétisé ces feuillets puis a texturé leur surface de manière à pouvoir accueillir d’autres composants utiles. Des atomes de cuivre ont été ancrés de façon hautement dispersée sur les feuillets, et un revêtement souple et flexible, semblable à un « imperméable » moléculaire, a été ajouté pour améliorer la dispersion des particules dans les fluides corporels et éviter l’agrégation. Enfin, ils ont fixé de l’acide folique — une vitamine que de nombreuses cellules tumorales captent avidement — comme dispositif de ciblage, et chargé la doxorubicine, un médicament de chimiothérapie courant, sur la surface. Le résultat final est une plateforme minuscule et stratifiée pouvant circuler dans le sang, reconnaître les cellules tumorales et transporter une cargaison importante de traitement.
Comment la lumière, la chimie et le médicament agissent ensemble
Une fois ces particules arrivées dans une tumeur, plusieurs phénomènes se produisent simultanément. Lorsqu’on illumine la zone tumorale à l’aide d’un laser rouge doux, les feuillets tungstène–soufre chauffent efficacement, augmentant localement la température suffisamment pour stresser et endommager les cellules cancéreuses sans surchauffer le reste du corps. Parallèlement, les atomes de cuivre sur les feuillets réagissent avec des molécules de peroxyde naturellement présentes à des niveaux plus élevés dans les tumeurs. Cette réaction transforme le peroxyde en oxydants très réactifs et de courte durée de vie qui perforent les constituants cellulaires de l’intérieur. Les tumeurs tendent aussi à être légèrement plus acides que les tissus sains ; dans cet environnement plus acide, et sous l’effet de la chaleur du laser, la liaison entre le feuillet et la doxorubicine s’affaiblit, permettant une libération accrue du médicament précisément là où il est nécessaire. Ces trois effets — chaleur, attaque chimique et chimiothérapie ciblée — sont conçus pour se renforcer mutuellement. 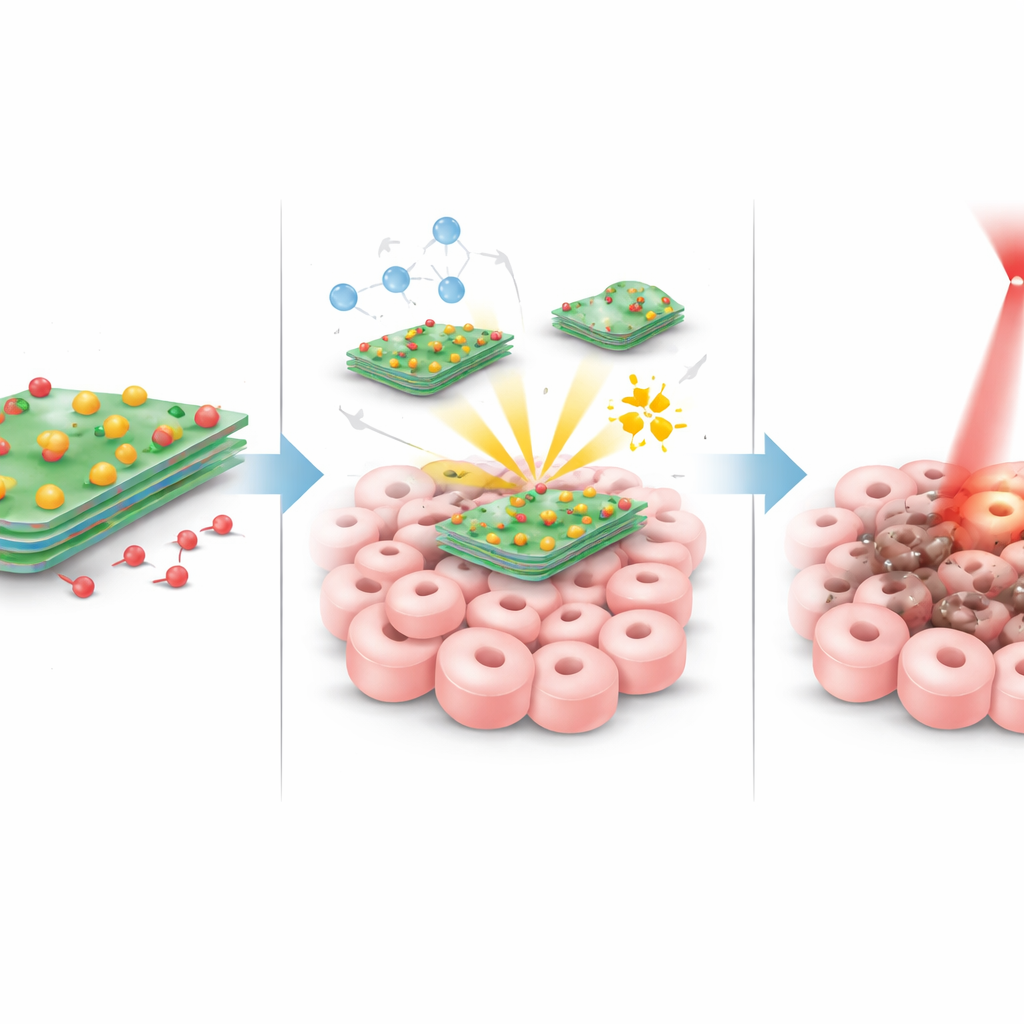
Preuves issues de cellules et de souris porteuses de tumeurs
En culture cellulaire, les feuillets revêtus seuls ont montré peu de toxicité pour les cellules normales, suggérant une sécurité de base satisfaisante. Mais lorsqu’ils étaient chargés en doxorubicine et exposés au laser en présence de peroxyde, ils induisaient une forte mortalité des cellules du cancer du sein, bien supérieure à celle obtenue par un traitement isolé. Les chercheurs ont également démontré que les particules génèrent une poussée d’oxydants réactifs à l’intérieur des cellules tumorales, confirmant l’activité de la chimie du cuivre. Chez des souris porteuses de tumeurs mammaires, les particules dotées du revêtement à l’acide folique s’accumulaient beaucoup plus fortement et plus longtemps dans les tissus tumoraux que les particules non ciblées. Lorsque les souris recevaient la combinaison complète — particules ciblées plus exposition à la lumière rouge — leurs tumeurs ont nettement régressé, leur durée de survie s’est allongée et leur poids corporel ainsi que la santé de leurs organes sont restés globalement normaux, indiquant des effets secondaires limités comparés au traitement standard.
Ce que cela pourrait signifier pour les soins du cancer à l’avenir
Pris ensemble, ces résultats suggèrent que ces feuillets ingénierés agissent comme un outil multifonction pour le traitement du cancer : ils localisent les tumeurs, les chauffent, les empoisonnent de l’intérieur via une chimie réactive et délivrent un médicament éprouvé de manière plus précise, tout en épargnant une grande partie du reste de l’organisme. Le travail en est encore au stade des études animales, et des questions importantes demeurent concernant la sécurité à long terme, la dégradation et la meilleure manière de produire ces particules pour un usage humain. Cependant, le concept montre qu’en combinant plusieurs traitements modestes dans un seul dispositif intelligent adapté à l’environnement tumoral, on peut obtenir un effet global beaucoup plus fort. Si des études futures confirment leur innocuité et leur efficacité, de telles nanoplates‑formes multifonctionnelles pourraient contribuer à rendre la thérapie du cancer du sein plus ciblée, plus efficace et moins pénible pour les patientes.
Citation: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
Mots-clés: thérapie du cancer du sein, nanomédecine, traitement photothermique, targeted drug delivery, thérapie chémodynamique