Clear Sky Science · fr
Système robotique de transport cellulaire basé sur la modélisation de la résistance des micropipettes
Déplacer de minuscules cellules sans microscope
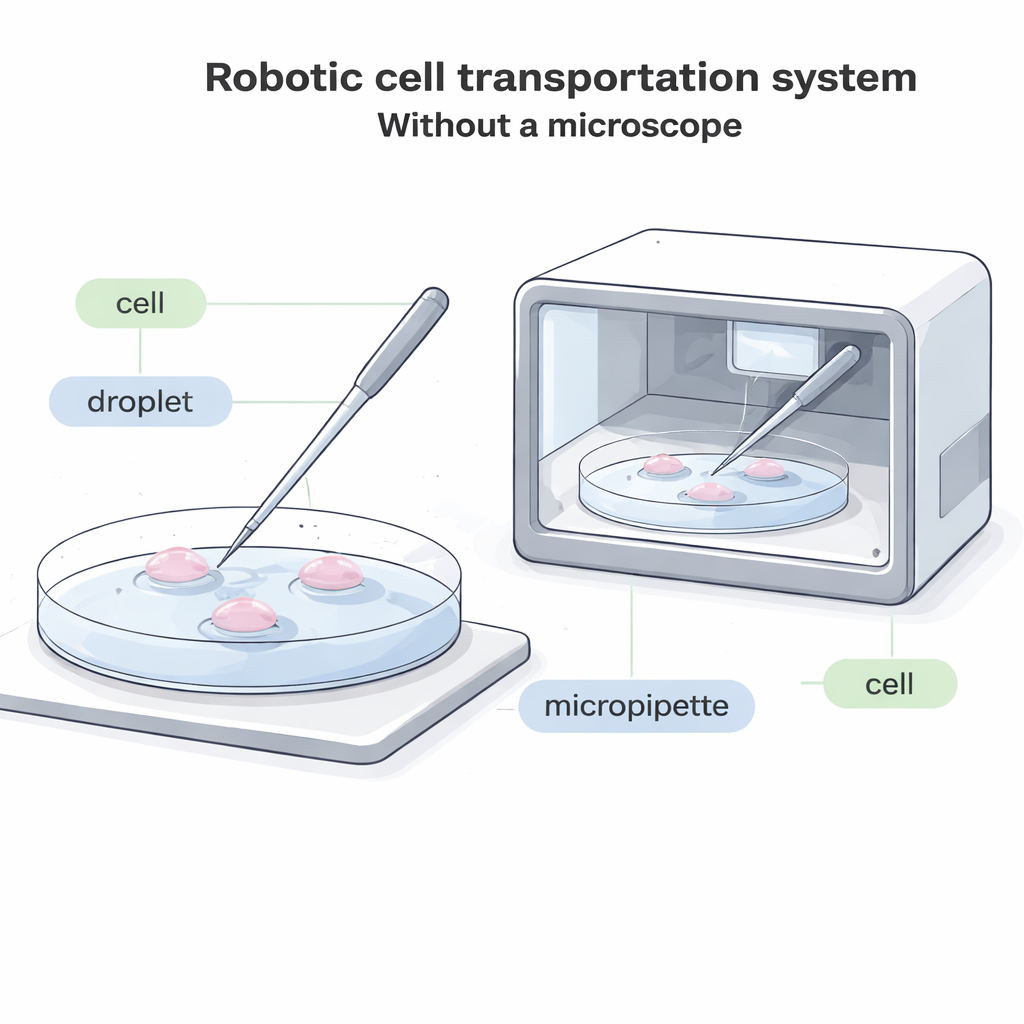
La biologie moderne dépend souvent d’une tâche étonnamment simple : prélever une seule cellule avec un tube en verre et la déposer ailleurs. Ceci est essentiel pour les traitements de fertilité, la congélation d’embryons, les thérapies à base de cellules et la recherche fondamentale. Pourtant, aujourd’hui, cela nécessite presque toujours un microscope encombrant et un opérateur humain très qualifié qui surveille chaque mouvement. Cet article décrit un nouveau système robotique capable de transférer des cellules uniques entre des gouttes de liquide sans aucune vue microscopique, ouvrant la voie à des « usines cellulaires » entièrement closes et automatisées, plus rapides, moins coûteuses et moins dommageables pour des cellules fragiles.
Pourquoi le transfert cellulaire a besoin d’un renouvellement
Dans les laboratoires actuels, un opérateur regarde au microscope et utilise un tube de verre fin, appelé micropipette, pour se poser sur le fond d’une boîte, aspirer délicatement une cellule, la déplacer vers une nouvelle goutte de fluide, puis la rejeter. Ce processus est lent, exigeant sur le plan visuel et difficile à automatiser. Dans de nombreux systèmes futurs — comme des dispositifs compacts et scellés qui font croître des embryons ou d’autres cellules à l’intérieur d’une enceinte — il n’y a tout simplement pas assez de place pour un microscope traditionnel. Dans d’autres cas, les cellules sont marquées par des colorants fluorescents qui peuvent s’estomper ou être endommagés par la lumière, si bien qu’il est important de limiter l’observation lumineuse au microscope. Les systèmes « à l’aveugle » existants qui ne reposent pas sur des images ne fonctionnent que pour des cellules exceptionnellement grandes, laissant la plupart des types cellulaires courants sans bonne solution automatisée.
Une paille spéciale avec un arrêt intégré
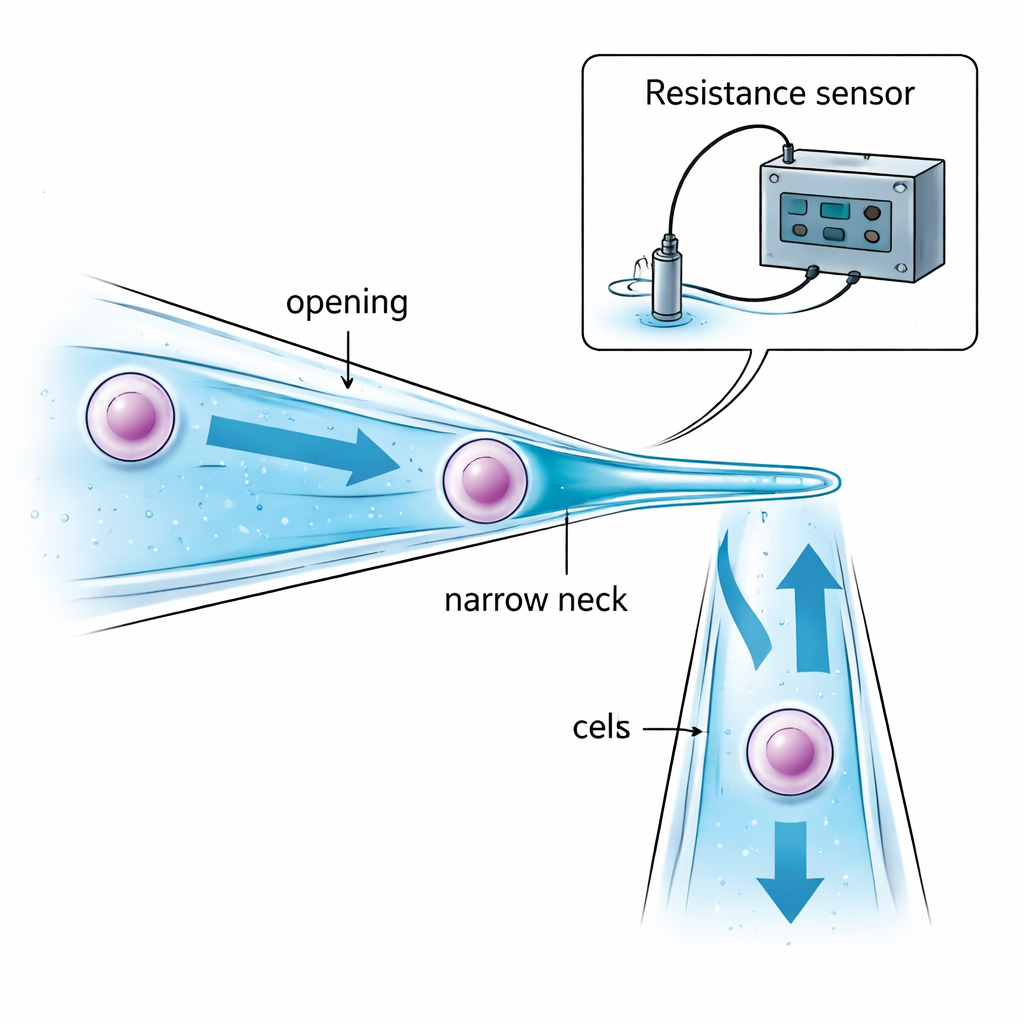
Les auteurs s’attaquent au problème en repensant la micropipette elle-même. Au lieu d’un tube de verre droit d’un diamètre constant, ils conçoivent une micropipette à col étroit. Son ouverture est légèrement plus large que la cellule cible afin que la cellule puisse y être aspirée. Plus en profondeur, le tube se rétrécit doucement vers un « col » plus petit que la cellule. Quand la succion attire la cellule vers cette constriction, la cellule est stoppée et maintenue à l’intérieur du tube — au lieu de pendre à la pointe et d’être exposée à l’huile ou à l’air entre les gouttes. Un choix soigneux du diamètre d’ouverture, de la taille du col et de la distance entre eux garantit que la cellule peut être capturée solidement sans être trop comprimée, et que seule une faible quantité de liquide est transportée d’une goutte à l’autre, réduisant la contamination.
Écouter des signaux électriques au lieu de regarder
Sans microscope, le robot doit tout de même connaître trois choses : quand la pointe de verre est suffisamment proche du fond de la boîte, quand la cellule a été capturée avec succès au niveau du col, et quand elle a été complètement relâchée dans la nouvelle goutte. L’équipe résout cela en surveillant de minuscules variations de résistance électrique dans le liquide à l’intérieur et autour de la micropipette. À mesure que la pipette inclinée approche du fond, l’espace de liquide entre elles diminue et la résistance électrique augmente de manière prévisible, signalant un atterrissage sûr juste avant le contact. Lorsqu’une cellule bouche le col étroit, le chemin électrique à travers le liquide se restreint et la résistance bondit soudainement ; lorsque la cellule est repoussée, la résistance chute tout aussi brusquement. Des modèles mathématiques de ces résistances de « gap », d’« aspiration » et d’« injection » permettent à un ordinateur d’interpréter ces signaux en temps réel et de décider quand arrêter la succion ou appliquer de la pression, le tout sans retour visuel.
Mettre le robot à l’épreuve
Pour vérifier si cette approche fonctionne en pratique, les chercheurs ont construit un système robotique complet combinant contrôle de mouvement, régulation de pression, détection de résistance et un ordinateur hôte. Ils l’ont testé sur de petites cellules cancéreuses connues sous le nom de cellules HeLa (environ 10 micromètres de diamètre) et sur des ovocytes porcins beaucoup plus grands (environ 150 micromètres). Le système a pu détecter de manière fiable l’atterrissage, la capture et le relâchement uniquement à partir des signaux de résistance sur une large gamme de tailles de pipettes. Dans des comparaisons directes, le robot a déplacé les cellules HeLa avec un taux de réussite de 90 % — meilleur qu’une méthode automatisée basée sur la vision antérieure — et a transporté les ovocytes porcins avec un taux de réussite de 95 %, supérieur à une approche standard guidée au microscope. Les temps d’opération par cellule étaient similaires ou plus rapides que les méthodes contrôlées par des humains, principalement parce que le col étroit supprime le besoin d’ajustements répétés et fins de la succion pour positionner la cellule.
Préserver la viabilité des cellules et monter en échelle
Tout assistant robotique en laboratoire doit éviter d’endommager les cellules qu’il manipule. Après transport par le nouveau système, tant les cellules HeLa que les ovocytes porcins ont été cultivés pendant une journée puis colorés avec un colorant qui n’émet que dans les cellules vivantes. Les taux de survie pour la nouvelle méthode étaient équivalents ou proches de ceux obtenus par transfert traditionnel guidé au microscope et par des cellules témoins non manipulées, indiquant que la légère compression mécanique au niveau du col n’affecte pas notablement la viabilité cellulaire lorsque les seuils sont correctement réglés. Pour l’avenir, les auteurs suggèrent que la même détection par résistance et le même contrôle de pression peuvent être intégrés dans des puces microfluidiques compactes. Cela permettrait de faire fonctionner de nombreux canaux en parallèle, rendant possible une manipulation cellulaire entièrement fermée et à haut débit, adaptée à la médecine reproductive automatisée, aux thérapies cellulaires et aux dispositifs de culture cellulaire à long terme où les microscopes ne peuvent pas facilement accéder.
Ce que cela signifie pour le travail cellulaire futur
Pour les non-spécialistes, le message principal est que le déplacement de cellules uniques n’a plus besoin d’être dépendant d’une personne regardant au microscope. En façonnant avec soin un tube de verre et en « écoutant » la façon dont l’électricité circule dans le liquide environnant, un robot peut sentir quand il a atterri, attrapé une cellule et relâché — le tout dans l’obscurité et dans des espaces confinés. Cela rend beaucoup plus pratique la conception de systèmes de culture cellulaires fermés et autonomes qui protègent des échantillons fragiles, simplifient les flux cliniques et rapprochent la manipulation cellulaire de qualité laboratoire d’une exploitation automatisée de type usine.
Citation: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Mots-clés: manipulation cellulaire, micropipette, robotique, microfluidique, automatisation