Clear Sky Science · fr
Stratégies pour contrôler l’organisation spatiale cellulaire dans les systèmes microphysiologiques
Construire de minuscules tissus en laboratoire
Nos organes fonctionnent si bien parce que leurs cellules ne sont pas réparties au hasard : elles sont soigneusement disposées dans l’espace. Cet article explore comment les scientifiques apprennent à recréer cet ordre complexe à l’intérieur des « organes-sur-puce » et d’autres tissus miniatures cultivés en laboratoire. En guidant la position des différents types cellulaires et leurs interactions, les chercheurs peuvent construire des modèles plus réalistes du cœur, du cerveau, de l’intestin, des vaisseaux sanguins et même des écosystèmes humains–microbiens. Ces systèmes avancés promettent des tests de médicaments plus sûrs, moins d’expériences animales et de meilleurs outils pour étudier les maladies et développer des traitements personnalisés.
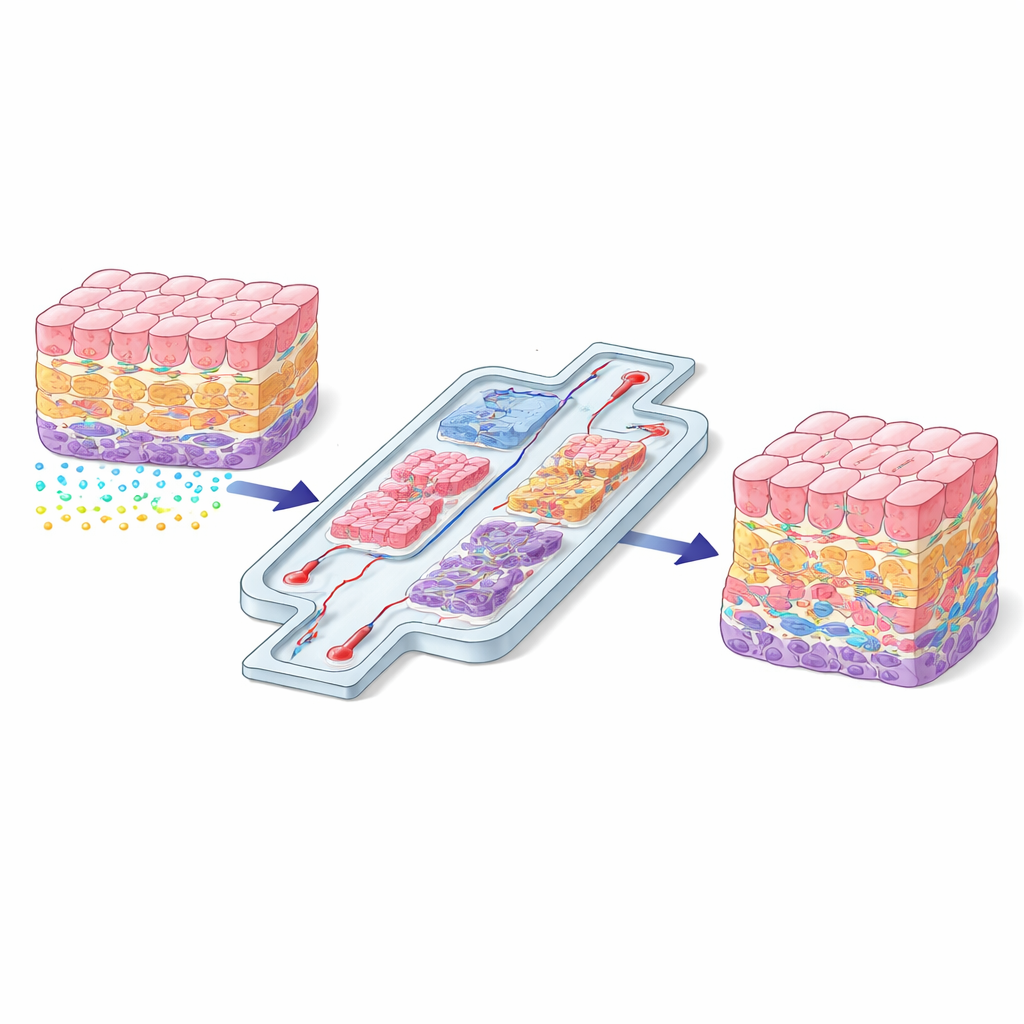
Pourquoi la position des cellules compte
Dans le corps, chaque cellule vit dans un « quartier » spécifique avec sa propre combinaison de structures de soutien, de signaux chimiques et de forces physiques. Une cellule hépatique proche d’un vaisseau sanguin reçoit des signaux très différents d’une cellule enfouie au cœur de l’organe. Ces différences de localisation contribuent à déterminer comment les cellules se développent, en quoi elles se différencient et comment elles répondent à une lésion ou à un médicament. Lorsque les scientifiques cultivent des cellules sur des boîtes de plastique planes, cette « conversation » spatiale est en grande partie perdue et les cellules se comportent souvent de façon non naturelle. L’article soutient que recréer une organisation spatiale réaliste n’est pas une amélioration optionnelle mais une exigence fondamentale si les tissus cultivés en laboratoire doivent imiter les organes réels.
Deux grandes approches pour disposer les cellules
Les auteurs regroupent les stratégies actuelles en deux familles larges : le contrôle direct et le contrôle indirect. Les méthodes directes placent physiquement les cellules ou les compartiments exactement là où ils sont nécessaires. On y trouve la bio-impression 3D, qui dépose des couches de cellules et d’hydrogels comme une imprimante biologique ; les puces microfluidiques qui façonnent des tissus en chambres et canaux connectés ; et les méthodes de piégeage physique qui placent les cellules à l’aide de la lumière, du son, d’aimants ou de champs électriques. Ces approches sont particulièrement efficaces lorsque la géométrie précise est cruciale — par exemple pour recréer une barrière hémato-encéphalique, une paroi vasculaire stratifiée ou le trajet de flux de l’intestin vers le foie.
Laisser les cellules lire leur environnement
Les méthodes indirectes, elles, modifient l’environnement et laissent les cellules faire le reste. Ici, les scientifiques ajustent le « paysage » perçu par les cellules : la composition du gel environnant, la rigidité et la texture des surfaces, ainsi que les gradients de substances dissoutes comme des facteurs de croissance ou des médicaments. Des molécules de soutien disposées avec soin peuvent amener certains types cellulaires à se localiser dans des régions spécifiques. Des hydrogels intelligents qui s’assouplissent ou libèrent des signaux lorsque les cellules les remodèlent favorisent des structures auto-organisées telles que des réseaux vasculaires ou des cryptes et villosités de type intestinal. Les dispositifs microfluidiques peuvent générer des gradients chimiques stables qui poussent des cellules souches à adopter différentes identités le long d’un canal, ou qui amènent des cellules cancéreuses et des cellules immunitaires à migrer vers des zones distinctes, révélant ainsi comment les maladies se propagent.
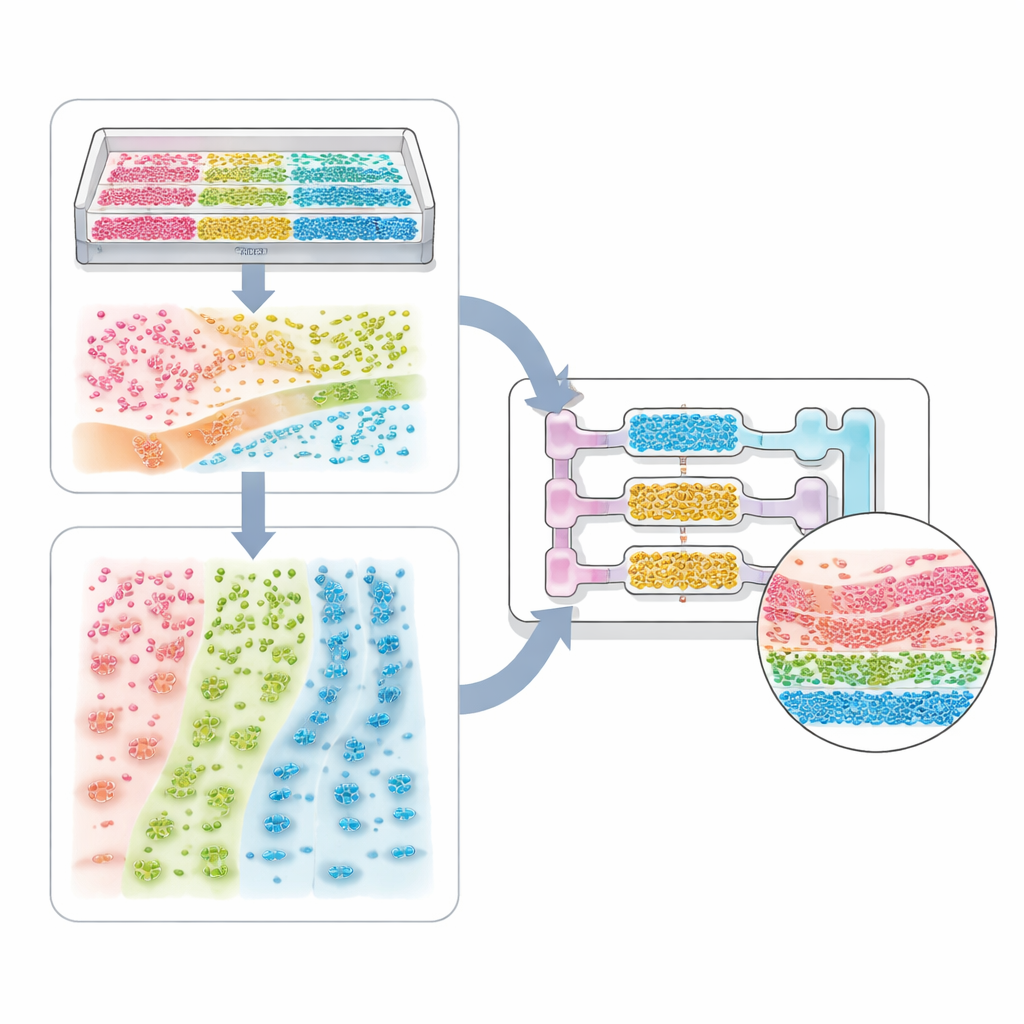
Des systèmes à cellule unique aux modèles corps-entier
La revue parcourt un spectre d’applications. À l’extrémité la plus simple se trouvent les systèmes à type cellulaire unique, où des rainures structurées ou des gradients de rigidité peuvent synchroniser les battements de cellules cardiaques ou aligner les prolongements des neurones. Les modèles tissulaires plus complexes mêlent plusieurs types cellulaires — par exemple des cellules tumorales, des cellules de soutien et des cellules endothéliales — pour former des sphéroïdes et organoïdes avec des noyaux et des couches distincts. Des puces à microcanaux et la bio-impression ajoutent ensuite des limites et du flux, permettant de recréer les alvéoles pulmonaires, les filtres rénaux, les zones hépatiques et des circuits multi-organes qui suivent l’absorption, la transformation et l’élimination d’un médicament. Les mêmes idées s’appliquent aux systèmes hôte–microbe, où l’organisation spatiale des bactéries le long de la paroi intestinale, ou à travers une couche de mucus, peut déterminer si elles nous protègent ou causent une maladie.
Vérifier que les motifs sont réels
À mesure que ces systèmes deviennent plus élaborés, les scientifiques ont besoin de méthodes fiables pour confirmer que les cellules se retrouvent aux bons endroits et se comportent comme prévu. L’article met en avant des méthodes d’imagerie capables d’observer des cellules vivantes se déplacer et évoluer dans le temps, ainsi que des techniques avancées de marquage et de séquençage qui cartographient les gènes, protéines et métabolites présents à chaque emplacement. Des capteurs intégrés aux puces peuvent suivre l’oxygène, les nutriments, les acides et les forces mécaniques, reliant les conditions locales aux réponses cellulaires. Ensemble, ces outils aident les chercheurs à vérifier qu’un design n’est pas seulement convaincant visuellement mais fidèle fonctionnellement au tissu réel.
Vers où se dirige ce travail
Les auteurs concluent que les systèmes les plus puissants combineront stratégies directes et indirectes : utiliser des puces et des bioprinters pour définir la disposition globale, puis superposer des gels modulables, des textures et des gradients qui permettent aux tissus de mûrir et de se remodeler avec le temps. Ils soulignent aussi des obstacles pratiques — comme l’industrialisation de la fabrication, la réduction de la variabilité entre laboratoires et les questions éthiques liées aux modèles tissulaires humains complexes. Malgré tout, le message est clair : maîtriser l’organisation spatiale est la clé pour transformer les systèmes microphysiologiques en substituts fiables des organes humains, ouvrant de nouvelles perspectives pour étudier le développement, tester des thérapies et adapter la médecine aux patients.
Citation: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Mots-clés: organe-sur-puce, organisation spatiale des cellules, bio-impression 3D, modèles tissulaires microfluidiques, systèmes microphysiologiques